Clear Sky Science · sv
En enskild cells spatiala karta över cis-reglerande element för sjukdomsrelaterade gener i makakens cortex
Varför denna hjärnkarta är viktig
Många hjärnsjukdomar, från schizofreni till Alzheimers, går i familjer — men de DNA‑förändringar som ökar risken sitter ofta i mystiska delar av genomet som inte kodar för proteiner. Den här studien tar sig an den gåtan genom att skapa en detaljerad karta över hur miljontals små DNA‑strömbrytare fungerar i olika celltyper och platser i makakens cortex, våra nära primatgrannar. Genom att koppla dessa strömbrytare till både cellidentitet och mänsklig sjukdomsrisk ger arbetet ett nytt fönster in i varför vissa hjärnceller och regioner är särskilt sårbara vid psykiatriska och neurodegenerativa störningar.
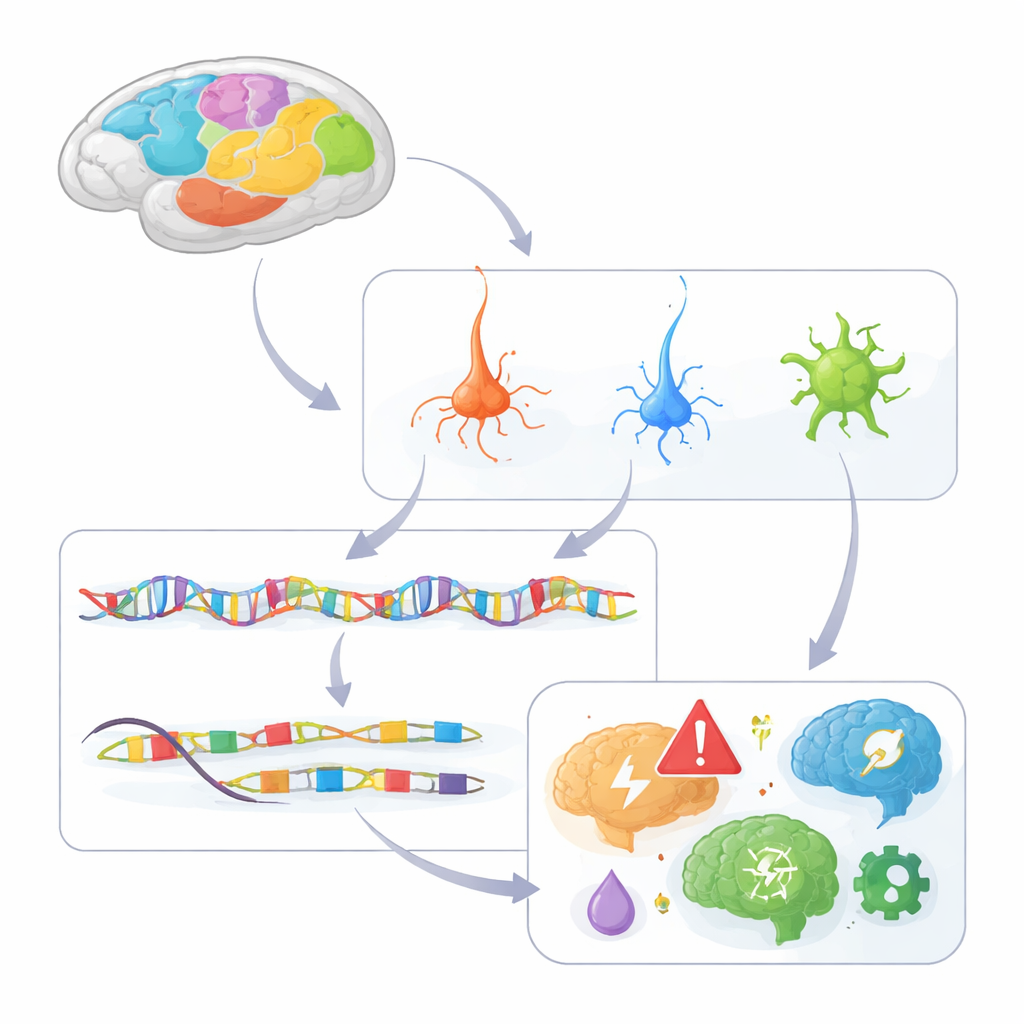
Bygga en cellnivå‑atlas över primatcortex
Forskarlaget analyserade kromatin‑tillgänglighet — hur öppet eller stängt DNA är — i omkring 1,6 miljoner enskilda nukleéer tagna från 142 regioner i makakens cortex. Öppna DNA‑sträckor markerar cis‑reglerande element, de ”på‑/av‑” strömbrytare som kontrollerar närliggande gener. Med en droppbaserad metod kallad single‑nucleus ATAC‑seq grupperade de celler i 230 distinkta typer, som omfattar excitatoriska glutamaterga neuroner, inhibitoriska GABAerga neuroner och olika stödjeceller som astrocyter, oligodendrocyter och mikroglia. De identifierade mer än 600 000 kandidatregulatoriska element och kopplade många av dem till specifika målgener, och byggde därigenom ett första utkast till cortexens regulatoriska kopplingsschema.
Lagrade och regionala mönster i genkontroll
Genom att kombinera denna DNA‑strömbrytarkarta med en högupplöst spatial karta över genaktivitet kunde teamet se var, inom de sex cortexlagren och i olika lober, olika reglerande element var aktiva. Många strömbrytare visade starka preferenser för lager och region. Till exempel var element kopplade till gener som markerar övre lagers neuroner mest aktiva i lager 2 och 3, medan andra begränsades till djupare lager. Vissa strömbrytare var mycket aktiva endast i primära synbarken (V1), vilket hjälper förklara varför vissa neuronstyper och genprogram är unika för denna region. Studien visade också kontraster mellan den evolutionärt äldre piriforma barken och neocortex, med olika uppsättningar strömbrytare aktiva i gliaceller versus djuplagsneuroner, vilket pekar på skilda regulatoriska program som formar dessa arkitekturer.
Primatutvecklingar i viktiga neuronstyper
Genom att jämföra makakdata med liknande kartor från människa och mus fann författarna neuronsubklasser som bara finns hos primater, särskilt vissa lager‑4 glutamaterga neuroner och en specialiserad grupp inhibitoriska celler kallade LAMP5/LHX6‑interneuroner. Dessa celler bar många regulatoriska element som är öppna hos människor och makaker men inte hos möss, och vissa av dessa element verkar ha uppkommit i samband med transposabla element — mobila DNA‑sekvenser som kan bidra till att skapa nya genströmbrytare. De primat‑specifika strömbrytarna reglerar gener inblandade i synaptisk funktion, neuroutveckling och neuronkommunikation, vilket tyder på att relativt nyliga regulatoriska förändringar hjälpt till att diversifiera kortikala kretsar unika för primater, särskilt i lager kopplade till komplex perception och kognition.
Stödceller och kopplingarna bakom plasticitet
Kartan belyser också icke‑neuronala celler. Oligodendrocytprekursorceller och mogna oligodendrocyter visade motsatt förekomst över cortex hierarki: regioner högre i hierarkin hade fler prekursorer och färre mogna myelinbildande celler, vilket antyder större flexibilitet i att justera kopplingar där. Deras regulatoriska element följde denna gradient och var förmånligt förekommande i primat‑biaserade strömbrytare kopplade till synaps‑ och synsystems‑gener. Astrocyter delade upp sig i interlaminära celler koncentrerade i det översta lagret och protoplasmatiska celler distribuerade genom djupare lager, var och en styrd av distinkta uppsättningar strömbrytare och transkriptionsfaktorer. Dessa mönster tyder på att inte bara neuroner, utan också de celler som när och isolerar dem och omformar dem, är fininställda av regionsspecifika regulatoriska program som kan påverka inlärningskapacitet och sårbarhet för skada.
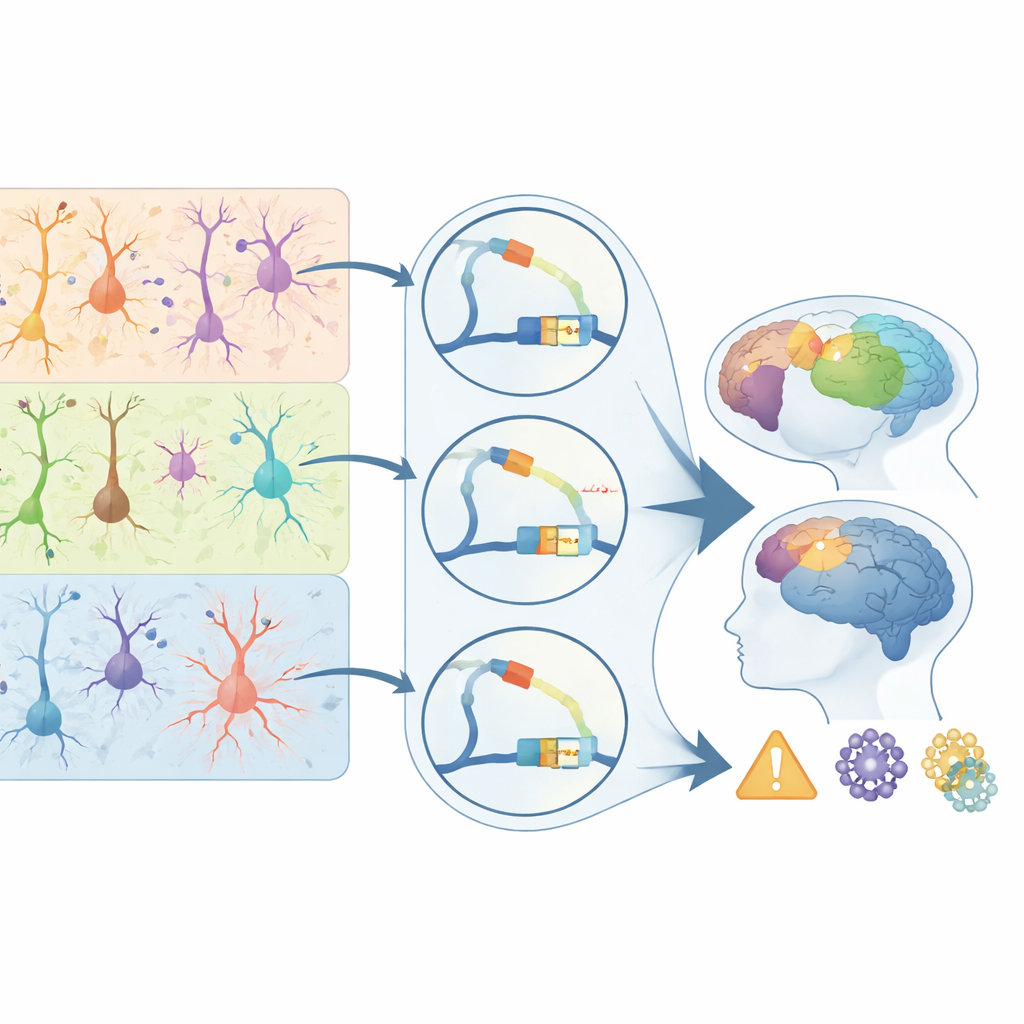
Koppla DNA‑strömbrytare till risk för hjärnsjukdom
För att koppla sin primatatlas till mänsklig hälsa överlagrade författarna den med genetiska studier av 28 hjärnrelaterade sjukdomar och egenskaper. De fann att sjukdomsassocierade varianter faller oproportionerligt ofta i regulatoriska element som är aktiva i specifika celltyper. Riskvarianter för schizofreni och bipolär sjukdom klustrar i strömbrytare som används av övre lags excitatoriska neuroner; epilepsisignaler är berikade i vissa inhibitoriska celler; och Alzheimers riskvarianter koncentreras påfallande i mikroglia‑regulatoriska element. Många av dessa sjukdomsassocierade strömbrytare är primat‑biaserade, särskilt i lager‑4 neuroner för schizofreni och i mikroglia för Alzheimers, och de riktar sig mot gener som påverkar synapser, immunsvar och proteinnedbrytning. För en allmän läsare är huvudbudskapet att sjukdomsrisk ofta inte verkar genom att direkt förstöra proteiner, utan genom att subtilt omkoppla när och var gener slås på i särskilda celler. Denna studie levererar en milstolpekarta över dessa kontrollpunkter i primatcortex, förtydligar varför vissa celltyper och regioner är sjukdoms‑hotspots och erbjuder en vägledning för framtida terapier som syftar till att korrigera hjärnans regulatoriska kod snarare än dess proteindelar.
Citering: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
Nyckelord: enskild-cells epigenomik, primatcortex, genreglering, hjärnsjukdomar, cis-reglerande element