Clear Sky Science · ru
Карта цис-регуляторных элементов на уровне отдельных клеток для генов, связанных с заболеваниями, в коре макаки
Почему эта карта мозга важна
Многие заболевания мозга — от шизофрении до болезни Альцгеймера — имеют семейную предрасположенность, но изменения в ДНК, повышающие риск, часто находятся в загадочных участках генома, которые не кодируют белки. Это исследование решает эту загадку, создавая подробную карту того, как миллионы крошечных переключателей ДНК работают в разных типах клеток и в разных участках коры макаки, нашего близкого приматного родственника. Связывая эти переключатели с идентичностью клеток и риском заболеваний у человека, работа открывает новое окно в понимание того, почему определённые клетки и области мозга особенно уязвимы при психиатрических и нейродегенеративных расстройствах.
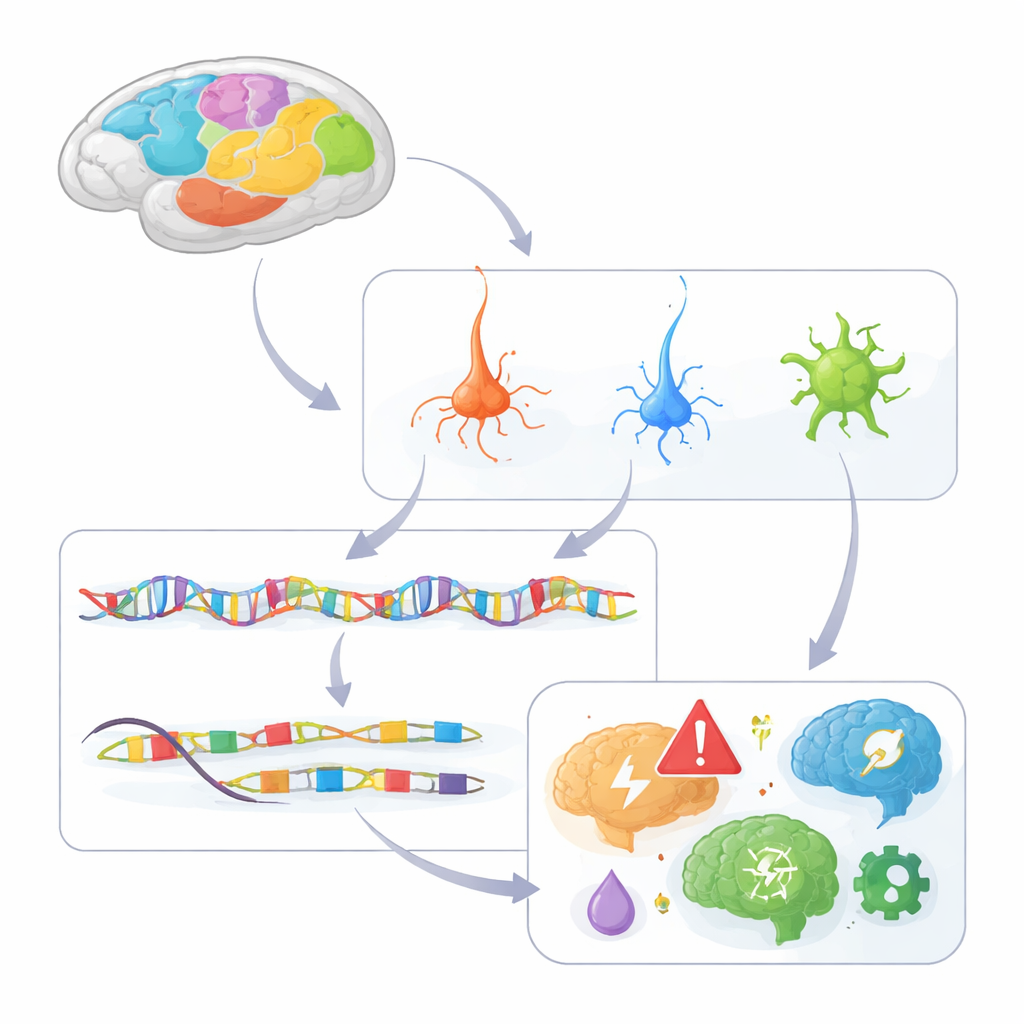
Создание атласа коры примата на уровне клеток
Исследователи проанализировали доступность хроматина — насколько ДНК открыта или закрыта — примерно в 1,6 миллиона отдельных ядер, взятых из 142 регионов коры макаки. Открытые участки ДНК отмечают цис-регуляторные элементы, «включатели-выключатели», контролирующие ближайшие гены. С помощью капельного метода single-nucleus ATAC-seq они сгруппировали клетки в 230 различных типов, охватывающих возбуждающие глутаматергические нейроны, ингибирующие ГАМК-ергические нейроны и различные поддерживающие клетки, такие как астроциты, олигодендроциты и микроглия. Они идентифицировали более 600 000 кандидатных регуляторных элементов и связали многие из них с конкретными целевыми генами, создав первый черновой вариант схемы регуляторных связей коры.
Слоистые и региональные паттерны регуляции генов
Комбинируя этот атлас переключателей ДНК с высокоразрешающей пространственной картой активности генов, команда могла видеть, где внутри шести корковых слоёв и по разным долям коры активны те или иные регуляторные элементы. Многие переключатели демонстрировали выраженные предпочтения по слоям и регионам. Например, элементы, связанные с генами, маркирующими верхние слои нейронов, были активны преимущественно во 2 и 3 слоях, тогда как другие ограничивались глубокими слоями. Некоторые переключатели были сильно активны только в первичной зрительной коре (V1), что помогает объяснить, почему некоторые типы нейронов и генетические программы уникальны для этой области. Исследование также выявило различия между эволюционно более древней обонятельной корой (пирформной) и неокортексом: у глиальных клеток и глубокослойных нейронов работали разные наборы переключателей, указывая на отличающиеся регуляторные программы, формирующие эти архитектуры.
Инновации у приматов в ключевых типах нейронов
Сравнивая данные макаки с подобными картами коры человека и мыши, авторы обнаружили подклассы нейронов, которые встречаются только у приматов, особенно определённые глутаматергические нейроны 4-го слоя и специализированную группу ингибирующих клеток, называемых LAMP5/LHX6 интернейронами. У этих клеток было много регуляторных элементов, открытых у человека и макаки, но не у мышей, и некоторые из этих элементов, по-видимому, возникли вместе с транспозируемыми элементами — подвижными последовательностями ДНК, которые могут способствовать появлению новых генетических переключателей. Примат-специфические переключатели регулируют гены, участвующие в синаптической функции, нейроразвитии и передаче сигналов между нейронами, что указывает на то, что относительно недавние регуляторные изменения способствовали диверсификации корковых цепей, характерной для приматов, особенно в слоях, связанных со сложным восприятием и когнитивными функциями.
Клетки поддержки и механизмы пластичности проводящих путей
Карта также проливает свет на внеклеточные, то есть не нейронные, клетки. Олигодендроцитарные предшественники и зрелые олигодендроциты показали противоположное распределение по иерархии коры: в областях более высокого уровня было больше предшественников и меньше зрелых миелинизирующих клеток, что намекает на большую гибкость в настройке проводящих путей в этих регионах. Их регуляторные элементы следовали этому градиенту и были обогащены примат-ориентированными переключателями, связанными с генами синапсов и зрительной системы. Астроциты разделялись на интерламинарные клетки, сконцентрированные в верхнем слое, и проплазматические клетки, распределённые по глубоким слоям, каждая из которых контролируется набором различных переключателей и транскрипционных факторов. Эти паттерны указывают на то, что не только нейроны, но и клетки, которые их питают, изолируют и перестраивают, настроены регион-специфическими регуляторными программами, которые могут влиять на способность к обучению и уязвимость к повреждениям.
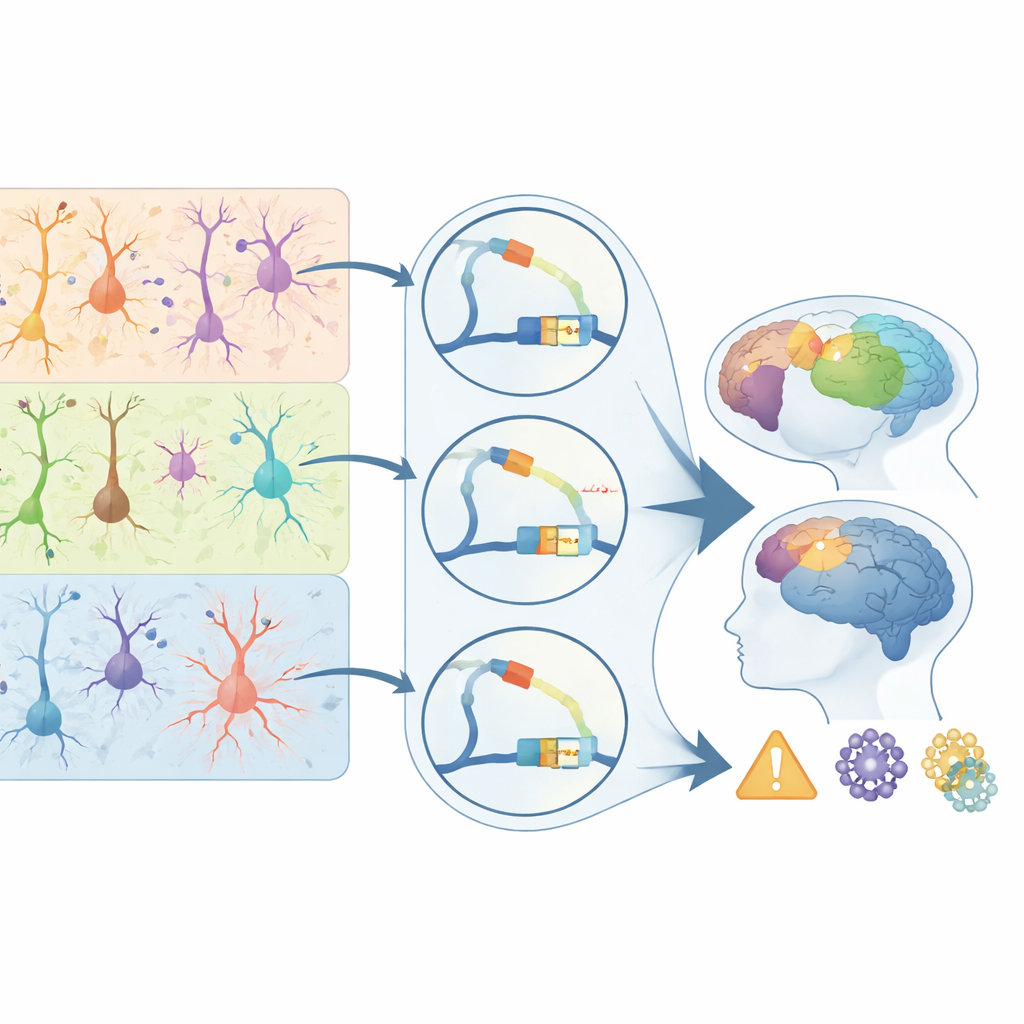
Связывание переключателей ДНК с риском заболеваний мозга
Чтобы связать свой приматный атлас с человеческим здоровьем, авторы наложили его на генетические исследования 28 расстройств и признаков, связанных с мозгом. Они обнаружили, что варианты, связанные с заболеваниями, непропорционально чаще попадают в регуляторные элементы, активные в конкретных типах клеток. Варианты риска шизофрении и биполярного расстройства сосредоточены в переключателях, используемых верхне-слойными возбуждающими нейронами; сигналы эпилепсии обогащены в определённых ингибирующих клетках; а варианты риска болезни Альцгеймера резко концентрируются в регуляторных элементах микроглии. Многие из этих связанных с заболеваниями переключателей смещены в сторону приматов, особенно в нейронах 4-го слоя для шизофрении и в микроглии для болезни Альцгеймера, и они нацелены на гены, известные своим влиянием на синапсы, иммунные ответы и клиренс белков. Для неспециалиста ключевое послание таково: риск заболевания часто действует не путём прямого разрушения белков, а через тонкую перекалибровку того, когда и где включаются гены в отдельных клетках. Это исследование предлагает знаковую карту таких точек контроля в коре приматов, проясняя, почему некоторые типы клеток и области являются очагами заболеваний, и даёт ориентиры для будущих терапий, направленных на исправление регуляторного кода мозга, а не на белковые составляющие.
Цитирование: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
Ключевые слова: эпигеномика отдельных клеток, кора приматов, регуляция генов, заболевания мозга, цис-регуляторные элементы