Clear Sky Science · de
Räumliche Einzelzellkarte cis‑regulatorischer Elemente für krankheitsrelevante Gene im Kortex der Makaken
Warum diese Gehirnkarte wichtig ist
Viele Gehirnerkrankungen, von Schizophrenie bis Alzheimer, treten familiär gehäuft auf – doch die DNA‑Veränderungen, die das Risiko erhöhen, liegen oft in rätselhaften Bereichen des Genoms, die keine Proteine codieren. Diese Studie geht dieses Rätsel an, indem sie eine detaillierte Karte erstellt, wie Millionen winziger DNA‑Schalter in verschiedenen Zelltypen und Lokalisationen im Kortex von Makaken, unseren nahen Verwandten unter den Primaten, funktionieren. Indem diese Schalter sowohl mit Zellidentität als auch mit dem menschlichen Krankheitsrisiko verknüpft werden, eröffnet die Arbeit ein neues Fenster darauf, warum bestimmte Gehirnzellen und -regionen bei psychiatrischen und neurodegenerativen Erkrankungen besonders anfällig sind.
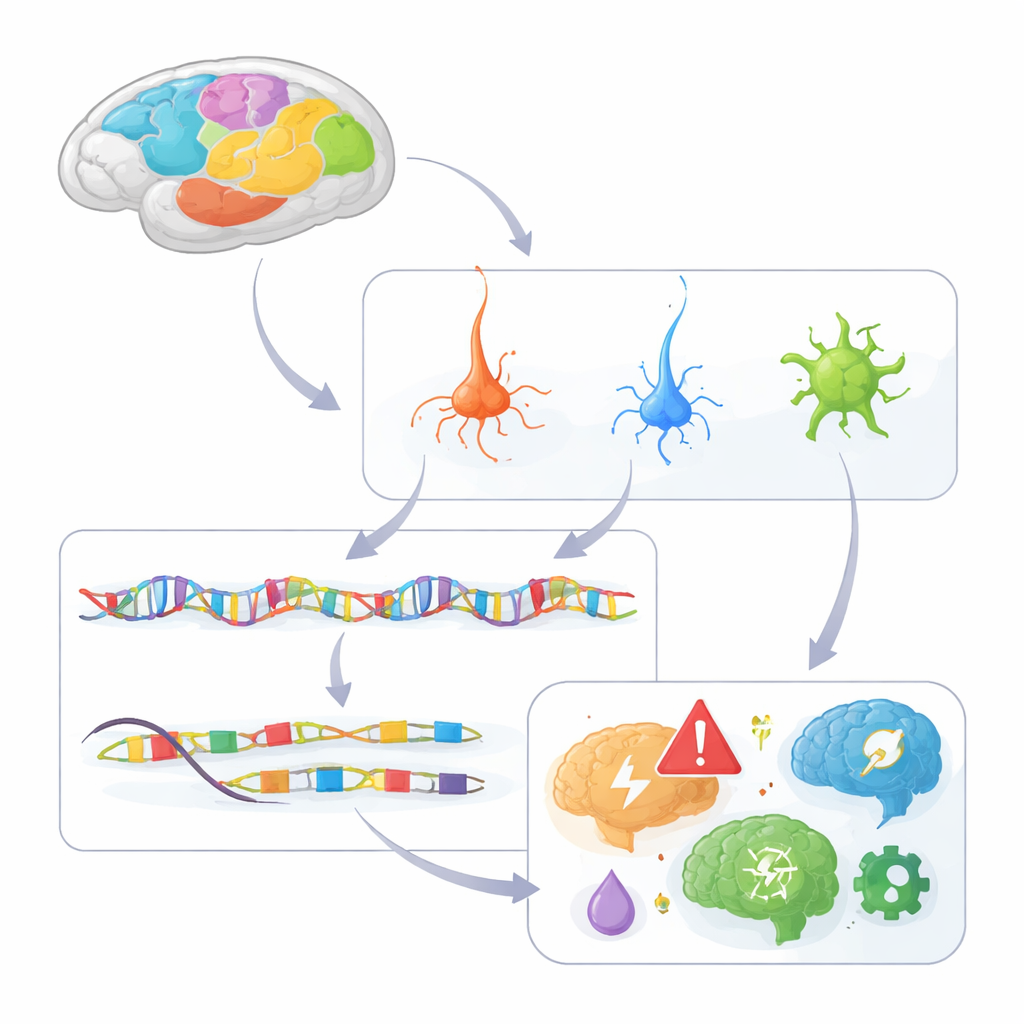
Aufbau eines zellulären Atlas des Primatenkortex
Die Forschenden analysierten die Chromatin‑Zugänglichkeit – wie offen oder geschlossen DNA ist – in etwa 1,6 Millionen einzelnen Zellkernen aus 142 Regionen des Makakenkortex. Offene DNA‑Abschnitte markieren cis‑regulatorische Elemente, die „Ein‑Aus“‑Schalter, die nahegelegene Gene steuern. Mit einer tröpfchenbasierten Methode namens single‑nucleus ATAC‑seq gruppierten sie Zellen in 230 verschiedene Typen, darunter exzitatorische glutamaterge Neurone, inhibitorische GABAerge Neurone und verschiedene Stütz‑ und Hilfszellen wie Astrozyten, Oligodendrozyten und Mikroglia. Sie identifizierten mehr als 600.000 candidate Regulator‑Elemente und verknüpften viele davon mit spezifischen Zielgenen und erstellten so einen ersten Entwurf des regulatorischen Verdrahtungsplans des Kortex.
Geschichtete und regionale Muster der Genkontrolle
Durch die Kombination dieser DNA‑Schalter‑Karte mit einer hochauflösenden räumlichen Karte der Genaktivität konnte das Team erkennen, wo innerhalb der sechs kortikalen Schichten und der verschiedenen Lappen unterschiedliche regulatorische Elemente aktiv sind. Viele Schalter zeigten starke Vorlieben für bestimmte Schichten und Regionen. Elemente, die mit Genen verbunden sind, die Neurone der oberen Schichten markieren, waren beispielsweise vornehmlich in Schicht 2 und 3 aktiv, während andere auf tiefere Schichten beschränkt waren. Bestimmte Schalter waren nur im primären visuellen Kortex (V1) stark aktiv, was dazu beiträgt zu erklären, warum einige Neuronentypen und Genprogramme in dieser Region einzigartig sind. Die Studie offenbarte außerdem Kontraste zwischen dem evolutionär älteren Riechrindenkortex (piriformer Kortex) und dem Neokortex: unterschiedliche Schaltgruppen waren in Gliazellen gegenüber tiefen Schichtneuronen aktiv, was auf unterschiedliche regulatorische Programme hinweist, die diese Architekturen formen.
Primate Innovationen in wichtigen Neuronentypen
Im Vergleich von Makaken‑Daten mit ähnlichen Karten aus menschlichem und Maus‑Kortex fanden die Autorinnen und Autoren Neuronenunterklassen, die nur bei Primaten vorkommen, insbesondere bestimmte Schicht‑4‑glutamaterge Neuronen und eine spezialisierte Gruppe inhibitorischer Zellen, die als LAMP5/LHX6‑Interneurone bezeichnet werden. Diese Zellen trugen viele regulatorische Elemente, die bei Menschen und Makaken offen sind, nicht aber bei Mäusen; einige dieser Elemente scheinen zusammen mit transposablen Elementen entstanden zu sein – mobilen DNA‑Sequenzen, die helfen können, neue Gen‑Schalter zu schaffen. Die primatenspezifischen Schalter regulieren Gene, die an Synapsenfunktion, Neuroentwicklung und neuronaler Kommunikation beteiligt sind, was nahelegt, dass relativ jüngere regulatorische Veränderungen zur Diversifizierung kortikaler Schaltkreise beitrugen, die für Primaten charakteristisch sind, insbesondere in Schichten, die mit komplexer Wahrnehmung und Kognition verbunden sind.
Stützenden Zellen und die Verdrahtung hinter Plastizität
Die Karte beleuchtet auch nicht‑neurale Zellen. Oligodendrozyten‑Vorläuferzellen und reife Oligodendrozyten zeigten entgegengesetzte Häufigkeitsmuster entlang der kortikalen Hierarchie: Höher gelegene Regionen wiesen mehr Vorläufer und weniger reife myelinisierende Zellen auf, was auf größere Flexibilität bei der Anpassung der Verschaltung dort hindeutet. Ihre regulatorischen Elemente spiegelten dieses Gefälle wider und waren angereichert in primaten‑biasierten Schaltern, die an Synapsen‑ und Visus‑Gene gekoppelt sind. Astrozyten teilten sich in interlaminare Zellen, die in der obersten Schicht konzentriert sind, und protoplasmatische Zellen, die in tieferen Schichten verteilt sind, wobei jede Gruppe von unterschiedlichen Schaltern und Transkriptionsfaktoren gesteuert wird. Diese Muster deuten darauf hin, dass nicht nur Neurone, sondern auch die Zellen, die sie ernähren, isolieren und umgestalten, durch regionsspezifische regulatorische Programme abgestimmt sind, die Lernfähigkeit und Anfälligkeit für Schäden beeinflussen können.
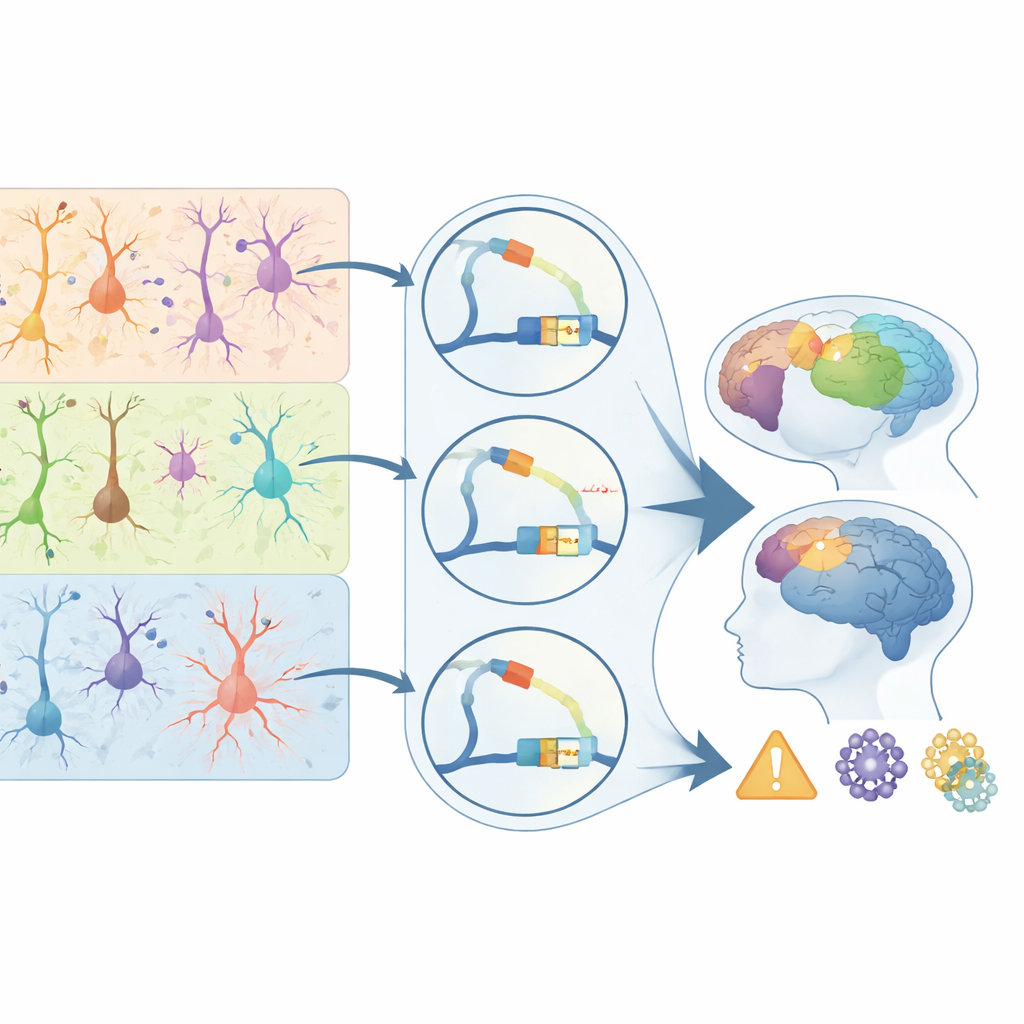
Verknüpfung von DNA‑Schaltern mit Krankheitsrisiko im Gehirn
Um ihren Primatenatlas mit der menschlichen Gesundheit zu verbinden, überlagerten die Autorinnen und Autoren ihn mit genetischen Studien zu 28 gehirnbezogenen Erkrankungen und Merkmalen. Sie stellten fest, dass krankheitsassoziierte Varianten überproportional häufig in regulatorische Elemente fallen, die in spezifischen Zelltypen aktiv sind. Schizophrenie‑ und bipolare Störungs‑Risikovarianten gruppieren sich in Schaltern, die von exzitatorischen Neuronen der oberen Schichten genutzt werden; Epilepsie‑Signale sind in bestimmten inhibitorischen Zellen angereichert; und Alzheimer‑Risikovarianten konzentrieren sich auffällig in mikroglialen regulatorischen Elementen. Viele dieser krankheitsassoziierten Schalter zeigen einen Primaten‑Bias, insbesondere in Schicht‑4‑Neuronen für Schizophrenie und in Mikroglia für Alzheimer, und sie zielen auf Gene ab, die für Synapsen, Immunantworten und Proteinräumung bekannt sind. Für eine breite Leserschaft lautet die Kernbotschaft: Krankheitsrisiko wirkt oft nicht durch direkte Schädigung von Proteinen, sondern indem es subtil neu verdrahtet, wann und wo Gene in bestimmten Zellen an- oder ausgeschaltet werden. Diese Studie liefert eine landmarkenhafte Karte dieser Kontrollpunkte im Primatenkortex, klärt, warum einige Zelltypen und Regionen Krankheits‑Hotspots sind, und bietet einen Leitfaden für künftige Therapien, die darauf abzielen, den regulatorischen Code des Gehirns zu korrigieren statt nur seine Proteine.
Zitation: Meng, J., Chen, C., Zhu, Z. et al. Single-cell spatial map of cis-regulatory elements for disease-related genes in the macaque cortex. Nat Commun 17, 4041 (2026). https://doi.org/10.1038/s41467-026-70497-x
Schlüsselwörter: Einzelzell-Epigenomik, Primatenkortex, Genregulation, Erkrankungen des Gehirns, cis‑regulatorische Elemente