Clear Sky Science · zh
通过本体强化迭代实现功能性蛋白设计与增强
教会计算机构建更优的蛋白质
蛋白质在生物细胞内承担几乎所有重要工作,从分解食物到抵抗感染。科学家希望按需设计新蛋白,例如更坚固的工业用酶或更好的医学工具,但将计算机的构想变成真实可用的分子仍然很困难。本研究介绍了一个名为 ORI 的新系统,它将人工智能与实验室实验直接相连,目标是让蛋白质设计更快、更可靠且更易控。
为何蛋白设计如此艰难
每种蛋白质由一长串氨基酸构成,这条链上的微小改动就能显著改变分子的折叠和行为。现代人工智能可以预测蛋白质结构,甚至生成新序列,但计算机上看起来不错的设计与试验管中真正有用的分子之间仍存在顽固差距。许多设计因不稳定、不能正确折叠或缺乏期望活性而失败,迫使研究者依赖缓慢的反复试验。
计算与实验之间的闭环
ORI 框架通过在人工智能模型与实际实验之间建立反馈闭环来解决这一问题 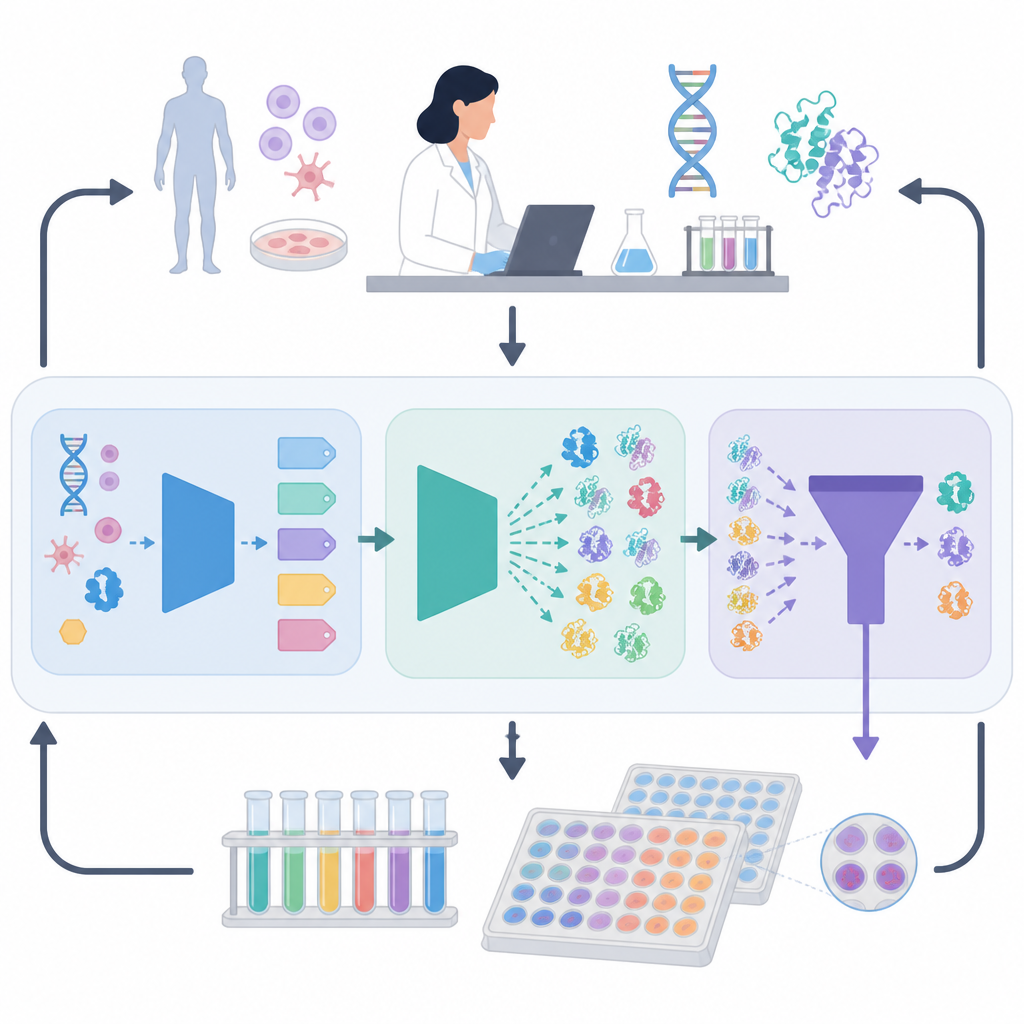
从实验反馈中学习
ORI 的不同之处在于它不仅停留在预测上,而是从实验的成功与失败中学习。被选出的蛋白设计将被合成并测试其表达情况、活性以及在应激条件下的表现。随后,这些结果通过一种借鉴强化学习的策略反馈回人工智能,使系统逐步偏好在现实中表现良好的序列模式,而不仅仅是在纸面上优秀。经过多轮迭代,人工智能在提出能够通过现实考验的候选序列方面表现得更好 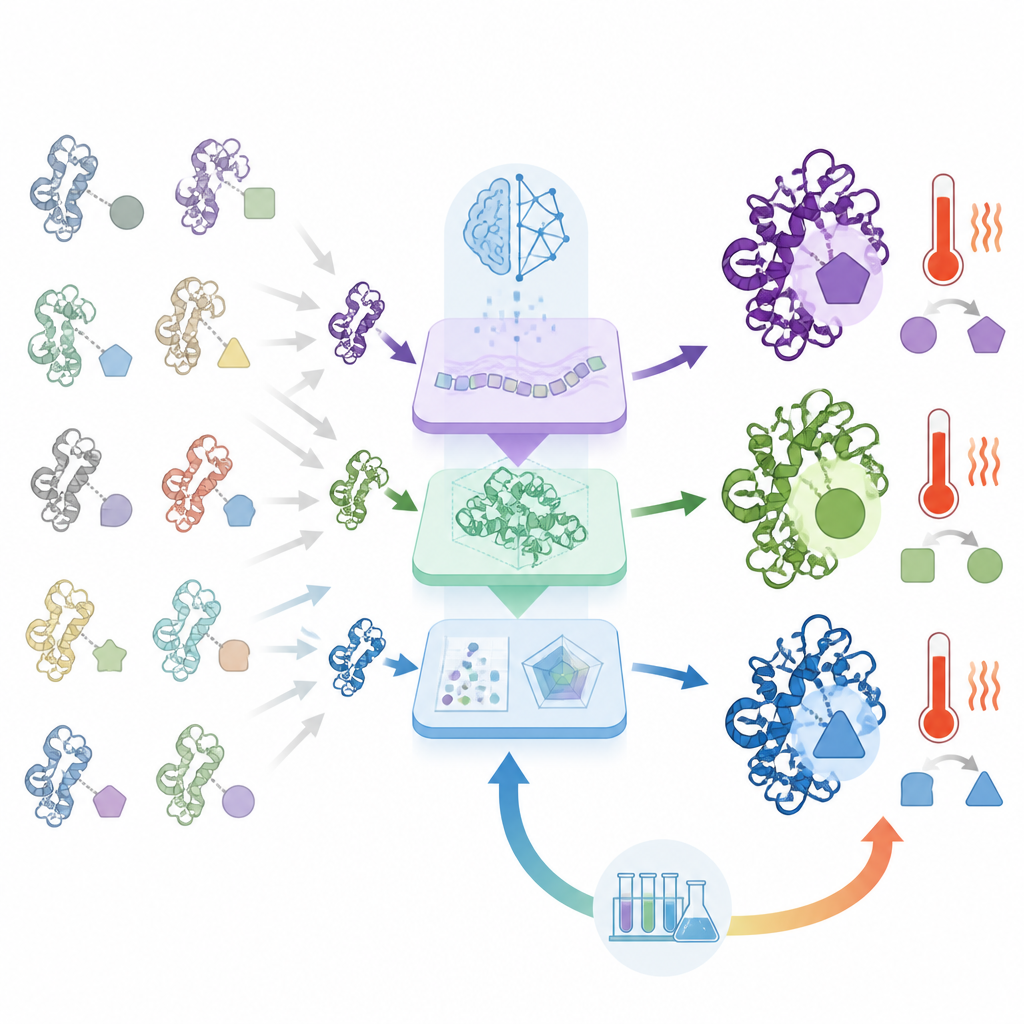
构建更强、更耐热和具双重功能的酶
为展示 ORI 的能力,作者将其应用于若干酶设计挑战。针对溶菌酶(可分解细菌细胞壁),系统生成了大量变体,并在从实验反馈中学习后,产出了活性远高于天然溶菌酶的版本,其中一个的活性大约比标准参考高出一百倍。ORI 还用于设计几丁酶——分解昆虫外壳和真菌中几丁质的酶。通过引导模型朝耐热特性优化,团队创造了在约85摄氏度仍能保持活性的几丁酶,远超大多数天然版本所能耐受的温度。最后,该系统还设计出将溶菌酶和几丁酶活性合而为一的单一蛋白,其中一些双功能酶在两项任务中都超越了它们在各自专长上的天然对应物。
探索蛋白可能性的全新途径
对非专业读者来说,关键思想是 ORI 将蛋白设计变成计算模型与湿实验室之间的持续对话,而非一次性预测。该系统使用有关蛋白类型与属性的结构化知识来引导其想象力,并认真倾听每项实验对新设计的反馈。通过不断循环这一流程,ORI 不仅能匹配天然蛋白,有时还可在强度、耐热性或多功能性上超越它们。这预示着一个未来:为医学、工业和环境用途定制的蛋白质可以更高效且更有把握地开发出来。
引用: He, B., Qin, C., Zhao, Y. et al. Functional protein design and enhancement with ontology reinforcement iteration. Nat Commun 17, 4158 (2026). https://doi.org/10.1038/s41467-026-69855-6
关键词: 蛋白工程, 酶设计, 人工智能, 耐热酶, 多功能蛋白