Clear Sky Science · sv
Funktionell proteindesign och förbättring med ontologisk förstärkningsiteration
Lära datorer att bygga bättre proteiner
Proteiner utför nästan allt arbete inne i levande celler, från att bryta ner föda till att bekämpa infektioner. Forskare vill gärna designa nya proteiner på begäran, såsom tåligare industriella enzymer eller bättre medicinska verktyg, men att omvandla datoridéer till verkliga, fungerande molekyler är fortfarande svårt. Den här studien introducerar ett nytt system kallat ORI som kopplar artificiell intelligens direkt till laboratorieexperiment, med målet att göra proteindesign snabbare, mer tillförlitlig och lättare att kontrollera.
Varför det är så svårt att designa proteiner
Varje protein byggs av en lång kedja av aminosyror, och små förändringar i den kedjan kan dramatiskt ändra hur molekylen viks och beter sig. Modern AI kan förutsäga proteiners former och till och med generera nya sekvenser, men det finns en envis klyfta mellan vad som ser lovande ut i en dator och vad som faktiskt fungerar i ett provrör. Många designer misslyckas eftersom de är instabila, inte viks korrekt eller saknar önskad aktivitet, vilket tvingar forskare att förlita sig på långsam trial-and-error.
En sluten loop mellan dator och laboratorium
ORI-ramverket tar itu med detta problem genom att skapa en återkopplingsslinga mellan AI-modeller och verkliga experiment 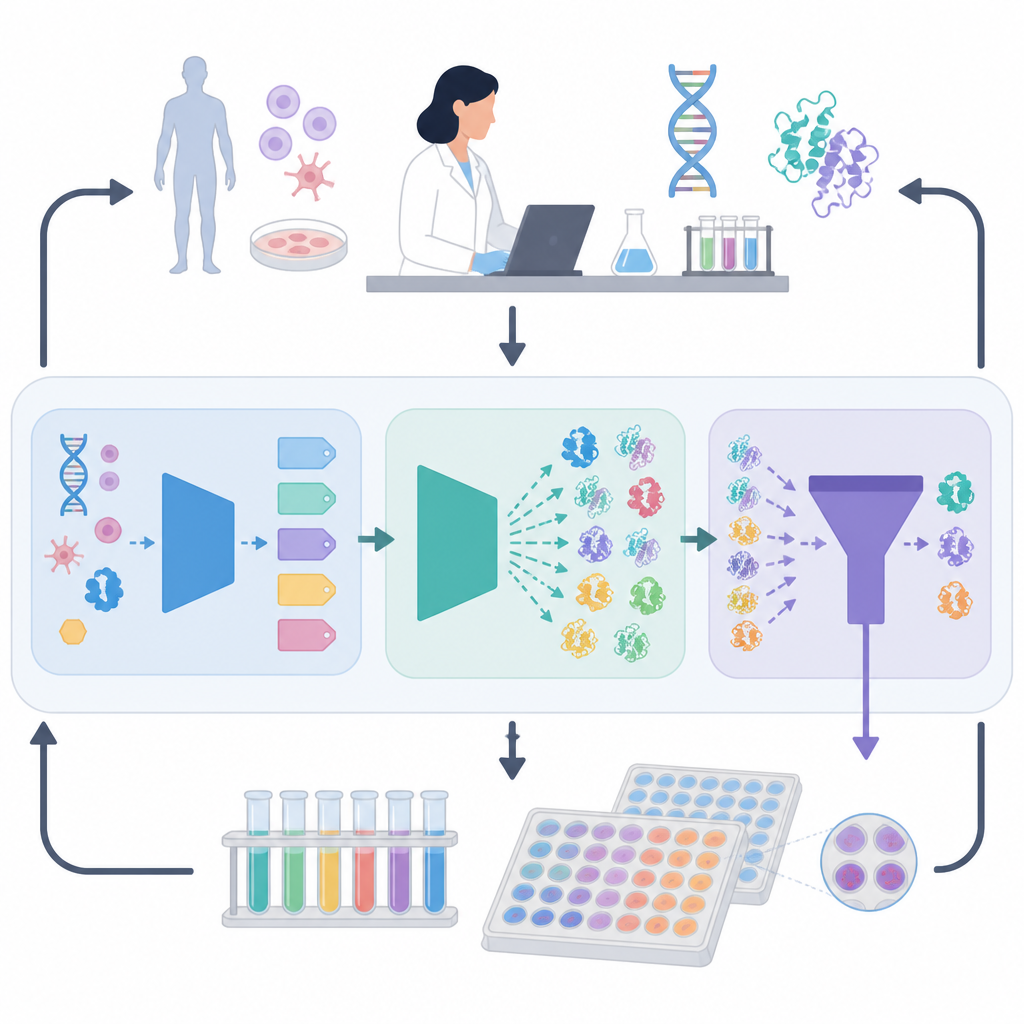
Lärande från experimentell återkoppling
Det som gör ORI annorlunda är att den inte stannar vid förutsägelse; den lär sig av laboratoriets framgångar och misslyckanden. Utvalda proteindesigner syntetiseras och testas för hur väl de uttrycks, hur aktiva de är och hur de beter sig under påfrestning. Dessa resultat matas sedan tillbaka till AI:n med en strategi anpassad från förstärkningsinlärning, vilket gör att systemet gradvis favoriserar sekvensmönster som presterar väl i verkligheten snarare än bara på papper. Över flera omgångar blir AI:n bättre på att föreslå kandidater som klarar denna verkliga prövning 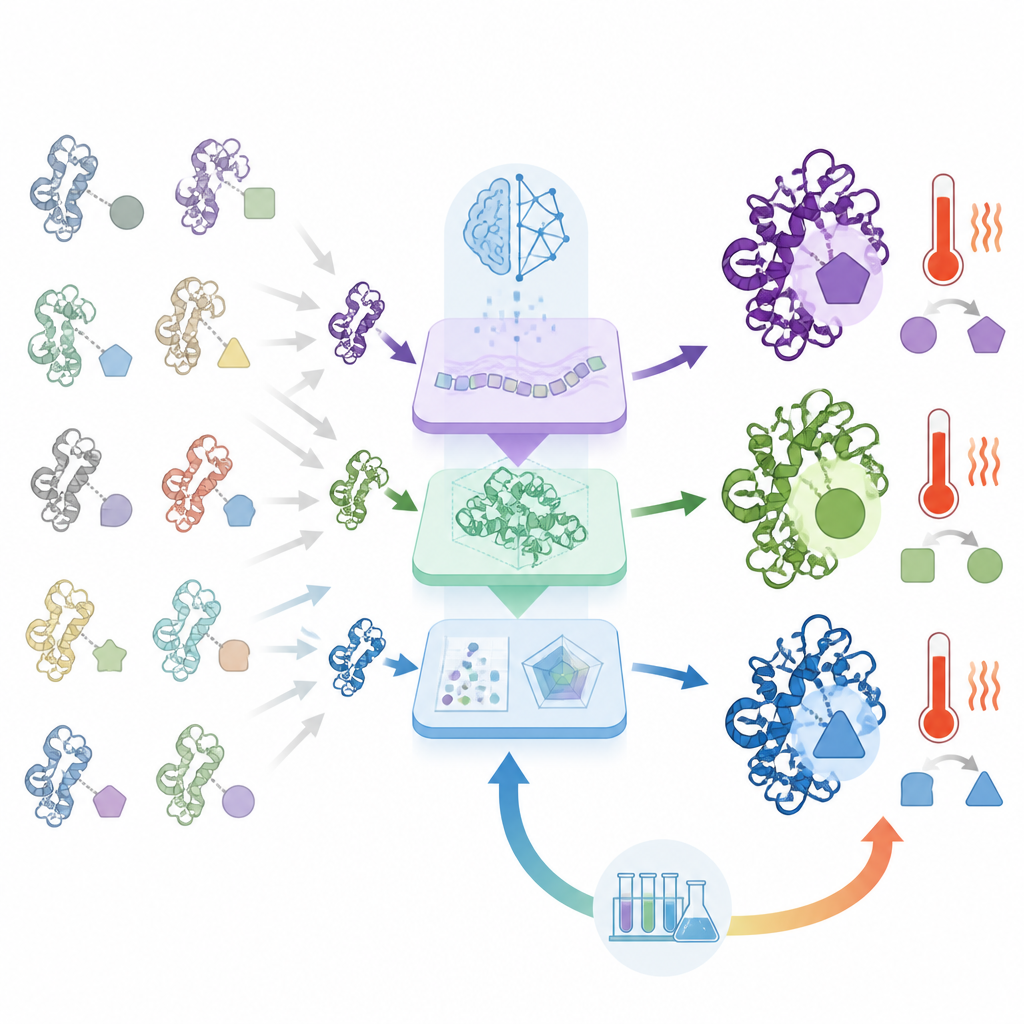
Bygga starkare, hetare och dubbelverkande enzymer
För att visa vad ORI kan göra tillämpade författarna det på flera utmaningar inom enzymdesign. För lysozymer, som bryter ner bakteriella cellväggar, genererade systemet många varianter och efter att ha lärt sig från experimentell återkoppling producerade det versioner med mycket högre aktivitet än naturliga lysozymer, inklusive en som var ungefär hundra gånger mer aktiv än en standardreferens. ORI användes också för att designa kitinaser, enzymer som bryter ner kitin som finns i insektskal och svampar. Genom att styra modellen mot värmetåliga egenskaper skapade teamet kitinaser som förblev aktiva vid temperaturer kring 85 grader Celsius, långt bortom vad de flesta naturliga varianter tål. Slutligen konstruerade systemet enskilda proteiner som kombinerar både lysozym- och kitinasaktivitet, och några av dessa dubbelverkande enzymer överträffade sina specialiserade naturliga motsvarigheter i båda uppgifterna.
Ett nytt sätt att utforska proteinmöjligheter
För icke-specialister är huvudidén att ORI förvandlar proteindesign till en pågående konversation mellan datormodeller och våtlabbet, snarare än en engångsförutsägelse. Systemet använder strukturerad kunskap om proteintyper och egenskaper för att styra sin fantasi, och det lyssnar noga på vad experimenten säger om varje ny design. Genom att loopa igenom denna process kan ORI inte bara matcha naturliga proteiner utan ibland överträffa dem i styrka, värmetålighet eller mångsidighet. Detta antyder en framtid där skräddarsydda proteiner för medicin, industri och miljöändamål kan utvecklas mer effektivt och med större förtroende.
Citering: He, B., Qin, C., Zhao, Y. et al. Functional protein design and enhancement with ontology reinforcement iteration. Nat Commun 17, 4158 (2026). https://doi.org/10.1038/s41467-026-69855-6
Nyckelord: proteinengineering, enzymdesign, artificiell intelligens, termostabila enzymer, multifunktionella proteiner