Clear Sky Science · de
Funktionelles Proteindesign und Optimierung durch Ontologie-verstärkte Iteration
Computern beibringen, bessere Proteine zu bauen
Proteine übernehmen nahezu alle Aufgaben in lebenden Zellen, vom Aufschließen von Nahrungsbestandteilen bis zur Abwehr von Infektionen. Wissenschaftler würden gerne auf Nachfrage neue Proteine entwerfen — etwa robustere Industrieenzyme oder verbesserte medizinische Werkzeuge — doch die Umsetzung von Computerentwürfen in reale, funktionale Moleküle ist weiterhin schwierig. Diese Studie stellt ein neues System namens ORI vor, das künstliche Intelligenz direkt mit Laborversuchen verbindet, mit dem Ziel, das Proteindesign schneller, verlässlicher und besser steuerbar zu machen.
Warum Proteindesign so schwierig ist
Jedes Protein besteht aus einer langen Kette von Aminosäuren, und kleinste Veränderungen in dieser Kette können die Faltung und das Verhalten des Moleküls dramatisch verändern. Moderne KI kann Proteinstrukturen vorhersagen und sogar neue Sequenzen erzeugen, aber es besteht eine hartnäckige Lücke zwischen dem, was im Computer vielversprechend aussieht, und dem, was im Reagenzglas tatsächlich funktioniert. Viele Entwürfe scheitern, weil sie instabil sind, sich nicht richtig falten oder die gewünschte Aktivität vermissen lassen, sodass Forschende auf langsame Versuchs- und Irrtumsverfahren angewiesen sind.
Ein geschlossener Kreislauf zwischen Computer und Labor
Das ORI-Framework begegnet diesem Problem, indem es eine Rückkopplungsschleife zwischen KI-Modellen und realen Experimenten schafft 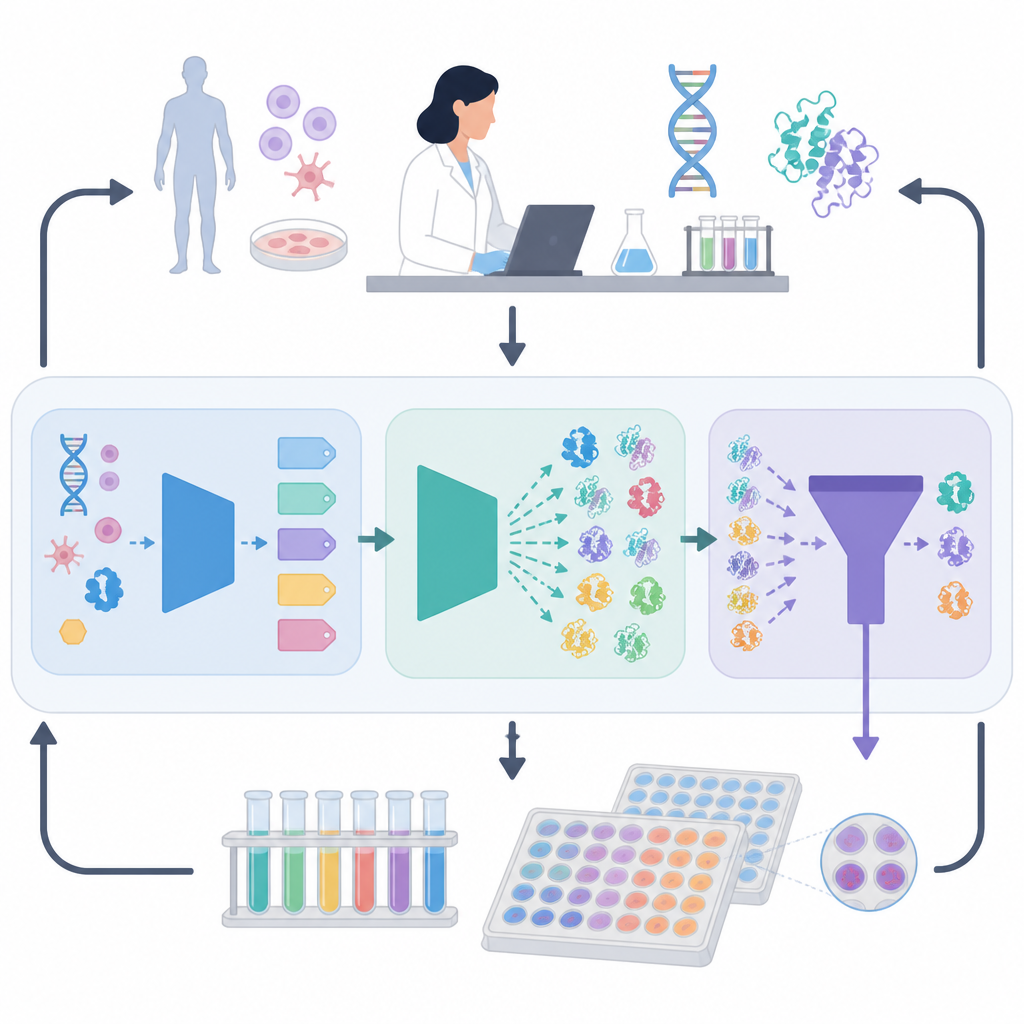
Vom experimentellen Feedback lernen
Was ORI unterscheidet, ist, dass es nicht bei der Vorhersage stehen bleibt, sondern aus den Erfolgen und Misserfolgen des Labors lernt. Ausgewählte Proteinentwürfe werden synthetisiert und daraufhin getestet, wie gut sie exprimierbar sind, wie aktiv sie sind und wie sie sich unter Stress verhalten. Diese Ergebnisse fließen dann mittels einer an Verstärkungslernen angelehnten Strategie zurück in die KI, sodass das System allmählich Sequenzmuster bevorzugt, die in der Praxis gut funktionieren, statt lediglich auf dem Papier überzeugend zu sein. Über mehrere Runden hinweg wird die KI besser darin, Kandidaten vorzuschlagen, die diese realen Prüfungen bestehen 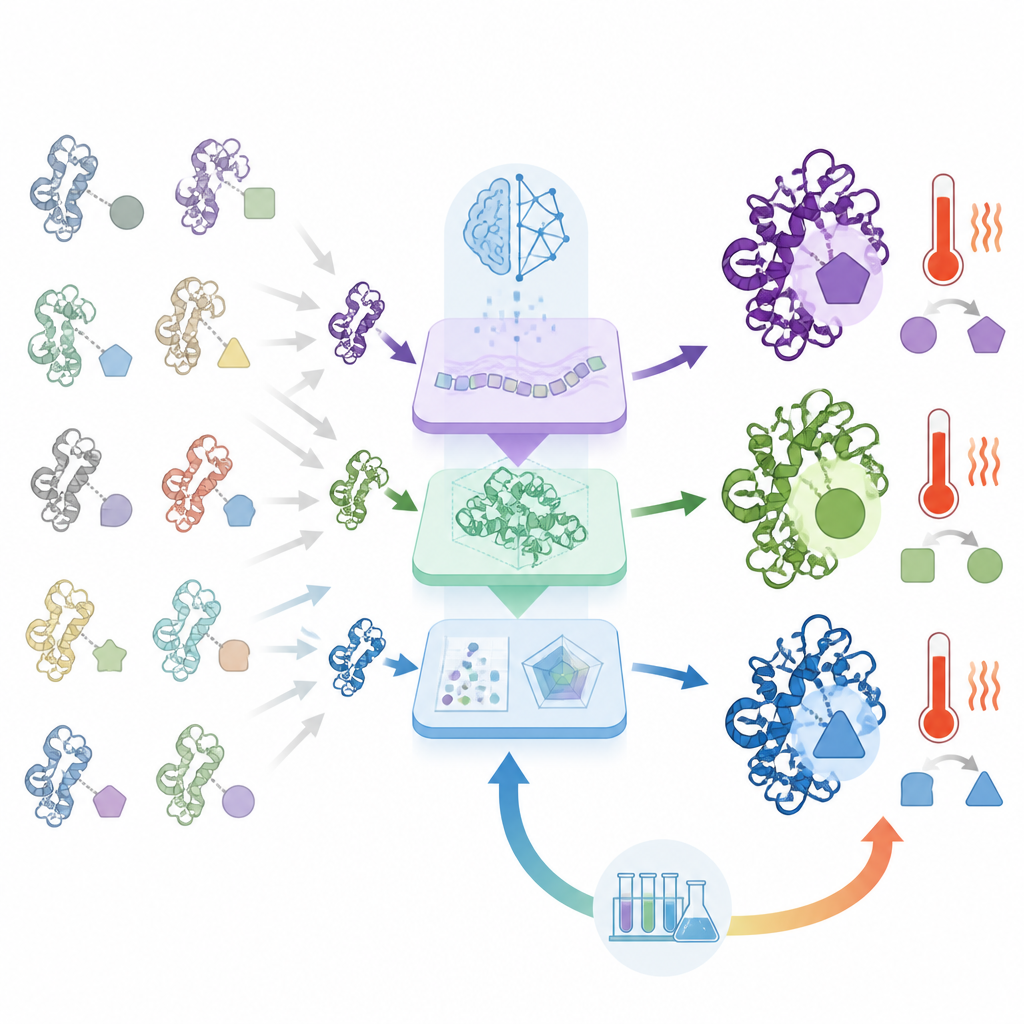
Stärkere, hitzebeständigere und dual-funktionale Enzyme entwickeln
Um die Fähigkeiten von ORI zu demonstrieren, wendeten die Autoren das System auf mehrere Enzymdesign-Aufgaben an. Bei Lysozymen, die bakterielle Zellwände abbauen, erzeugte das System viele Varianten und brachte nach dem Lernen aus experimentellem Feedback Versionen hervor, deren Aktivität deutlich über der natürlicher Lysozyme lag — einschließlich einer Variante, die etwa hundertmal aktiver war als eine Standardreferenz. ORI wurde auch zur Gestaltung von Chitinasen eingesetzt, Enzymen, die Chitin aus Insektenpanzern und Pilzen abbauen. Indem das Modell in Richtung hitzeresistenter Merkmale gelenkt wurde, entstanden Chitinasen, die bei Temperaturen um 85 Grad Celsius aktiv blieben — weit über dem, was die meisten natürlichen Varianten aushalten. Schließlich konstruierte das System einzelne Proteine, die sowohl Lysozym- als auch Chitinase-Aktivität vereinen; einige dieser Doppelaktivitäts-Enzyme übertrafen ihre spezialisierten natürlichen Gegenstücke in beiden Aufgaben.
Ein neuer Weg, Proteinmöglichkeiten zu erkunden
Für Nicht-Fachleute ist die zentrale Idee, dass ORI das Proteindesign in einen fortlaufenden Dialog zwischen Computermodellen und dem Nasslabor verwandelt, statt in eine einmalige Vorhersage. Das System nutzt strukturiertes Wissen über Proteintypen und -eigenschaften, um seine „Vorstellungskraft“ zu leiten, und hört genau darauf, was Experimente über jeden neuen Entwurf aussagen. Durch wiederholtes Durchlaufen dieses Prozesses kann ORI nicht nur natürliche Proteine erreichen, sondern sie in Stärke, Hitzebeständigkeit oder Vielseitigkeit teilweise übertreffen. Das deutet auf eine Zukunft hin, in der maßgeschneiderte Proteine für Medizin, Industrie und Umweltanwendungen effizienter und mit größerer Zuverlässigkeit entwickelt werden können.
Zitation: He, B., Qin, C., Zhao, Y. et al. Functional protein design and enhancement with ontology reinforcement iteration. Nat Commun 17, 4158 (2026). https://doi.org/10.1038/s41467-026-69855-6
Schlüsselwörter: Proteinengineering, Enzymdesign, künstliche Intelligenz, thermostabile Enzyme, multifunktionale Proteine