Clear Sky Science · zh
ASB7通过泛素介导的ATF2降解促进骨肉瘤肺转移
为何失控的骨肿瘤令人关注
骨肉瘤是一种少见但侵袭性强的骨癌,主要发生于儿童、青少年和老年人。其最致命的特点是容易向肺部转移,常将可局部治疗的疾病变为危及生命的状态。本研究提出了一个简单却关键的问题:哪些分子“开关”帮助骨肉瘤细胞脱离骨组织、在体内迁移并在肺部定植——这些开关能否被重新关闭?
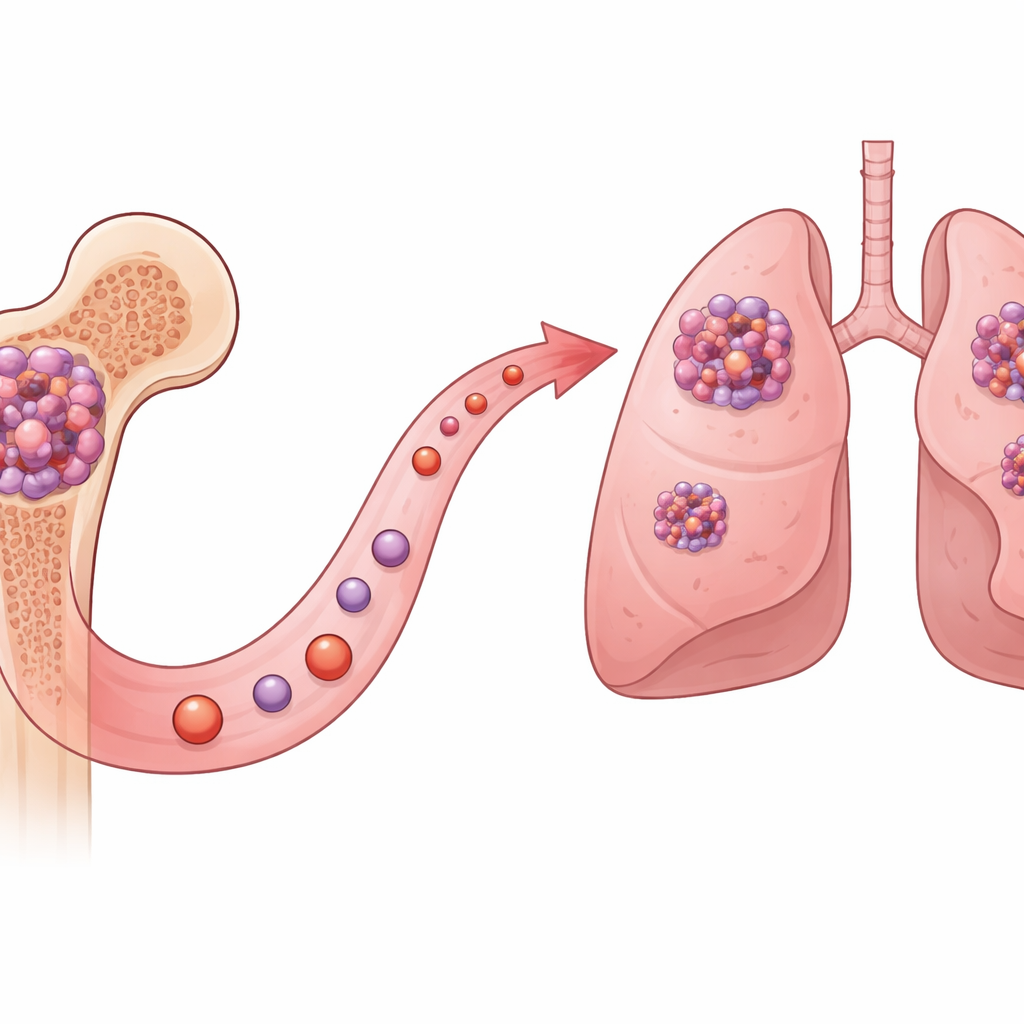
癌症扩散的隐秘帮手
研究者将注意力集中在一种名为ASB7的蛋白上,此前已知其参与细胞对其他蛋白的降解。通过挖掘大型公共癌症数据库并分析患者肿瘤样本,他们发现骨肉瘤细胞常携带ASB7基因的拷贝增加并产生异常高水平的ASB7蛋白。肿瘤中ASB7含量高的患者通常预后较差,这提示该分子不仅仅是常规的细胞保洁者——它似乎在促进肿瘤更具侵袭性方面发挥作用。
从平滑细胞到四处游走的入侵者
为了弄清ASB7在癌细胞中的实际作用,团队构建了过表达或缺失ASB7的骨肉瘤细胞系。当ASB7水平升高时,细胞长出许多由肌动蛋白构成的细长指状和扇形突起,正是正常细胞用来爬行的支架结构。这些ASB7高表达细胞在体外迁移实验中移动更快,并能穿透模拟体内组织的凝胶。在小鼠胫骨植入实验中,它们在肺部形成的转移灶也明显更多。去除ASB7则产生相反效果:细胞失去突起、迁移能力下降,并且肺转移显著减少,而细胞增殖速度变化不大。
被拆解的保护性“刹车”
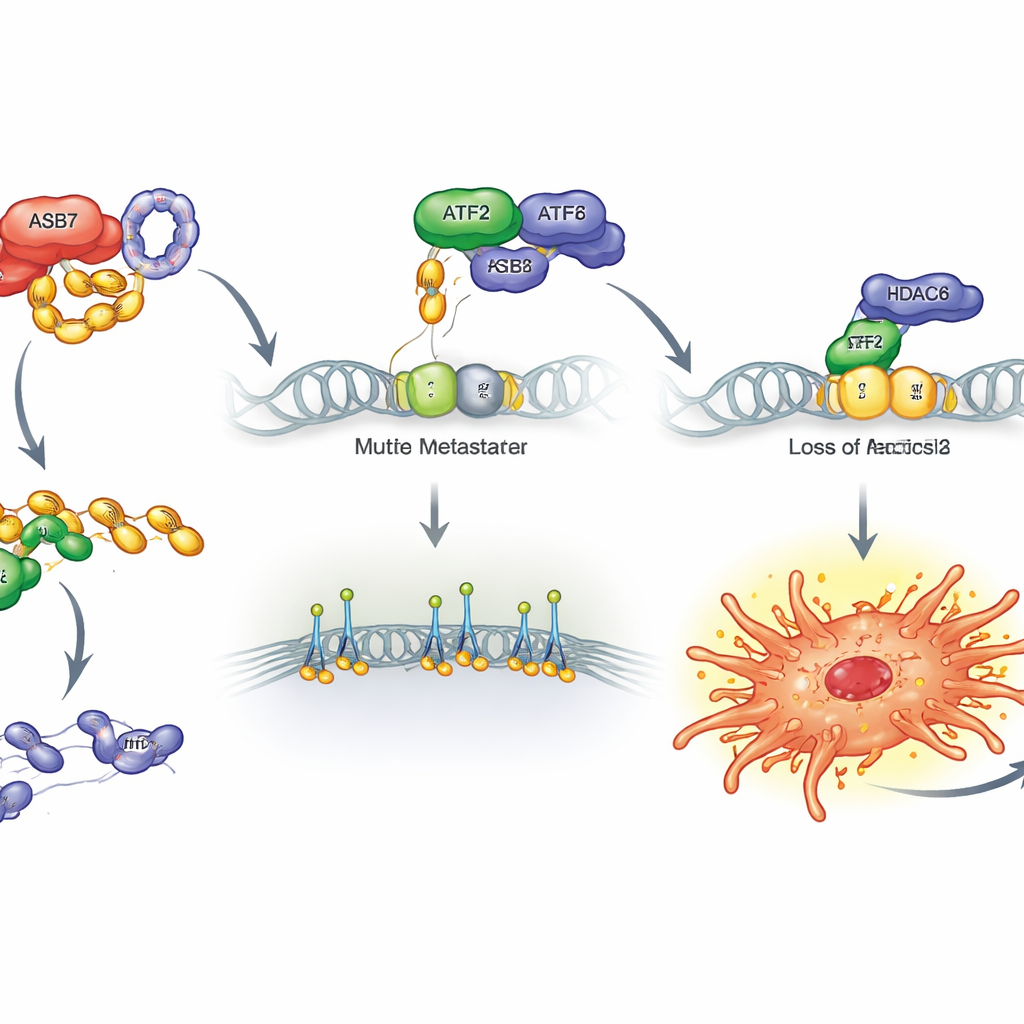
进一步研究表明,另一个蛋白ATF2是抑制转移的重要“刹车”。ATF2是一种转录因子,能与DNA结合并帮助控制基因的开启。在患者样本和大型蛋白数据集中,ASB7含量高的肿瘤通常ATF2含量低,ATF2低的患者预后不佳。在骨肉瘤细胞中提高ATF2可减少突起、减慢迁移和侵袭,并在小鼠中减少肺转移;删除ATF2则产生相反效应。生化实验证明了其机制:ASB7与其伙伴CUL5联手,在ATF2的特定位点上标记小的泛素分子,将其标记为细胞蛋白降解机器的降解目标。由于ATF2持续被降解,其抑制有害基因的能力随之丧失。
解除对外周环境的关键束缚
接着,团队探查了ATF2通常抑制哪些基因。通过将基因表达谱与公共的DNA结合位点图谱结合,他们锁定了ITGB2——整合素家族的一员,这类蛋白将细胞与外部微环境连接,并帮助细胞向前牵拉。ATF2通常位于ITGB2基因附近,并与另一种蛋白HDAC6共同维持其沉默状态。当ASB7促使ATF2被破坏时,这种协同被打破,HDAC6的结合减少,ITGB2得以被强烈激活。实验证实了这一链条:升高ASB7或删除ATF2会增加ITGB2,而提高ATF2或去除ASB7会降低ITGB2。单独强制过表达ITGB2即可增强突起、迁移、侵袭并在小鼠中促进肺定植,而去除ITGB2则削弱了这些行为。
这对未来治疗意味着什么
总体来看,这项工作勾画出骨肉瘤细胞获得转移能力的一条清晰路径。ASB7充当分子“杀手”,摧毁ATF2,削弱其与HDAC6在ITGB2基因处的协作。这释放了ITGB2及相关基因,使肿瘤细胞在侵入血管并在肺中定植时获得更强的附着力和运动能力。由于该通路在骨肉瘤中特别活跃,这提示了若干有前景的治疗策略:阻断ASB7活性、稳定ATF2、抑制ITGB2或调节相关的DNA沉默机制,均可能有助于阻止骨肉瘤转移,从而把一种常致命的疾病转变为更易管理的状态。
引用: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
关键词: 骨肉瘤, 转移, ASB7, ATF2, 整合素