Clear Sky Science · ar
ASB7 يعزز نقائل الساركوما العظمية إلى الرئتين عبر التحلل المحدّد باليوبيكويتين لـ ATF2
لماذا تهم أورام العظام الهاربة
الساركومة العظمية سرطان عظمي نادر لكنه عدواني يصيب أساسًا الأطفال والمراهقين وكبار السن. وأخطر ما يميزه هو ميله للانتشار إلى الرئتين، مما يحول في كثير من الأحيان مرضًا موضعيًا قابلًا للعلاج إلى حالة تهدد الحياة. تطرح هذه الدراسة سؤالًا بسيطًا لكنه حاسم: ما هي «مفاتيح» جزيئية تساعد خلايا الساركومة العظمية على الانفصال عن العظم، والسفر عبر الجسم، والاستعمار في الرئتين—وهل يمكن إعادة إيقاف هذه المفاتيح؟
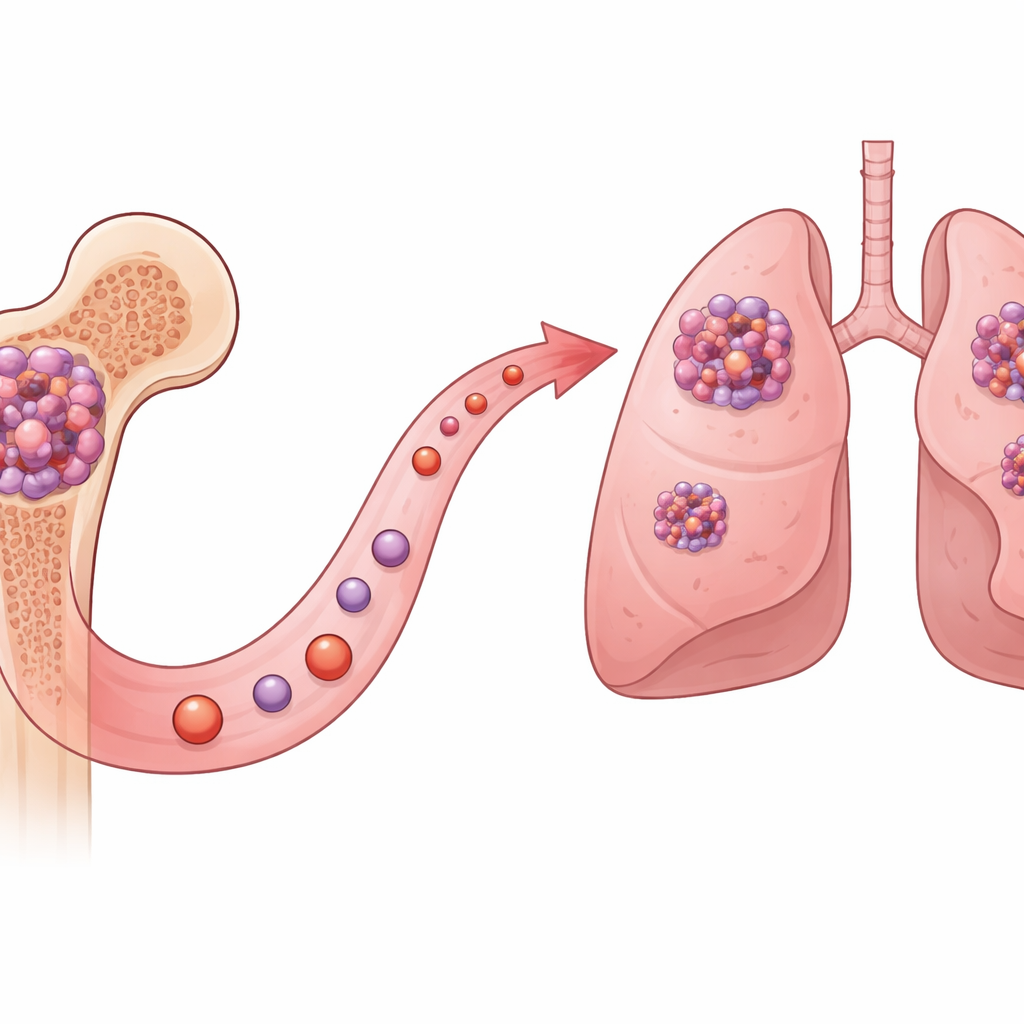
مساعد خفي لانشار السرطان
ركّز الباحثون على بروتين يدعى ASB7، كان معروفًا سابقًا بمساعدته الخلايا على التخلص من بروتينات أخرى. من خلال تنقيب مجموعات بيانات سرطانية عامة كبيرة وتحليل عينات أورام مرضى، وجدوا أن خلايا الساركومة العظمية كثيرًا ما تحمل نسخًا زائدة من جين ASB7 وتنتج كميات غير معتادة من بروتين ASB7. المرضى الذين كانت أورامهم غنية بـ ASB7 كانوا يميلون إلى بقاء أقل، مما يوحي أن هذه الجزئية تؤدي دورًا يتجاوز مجرد أعمال التنظيف الروتينية—فهي تبدو أنها تساعد الأورام لتتصرف بشكل أكثر عدوانية.
من خلايا ملساء إلى غزاة جوالين
لمعرفة ما يفعله ASB7 فعليًا في خلايا السرطان، صمّم الفريق خلايا ساركومة عظمية لتعبر إما عن ASB7 بكمية زائدة أو تفتقر إليه. عند رفع مستويات ASB7، نشأت لدى الخلايا نتوءات رفيعة على شكل أصابع ومراوح مبنية من الأكتين، نفس الهياكل التي تستخدمها الخلايا الطبيعية للحركة. هذه الخلايا العالية في ASB7 تحركت أسرع عبر حجرات الاختبار المختبرية وغَزَت هلامًا يحاكي نسيج الجسم. عند زراعتها في عظام أرجل الفئران، كانت أكثر عرضة لتأسيس مستعمرات عديدة في الرئتين. وإزالة ASB7 أعطت تأثيرًا معاكسًا: فقدت الخلايا نتؤاتها، وهاجرت بشكل ضعيف، وشكلت نقائل رئوية أقل بكثير، دون تغييرات كبيرة في سرعة انقسامها.
فرامل حامية تُفكك
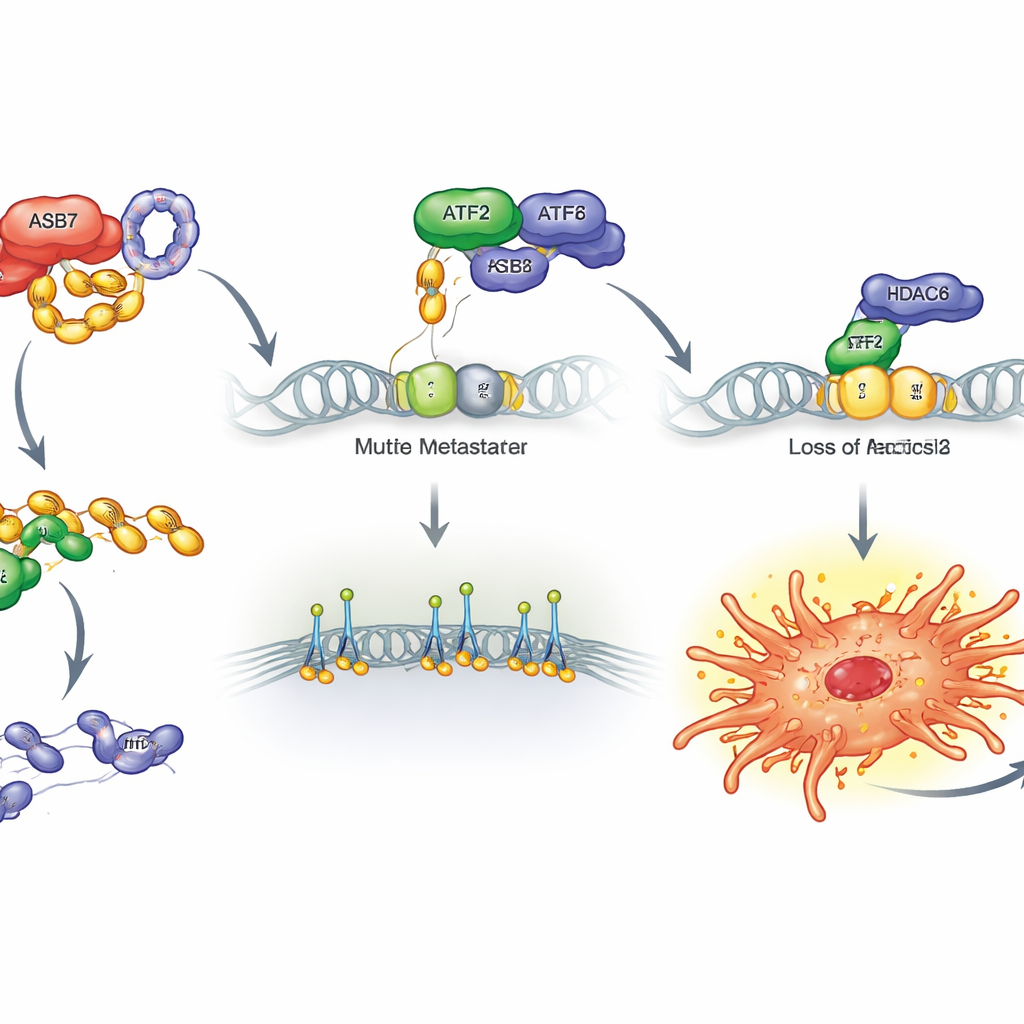
باتباع مسار أعمق، حدد العلماء بروتينًا آخر، ATF2، كفرملة رئيسية للنقائل. ATF2 عامل نسخ، أي بروتين يلتصق بالحمض النووي ويساعد في التحكم في أي الجينات تُفعّل. في عينات المرضى ومجموعات بيانات البروتين الكبيرة، كانت الأورام التي تحتوي على كميات كبيرة من ASB7 تتميز بكمية قليلة من ATF2، والمرضى ذوو مستويات ATF2 المنخفضة كان أداؤهم السريري أسوأ. رفع مستوى ATF2 في خلايا الساركومة العظمية قلّل النتوءات، وأبطأ الهجرة والغزو، وخفّض النقائل الرئوية في الفئران؛ وإزالة ATF2 فعلت العكس. أظهرت تجارب بيوكيميائية السبب: يتعاون ASB7 مع شريك، CUL5، لوضع وسم صغير من اليوبيكويتين في موقع محدد على ATF2، مما يعلّمه للدمار بواسطة آلية تفكيك البروتين داخل الخلية. مع تكسير ATF2 باستمرار، تختفي قدرته على كبح الجينات الخطرة.
فك قبضة رئيسية على المحيط
سأل الفريق بعد ذلك أي الجينات يضبطها ATF2 عادة. بدمج ملفات نشاط الجينات مع خرائط ربط الحمض النووي العامة، ركزوا على ITGB2، عضو من عائلة الإنتغرينات من البروتينات التي تربط الخلايا ماديًا بمحيطها وتساعدها على الدفع بنفسها للأمام. عادة يجلس ATF2 بالقرب من جين ITGB2 ومع بروتين آخر يدعى HDAC6 يبقيه هادئًا. عندما يدمر ASB7 ATF2، ينكسر هذا التحالف، ويلتزم HDAC6 أقل، ويتحرر ITGB2 ليُفعّل بقوة. أكدت التجارب هذا السلسلة: رفع ASB7 أو حذف ATF2 زاد ITGB2، بينما رفع ATF2 أو إزالة ASB7 خفّضه. وإجبار الخلايا على إنتاج وفرة من ITGB2 وحده كان كافيًا لزيادة النتوءات والهجرة والغزو واستعمار الرئتين في الفئران، بينما أدى حذف ITGB2 إلى تلاشي هذه السلوكيات.
ماذا يعني هذا للعلاج المستقبلي
بالمجمل، تصف هذه العمل مسارًا واضحًا تكتسب من خلاله خلايا الساركومة العظمية قدرة الانتشار. يعمل ASB7 كـ «قاتل مأجور» جزيئي يدمر ATF2، مضعفًا تحالفه مع HDAC6 عند جين ITGB2. هذا يطلق ITGB2 وجينات مرتبطة أخرى، مما يمنح خلايا الورم قبضة وحركية زائدة أثناء غزوها للأوعية الدموية وتأسيسها في الرئتين. وبما أن هذا المسار يبدو نشطًا بشكل خاص في ساركومات العظم، فإنه يسلط الضوء على عدة أفكار علاجية واعدة: حجب فعالية ASB7، تثبيت ATF2، كبح ITGB2، أو تعديل آليات صمت الحمض النووي المرتبطة قد يساعد جميعها في منع نقائل الساركومة العظمية، وتحويل هذا المرض الذي غالبًا ما يكون مميتًا إلى حالة أكثر قابلية للإدارة.
الاستشهاد: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
الكلمات المفتاحية: الساركومة العظمية, النقائل, ASB7, ATF2, الإنتغرينات