Clear Sky Science · he
ASB7 מקדם גרורות ריאתיות של אוסטאוסרקומה דרך פירוק מתווך‑יוביקוויטין של ATF2
למה גידולי עצם משתוללים חשובים
אוסטאוסרקומה היא סרטן עצם נדיר אך תוקפני שפוגע בעיקר בילדים, מתבגרים ומבוגרים מבוגרים. התכונה המסוכנת ביותר שלה היא הנטייה להתפשט לריאות, לעיתים ולהפוך מחלה מקומית ברת טיפול למצב מאיים על החיים. המחקר הזה שואל שאלה פשוטה אך מרכזית: אילו "מפסקים" מולקולריים עוזרים לתאי האוסטאוסרקומה להתנתק מהעצם, לנסוע בגוף ולהתמקם בריאות — והאם ניתן לכבות אותם בחזרה?
עוזר חבוי בהתפשטות הסרטן
החוקרים התרכזו בחלבון שנקרא ASB7, שכבר היה ידוע כסיוע בתהליך הפינוי של חלבונים אחרים. באמצעות כרייה של מאגרי נתוני סרטן ציבוריים רחבי היקף וניתוח דגימות גידול של מטופלים, הם מצאו שתאי אוסטאוסרקומה לעיתים נושאים העתקים נוספים של גן ASB7 ומייצרים כמויות לא רגילות של חלבון ASB7. מטופלים שלגידולם היה הרבה ASB7 נטו לתוצאות הישרדות גרועות יותר, דבר שמעיד שמולקולה זו עושה יותר מאשר משימות תחזוקה שגרתיות — היא נראית ככזו שמסייעת לגידולים להתנהג באגרסיביות רבה יותר.
מתאים חלק לשוטטים פולשים
כדי לבדוק מה ASB7 עושה בפועל בתאי סרטן, הקבוצה תיכננה תאי אוסטאוסרקומה להפיק יותר ASB7 או לשאת חוסר בו. כאשר רמות ASB7 הוגברו, התאים ייצרו רבות של בליטות דקות בדמויות אצבע ומניפה מבוססות אקטין, אותו שלד שמאפשר לתאים רגילים לזחול. תאים עם כמות גבוהה של ASB7 נעו מהר יותר דרך תאי מבחנה ופלשו דרך ג'ל המדמה רקמת גוף. כאשר הושתלו בעצמות הרגל של עכברים, הם היו בסבירות גבוהה בהרבה לייסד מושבות רבות בריאות. הסרת ASB7 פעלה בצורה ההפוכה: התאים איבדו את הבליטות, נדדו פחות וכפועל יוצא ייצרו גרורות ריאתיות מועטות בהרבה, ללא שינויים מהותיים בקצב החלוקה שלהם.
בלם מגן שמתפרק
בחקר מעמיק יותר זיהו המדענים חלבון נוסף, ATF2, כבלם מרכזי על תהליך הגרורות. ATF2 הוא גורם שעתוק — חלבון הקושר DNA ועוזר לשלוט אילו גנים דלוקים. בדגימות מטופלים ובמאגרי חלבונים נרחבים, גידולים עם הרבה ASB7 הציגו מעט ATF2, ומטופלים עם רמות נמוכות של ATF2 חוו תוצאות גרועות יותר. העלאת רמות ATF2 בתאי אוסטאוסרקומה צמצמה את הבליטות, האטה נדידה ופלישה והפחיתה גרורות ריאתיות בעכברים; השמטת ATF2 עשתה את ההיפך. ניסויים ביוכימיים חשפו את המנגנון: ASB7 משתף פעולה עם שותף שנקרא CUL5 כדי לתייג את ATF2 באתר ספציפי בקטעי יוביקוויטין קטנים, שמסמנות אותו לפירוק על ידי מערכת פירוק החלבונים של התא. עם פירוק מתמיד של ATF2, היכולת שלו לעכב גנים מסוכנים נעלמת.
שחרור אחיזה מרכזית בסביבה
הקבוצה אחר כך חקרה אילו גנים ATF2 בדרך כלל מדכא. על‑ידי שילוב פרופילים של פעילות גנים עם מפות קישור DNA ציבוריות, הם התמקדו ב‑ITGB2, חבר במשפחת האינטגרינים — חלבונים שמחברים פיזית את התאים לסביבתם ועוזרים להם לגרור את עצמם קדימה. בדרך הרגילה ATF2 נמצא קרוב לגֵן ITGB2 וביחד עם חלבון נוסף שנקרא HDAC6 הוא משמורר את ביטויו. כאשר ASB7 הורס את ATF2, השותפות הזו מופרעת, קשירת HDAC6 פוחתת ו‑ITGB2 משתחרר להידלק בעוצמה. ניסויים אישרו את שרשרת האירועים הזו: העלאת ASB7 או השמטת ATF2 הגדילו את ITGB2, בעוד שהעלאת ATF2 או הסרת ASB7 הורידו אותו. אילוץ תאים להפיק כמות עודפת של ITGB2 לבדו הספיק להגביר בליטות, נדידה, פלישה והתיישבות ריאתית בעכברים, בעוד שהסרת ITGB2 החלישה את ההתנהגויות האלה.
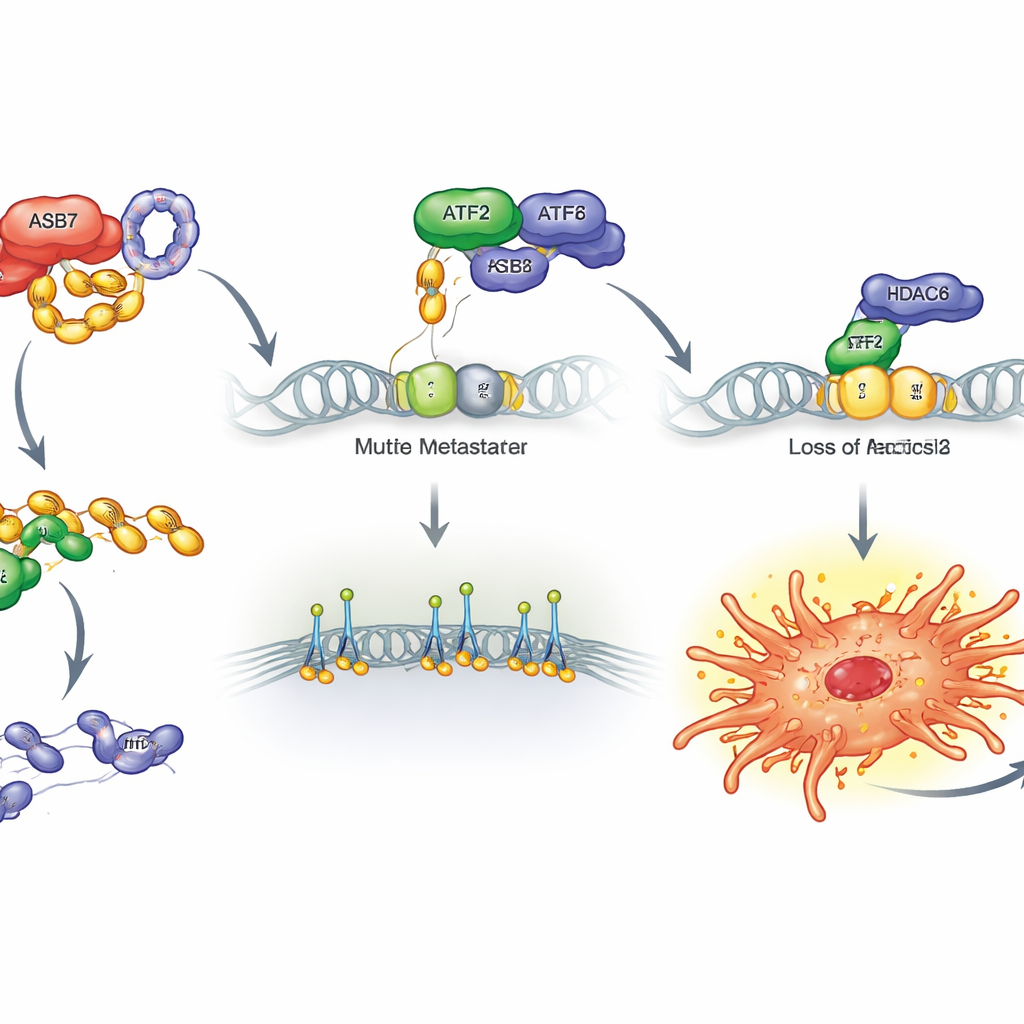
מה משמעות הדבר לטיפול עתידי
בצירוף כל הממצאים, העבודה מתווה מסלול ברור שבו תאי אוסטאוסרקומה רוכשים את היכולת להתפשט. ASB7 פועל כ"הורג ממוקד" מולקולרי שמשמיד את ATF2, ומחליש את השותפות שלו עם HDAC6 על גן ITGB2. הדבר משחרר את ITGB2 וגנים קשורים, ומעניק לתאי הגידול אחיזה וניידות מוגברות כשהם פולשים לכלי דם ומייסדים גרורות בריאות. מכיוון שהמסלול הזה נראה פעיל במיוחד בסרקומות עצם, הוא מדגיש כמה רעיונות טיפוליים מבטיחים: חסימת פעילות ASB7, ייצוב ATF2, דיכוי ITGB2 או כוונון של המכונה המשמשת להשתקת DNA עשויים כולם לעזור למנוע גרורות באוסטאוסרקומה ולהפוך מחלה שלעתים קרובות קטלנית לאחת שניתן לנהל טוב יותר.
ציטוט: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
מילות מפתח: אוסטאוסרקומה, גרורות, ASB7, ATF2, אינטגרינים