Clear Sky Science · fr
ASB7 favorise les métastases pulmonaires de l’ostéosarcome via la dégradation ubiquitine‑dépendante d’ATF2
Pourquoi les tumeurs osseuses incontrôlées comptent
L’ostéosarcome est un cancer osseux rare mais agressif qui touche principalement les enfants, les adolescents et les adultes plus âgés. Sa caractéristique la plus mortelle est sa propension à se propager aux poumons, transformant souvent une maladie locale traitable en une menace vitale. Cette étude pose une question simple mais cruciale : quels « interrupteurs » moléculaires permettent aux cellules d’ostéosarcome de se détacher de l’os, de voyager dans l’organisme et de coloniser les poumons — et peut‑on rééteindre ces interrupteurs ?
Un complice caché de la dissémination tumorale
Les chercheurs se sont concentrés sur une protéine appelée ASB7, connue auparavant pour aider les cellules à éliminer d’autres protéines. En exploitant de larges jeux de données publiques sur le cancer et en analysant des échantillons tumoraux de patients, ils ont constaté que les cellules d’ostéosarcome portent souvent des copies supplémentaires du gène ASB7 et produisent des quantités anormalement élevées de la protéine ASB7. Les patients dont les tumeurs étaient riches en ASB7 présentaient une survie plus faible, suggérant que cette molécule fait plus que le ménage habituel : elle semble favoriser un comportement tumoral plus agressif.
De cellules lisses à envahisseurs mobiles
Pour savoir ce que fait réellement ASB7 dans les cellules cancéreuses, l’équipe a modifié des cellules d’ostéosarcome pour qu’elles surexpriment ou manquent d’ASB7. Quand les niveaux d’ASB7 augmentaient, les cellules produisaient de nombreux prolongements fins en forme de doigts ou d’éventail constitués d’actine, le même échafaudage utilisé par les cellules normales pour se déplacer. Ces cellules à fort taux d’ASB7 se déplaçaient plus vite dans des chambres d’essai et traversaient un gel mimant les tissus. Implantées dans les os des souris, elles semaient beaucoup plus de colonies dans les poumons. La suppression d’ASB7 avait l’effet inverse : les cellules perdaient leurs prolongements, migraient mal et formaient beaucoup moins de métastases pulmonaires, sans changement majeur de leur rythme de division.
Un frein protecteur démantelé
En creusant plus loin, les scientifiques ont identifié une autre protéine, ATF2, comme un frein clé des métastases. ATF2 est un facteur de transcription, une protéine qui se lie à l’ADN et contribue à contrôler l’activation des gènes. Dans les échantillons de patients et les grandes bases de données protéiques, les tumeurs riches en ASB7 présentaient peu d’ATF2, et les patients ayant un faible ATF2 avaient un mauvais pronostic. Augmenter ATF2 dans des cellules d’ostéosarcome réduisait les prolongements, ralentissait la migration et l’invasion, et diminuait les métastases pulmonaires chez la souris ; supprimer ATF2 produisait l’effet inverse. Des expériences biochimiques ont expliqué pourquoi : ASB7 s’associe à un partenaire, CUL5, pour marquer ATF2 en un site spécifique par l’ajout de petites molécules d’ubiquitine, l’étiquetant ainsi pour destruction par les machines intracellulaires de dégradation des protéines. Avec ATF2 constamment détruit, sa capacité à freiner des gènes dangereux disparaît.
Relâcher une prise clé sur l’environnement
L’équipe a ensuite cherché quels gènes ATF2 réprimait normalement. En combinant des profils d’activité génique avec des cartes publiques de liaison à l’ADN, ils ont identifié ITGB2, un membre de la famille des intégrines qui relient physiquement les cellules à leur environnement et les aident à se propulser. ATF2 se situe normalement à proximité du gène ITGB2 et, avec une autre protéine appelée HDAC6, le maintien à l’état silencieux. Quand ASB7 détruit ATF2, ce partenariat est perturbé, HDAC6 se lie moins, et ITGB2 est libéré pour s’exprimer fortement. Les expériences ont confirmé cette chaîne causale : augmenter ASB7 ou supprimer ATF2 augmentait ITGB2, alors qu’augmenter ATF2 ou supprimer ASB7 le diminuait. Forcer la surexpression d’ITGB2 à lui seul suffisait à accroître les prolongements, la migration, l’invasion et la colonisation pulmonaire chez la souris, tandis que la suppression d’ITGB2 atténuait ces comportements.
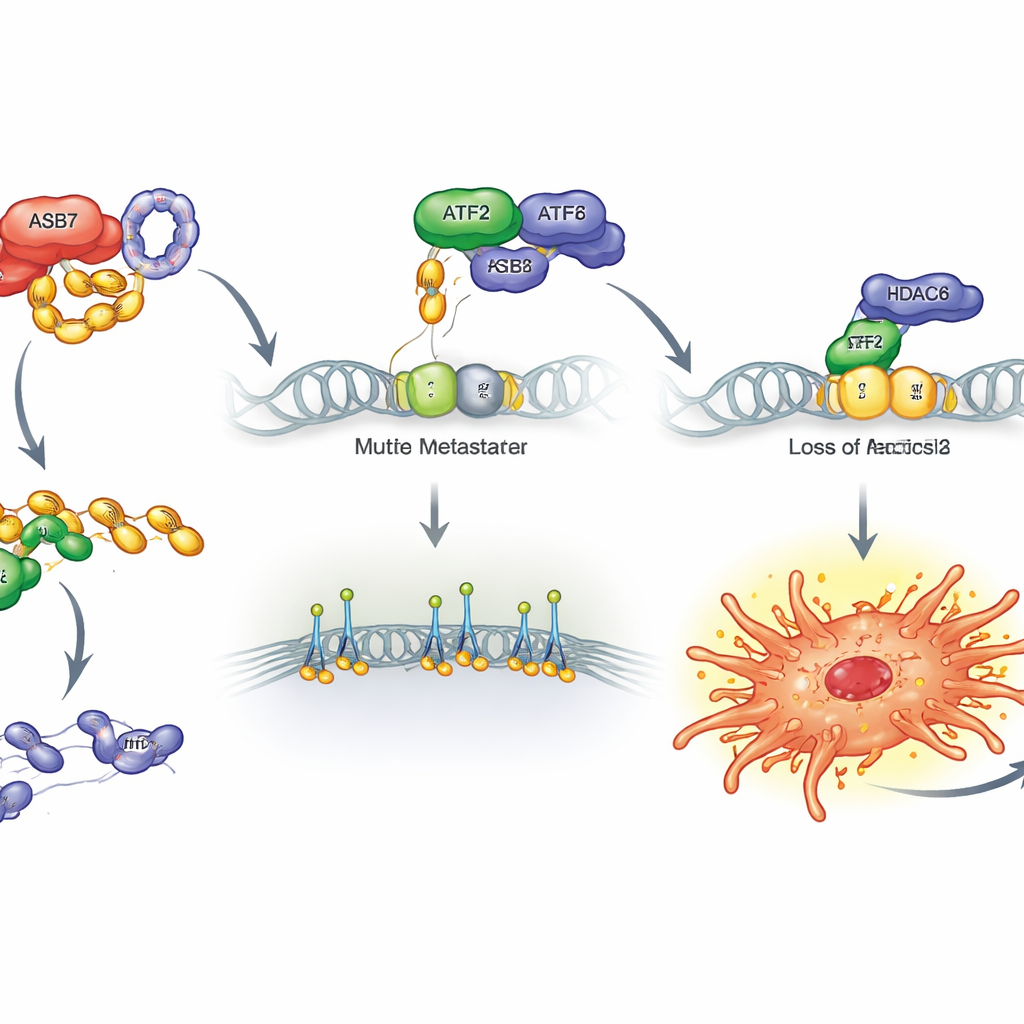
Ce que cela implique pour les traitements futurs
Pris ensemble, ces travaux décrivent une voie claire par laquelle les cellules d’ostéosarcome gagnent en capacité de dissémination. ASB7 agit comme un « tueur » moléculaire qui détruit ATF2, affaiblissant son partenariat avec HDAC6 au niveau du gène ITGB2. Cela libère ITGB2 et des gènes apparentés, donnant aux cellules tumorales une meilleure adhérence et mobilité pour envahir les vaisseaux sanguins et coloniser les poumons. Comme cette voie semble particulièrement active dans les sarcomes osseux, elle met en lumière plusieurs pistes thérapeutiques prometteuses : inhiber l’activité d’ASB7, stabiliser ATF2, réduire ITGB2, ou moduler la machinerie de silencement de l’ADN associée pourraient toutes aider à empêcher l’ostéosarcome de métastaser, transformant une maladie souvent mortelle en une pathologie bien plus gérable.
Citation: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
Mots-clés: ostéosarcome, métastase, ASB7, ATF2, intégrines