Clear Sky Science · de
ASB7 fördert Lungenmetastasen bei Osteosarkom durch ubiquitinvermittelte Degradation von ATF2
Warum entgleiste Knochentumoren wichtig sind
Osteosarkom ist ein seltener, aber aggressiver Knochenkrebs, der vor allem Kinder, Jugendliche und ältere Erwachsene trifft. Sein tödlichstes Merkmal ist die Neigung, in die Lunge zu streuen und aus einer lokal behandelbaren Erkrankung eine lebensbedrohliche zu machen. Diese Studie stellt eine einfache, aber entscheidende Frage: Welche molekularen „Schalter“ helfen Osteosarkomzellen, sich vom Knochen zu lösen, durch den Körper zu wandern und die Lunge zu besiedeln — und lassen sich diese Schalter wieder ausschalten?
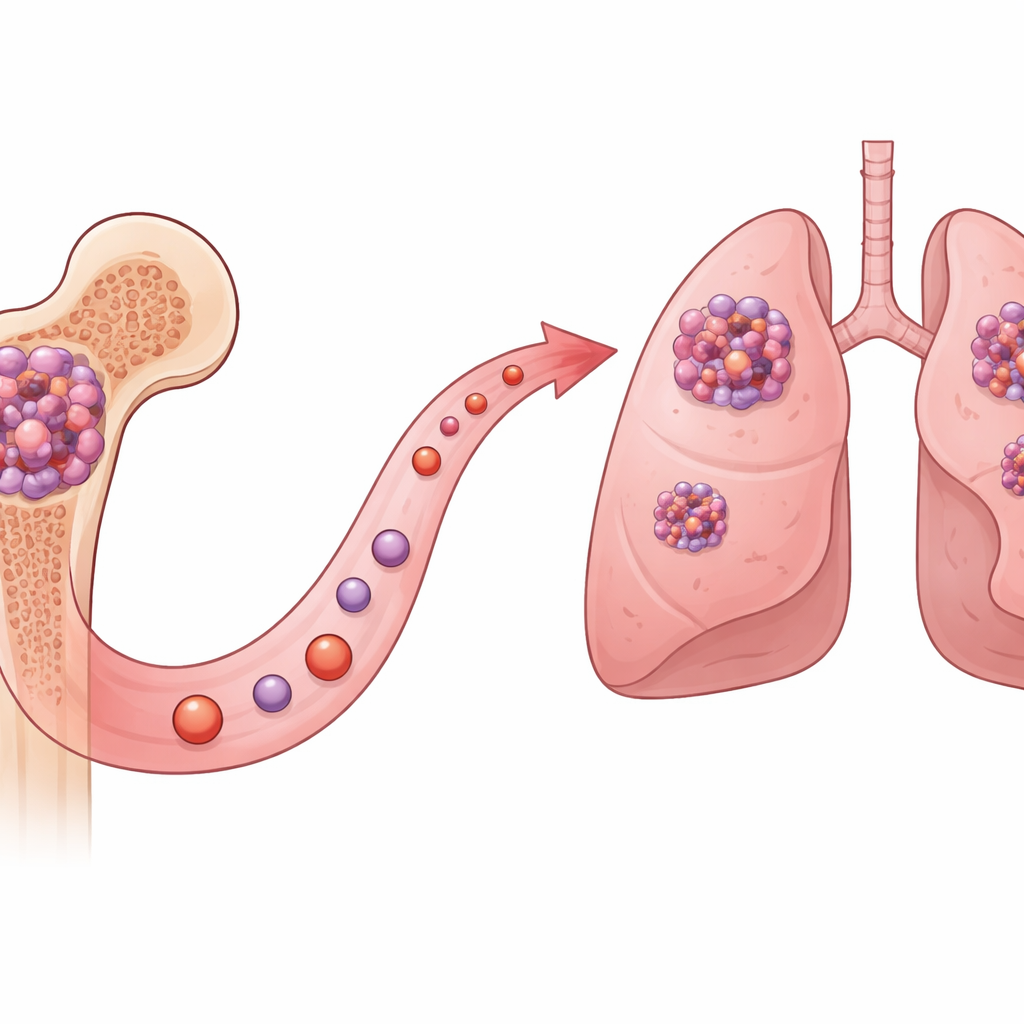
Ein verborgener Helfer der Tumorausbreitung
Die Forschenden konzentrierten sich auf ein Protein namens ASB7, das bislang vor allem dafür bekannt war, Zellen beim Abbau anderer Proteine zu helfen. Durch das Auswerten großer öffentlicher Krebsdatensätze und die Analyse von Patiententumoren fanden sie heraus, dass Osteosarkomzellen häufig zusätzliche Kopien des ASB7-Gens tragen und ungewöhnlich viel ASB7-Protein produzieren. Patienten mit ASB7-reichen Tumoren hatten tendenziell eine schlechtere Überlebensprognose, was darauf hindeutet, dass dieses Molekül mehr ist als nur Routine-Haushalt — es scheint Tumoren aggressiver machen zu können.
Von ruhigen Zellen zu umherwandernden Eindringlingen
Um zu verstehen, was ASB7 in Krebszellen tatsächlich bewirkt, veränderte das Team Osteosarkomzellen so, dass sie entweder zu viel oder gar kein ASB7 produzierten. Bei erhöhten ASB7-Werten bildeten die Zellen viele dünne, fingerartige und fächerförmige Vorsprünge aus Aktin, dem gleichen Gerüst, das normale Zellen zum Kriechen nutzen. Diese ASB7-hohen Zellen bewegten sich schneller durch Laborchambers und drangen durch Gel, das Gewebe imitiert. Nach Implantation in die Beinböden von Mäusen bildeten sie weitaus häufiger zahlreiche Herde in der Lunge. Die Entfernung von ASB7 hatte den gegenteiligen Effekt: Die Zellen verloren ihre Vorsprünge, wanderten schlecht und bildeten deutlich weniger Lungenmetastasen, ohne dass sich ihre Teilungsrate wesentlich änderte.
Eine schützende Bremse, die demontiert wird
Tiefer gehend identifizierten die Wissenschaftler ein weiteres Protein, ATF2, als wichtigen Bremsmechanismus gegen Metastasierung. ATF2 ist ein Transkriptionsfaktor — ein Protein, das an DNA bindet und hilft zu steuern, welche Gene aktiviert werden. In Patientenproben und großen Proteindatensätzen wiesen Tumoren mit viel ASB7 wenig ATF2 auf, und Patienten mit niedrigem ATF2 hatten schlechtere Verläufe. Eine Erhöhung von ATF2 in Osteosarkomzellen verringerte Vorsprünge, verlangsamte Migration und Invasion und reduzierte Lungenmetastasen bei Mäusen; das Entfernen von ATF2 bewirkte das Gegenteil. Biochemische Experimente erklärten den Grund: ASB7 bildet mit einem Partner, CUL5, ein Team, das ATF2 an einer bestimmten Stelle mit kleinen Ubiquitin-Molekülen markiert und damit für den Abbau durch die zelluläre Proteasom-Maschinerie kennzeichnet. Durch den ständigen Abbau von ATF2 geht seine Fähigkeit verloren, gefährliche Gene zu kontrollieren.
Ein zentrales Haltemanöver auf die Umgebung wird gelöst
Das Team fragte dann, welche Gene ATF2 normalerweise unterdrückt. Durch die Kombination von Genaktivitätsprofilen mit öffentlichen DNA-Bindungskarten fokussierten sie auf ITGB2, ein Mitglied der Integrin-Familie, die Zellen physisch mit ihrer Umgebung verbindet und ihnen hilft, sich vorwärts zu ziehen. ATF2 sitzt normalerweise in der Nähe des ITGB2-Gens und hält es zusammen mit einem weiteren Protein, HDAC6, still. Wenn ASB7 ATF2 zerstört, wird diese Partnerschaft gestört, HDAC6 bindet weniger und ITGB2 wird freigegeben, sich stark zu aktivieren. Experimente bestätigten diese Kette: Erhöhtes ASB7 oder das Entfernen von ATF2 steigerten ITGB2, während eine Erhöhung von ATF2 oder das Entfernen von ASB7 ITGB2 senkte. Das erzwungene Überproduzieren von ITGB2 allein reichte aus, um Vorsprünge, Migration, Invasion und Lungenbesiedlung in Mäusen zu verstärken, während das Entfernen von ITGB2 diese Eigenschaften abschwächte.
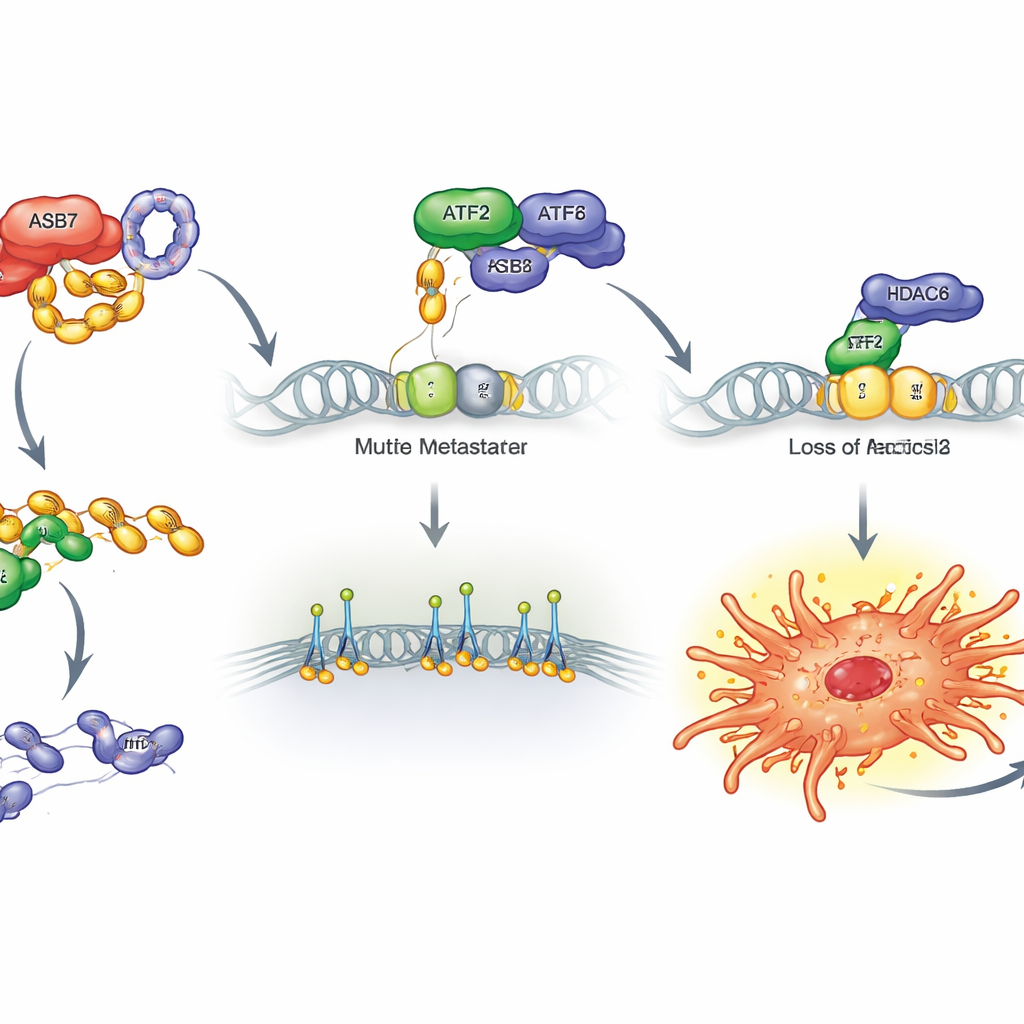
Was das für zukünftige Therapien bedeutet
In der Summe zeichnet die Arbeit einen klaren Weg nach, wie Osteosarkomzellen die Fähigkeit zur Ausbreitung erlangen. ASB7 fungiert als molekularer „Auftragskiller“, der ATF2 zerstört und damit dessen Zusammenarbeit mit HDAC6 am ITGB2-Gen schwächt. Dadurch werden ITGB2 und verwandte Gene freigesetzt, was Tumorzellen zusätzliche Haftung und Mobilität verleiht, während sie in Blutgefäße eindringen und die Lunge besiedeln. Da dieser Signalweg besonders in Knochensarkomen aktiv zu sein scheint, eröffnet er mehrere vielversprechende therapeutische Ansätze: das Blockieren der ASB7-Aktivität, das Stabilisieren von ATF2, das Dämpfen von ITGB2 oder das Einstellen der verbundenen DNA‑Stummschalt‑Maschinerie könnten alle dazu beitragen, die Metastasierung von Osteosarkomen zu verhindern und eine oft tödliche Krankheit deutlich besser beherrschbar zu machen.
Zitation: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
Schlüsselwörter: Osteosarkom, Metastasierung, ASB7, ATF2, Integrine