Clear Sky Science · pl
ASB7 sprzyja przerzutom osteosarcomy do płuc przez ubikwitynowo‑zależną degradację ATF2
Dlaczego wymykające się spod kontroli nowotwory kości mają znaczenie
Osteosarcoma to rzadki, ale agresywny nowotwór kości, który dotyka głównie dzieci, nastolatków oraz osoby starsze. Najgroźniejszą cechą tej choroby jest skłonność do przerzutów do płuc, co często zamienia możliwy do leczenia lokalny guz w zagrożenie dla życia. W tym badaniu postawiono proste, lecz kluczowe pytanie: jakie molekularne „przełączniki” pozwalają komórkom osteosarcomy oderwać się od kości, przemieszczać przez organizm i kolonizować płuca — i czy da się te przełączniki wyłączyć?
Ukryty pomocnik rozprzestrzeniania się raka
Naukowcy skupili się na białku ASB7, wcześniej znanym z roli w usuwaniu innych białek z komórki. Analizując duże publiczne zbiory danych onkologicznych i próbki guzów od pacjentów, stwierdzili, że komórki osteosarcomy często mają dodatkowe kopie genu ASB7 i wytwarzają nietypowo duże ilości białka ASB7. Pacjenci, których guzy obfitowały w ASB7, mieli gorsze przeżycie, co sugeruje, że ta cząsteczka pełni więcej niż zwykłą funkcję porządkową — wydaje się napędzać bardziej agresywne zachowanie nowotworu.
Ze gładkich komórek w wędrujące najeźdźców
Aby sprawdzić, co ASB7 robi w komórkach nowotworowych, zespół zmodyfikował komórki osteosarcomy tak, by albo nadmiernie wytwarzały ASB7, albo go pozbawione były. Przy zwiększonym poziomie ASB7 komórki tworzyły wiele cienkich, palcowatych i wachlarzowatych wypustek zbudowanych z aktyny — tej samej struktury podporowej, której normalne komórki używają do przemieszczania się. Komórki z wysokim ASB7 poruszały się szybciej w testach in vitro i penetrowały żel imitujący tkankę. Po wszczepieniu do kości u myszy znacznie częściej dawały liczne ogniska w płucach. Usunięcie ASB7 przynosiło przeciwny efekt: komórki traciły wypustki, słabiej migrowały i tworzyły znacznie mniej przerzutów do płuc, bez istotnych zmian w szybkości podziałów.
Ochronny hamulec, który zostaje zdemontowany
Dalsze badania wykazały, że drugim kluczowym białkiem jest ATF2 — czynnik transkrypcyjny, czyli białko wiążące DNA i regulujące, które geny są aktywne. W próbkach pacjentów i w dużych zbiorach białkowych guzy z wysokim poziomem ASB7 miały niski poziom ATF2, a pacjenci z małą ilością ATF2 mieli gorsze rokowania. Zwiększenie poziomu ATF2 w komórkach osteosarcomy zmniejszało liczbę wypustek, spowalniało migrację i inwazję oraz redukowało przerzuty do płuc u myszy; usunięcie ATF2 działało odwrotnie. Eksperymenty biochemiczne wyjaśniły mechanizm: ASB7 łączy się z partnerem CUL5, by znakować ATF2 w konkretnym miejscu małymi cząsteczkami ubikwityny, oznaczając je do zniszczenia przez komórkowe „niszczarki” białek. Przy ciągłej degradacji ATF2 jego zdolność do hamowania niebezpiecznych genów zanika.
Zerwanie kluczowego uchwytu względem otoczenia
Zespół zapytał następnie, które geny ATF2 normalnie tłumi. Łącząc profile aktywności genów z publicznymi mapami wiązania DNA, wytypowali ITGB2 — członka rodziny integryn, białek łączących komórkę z otoczeniem i pomagających jej się poruszać. ATF2 zwykle znajduje się w pobliżu genu ITGB2 i razem z innym białkiem, HDAC6, utrzymuje go w stanie ciszy. Kiedy ASB7 niszczy ATF2, to partnerstwo zostaje zaburzone, HDAC6 wiąże się słabiej, a ITGB2 ma wolną drogę do silnej ekspresji. Eksperymenty potwierdziły tę sekwencję: podniesienie ASB7 lub usunięcie ATF2 zwiększało ITGB2, natomiast zwiększenie ATF2 lub usunięcie ASB7 je obniżało. Wymuszenie nadprodukcji ITGB2 samo w sobie wystarczało, by zwiększyć liczbę wypustek, migrację, inwazję i kolonizację płuc u myszy, podczas gdy usunięcie ITGB2 osłabiało te zachowania.
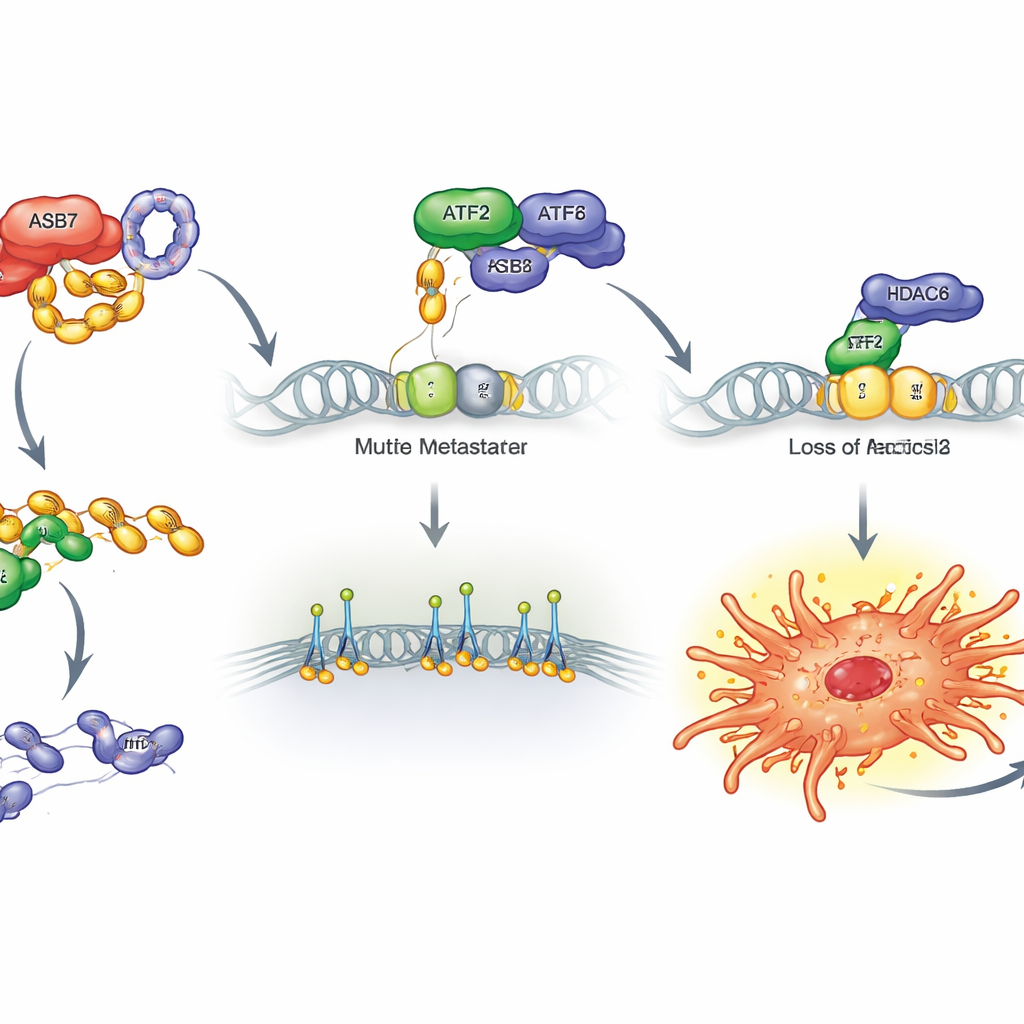
Co to oznacza dla przyszłego leczenia
Podsumowując, praca wyznacza klarowną drogę, dzięki której komórki osteosarcomy zyskują zdolność do rozprzestrzeniania się. ASB7 działa jak molekularny „płatny zabójca”, który niszczy ATF2, osłabiając jego współpracę z HDAC6 przy genie ITGB2. To uwalnia ITGB2 i powiązane geny, dając komórkom nowotworowym dodatkowy uchwyt i mobilność w trakcie inwazji naczyń krwionośnych i zasiewu w płucach. Ponieważ ten szlak wydaje się szczególnie aktywny w nowotworach kości, wskazuje na kilka obiecujących strategii terapeutycznych: blokowanie aktywności ASB7, stabilizowanie ATF2, tłumienie ITGB2 lub modulowanie powiązanych mechanizmów wyciszania DNA może pomóc powstrzymać przerzuty osteosarcomy i przekształcić często śmiertelną chorobę w stan znacznie bardziej możliwy do opanowania.
Cytowanie: Zou, Y., Zhong, J., Huo, L. et al. ASB7 promotes osteosarcoma lung metastasis through ubiquitin-mediated degradation of ATF2. Cell Discov 12, 31 (2026). https://doi.org/10.1038/s41421-026-00890-9
Słowa kluczowe: osteosarcoma, metastasis, ASB7, ATF2, integrins