Clear Sky Science · zh
BH3 模拟物与 NK 细胞介导免疫治疗在 T-ALL 中的治疗潜力
帮助身体对抗顽固血癌的新途径
T 细胞急性淋巴细胞白血病(T‑ALL)是一种侵袭性血液恶性肿瘤,主要影响儿童和年轻成人,常以强烈的化疗为主。尽管这些治疗能治愈许多患者,但也会带来严重副作用,并非对所有人有效,尤其是在复发后。本研究探讨了两种更新、更有针对性的策略——推动癌细胞自我毁灭的“智能”药物以及追踪肿瘤的免疫细胞——以评估它们是否能为 T‑ALL 患者提供更安全、更有效的选择。
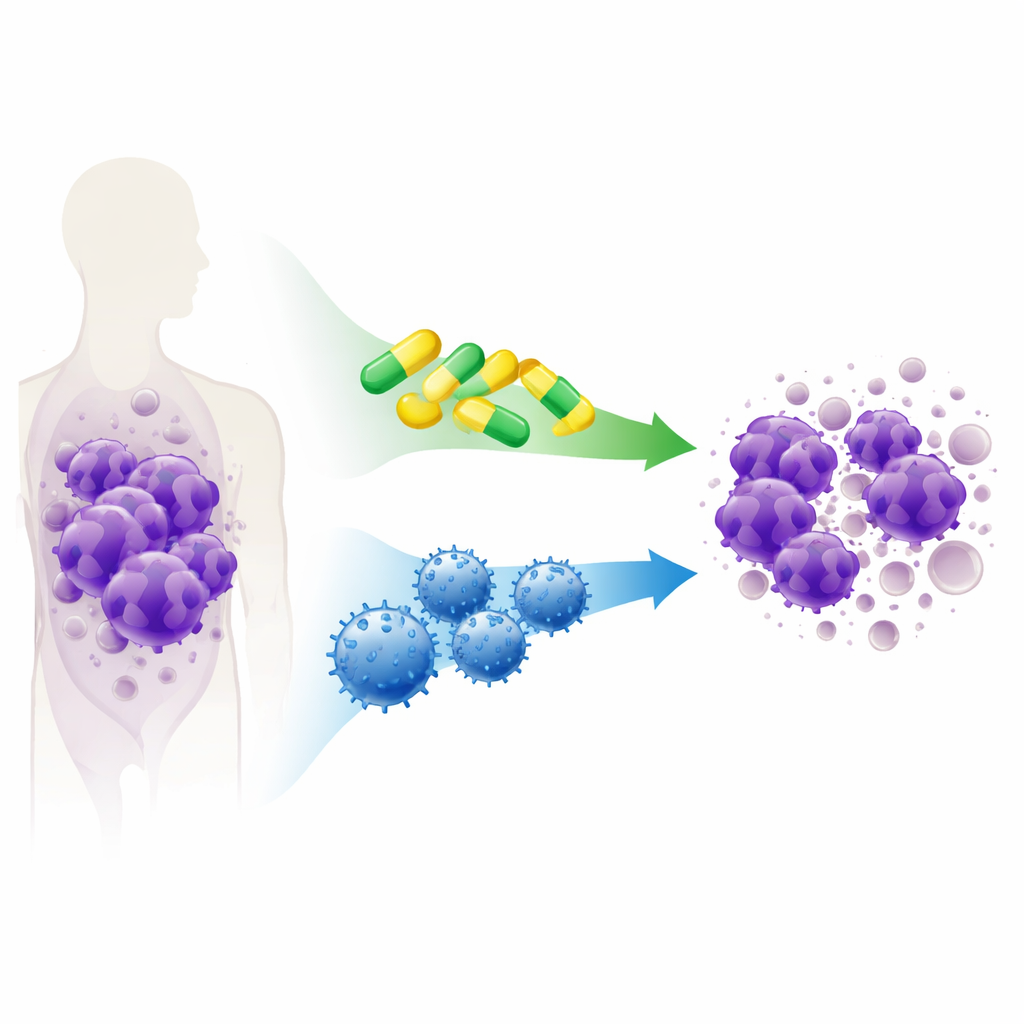
理解癌细胞的生存伎俩
癌细胞常通过挟持细胞内的“自杀”机制来规避死亡,这是一种通常用于清除受损或危险细胞的安全系统。在 T‑ALL 中,这种逃避依赖于一组像保镖一样的蛋白质,阻止细胞启动自我毁灭。研究人员测试了几种实验性和已获批的药物,称为 BH3‑模拟物,旨在解除这些“保镖”的保护并将细胞推向凋亡。他们在实验室的 T‑ALL 细胞系和来自真实患者并在小鼠中生长的白血病样本中,检查了分别针对不同“保镖”蛋白(BCL‑2、BCL‑XL 和 MCL‑1)的药物,单用或组合使用。
哪种“智能”药物效果最好?
研究团队发现,并非所有 T‑ALL 都依赖相同的生存蛋白,这一点对药物反应至关重要。一种高风险亚型,称为早期 T 细胞前体(ETP)ALL,对阻断 BCL‑2 特别敏感,这与早先表明这些细胞严重依赖该蛋白的线索相吻合。相反,大多数典型 T‑ALL 对单独阻断 BCL‑2 或 MCL‑1 抵抗,但许多样本对阻断 BCL‑XL 十分敏感。一种同时作用于 BCL‑2 和 BCL‑XL 的双靶点药物 AZD4320 在许多情况下显示出强效,尤其当白血病细胞的蛋白表达谱显示它们依赖这些靶点时。研究人员还使用称为 BH3‑描记(BH3‑profiling)的功能性检测来测量细胞距离触发自我毁灭的接近程度,并证明该测定能预测哪种药物或药物组合最可能奏效。
结合死亡信号以克服耐药
当科学家更仔细地观察白血病细胞随时间的反应时,他们看到阻断一种生存蛋白常常导致细胞转而依赖另一种,有点像更换保镖。例如,当单独使用双靶点 BCL‑2/BCL‑XL 药物时,细胞经常转向依赖 MCL‑1,从而削弱药物效果。通过将 AZD4320 与 MCL‑1 抑制剂配对,研究人员切断了这一逃逸通路。在细胞系和来源于患者的样本中,这种组合在本来耐药的情况下以相对低剂量诱导了强烈且常常具有协同效应的白血病细胞杀伤,提示精心设计的组合可能比将单一药物剂量推高更强大且更安全。
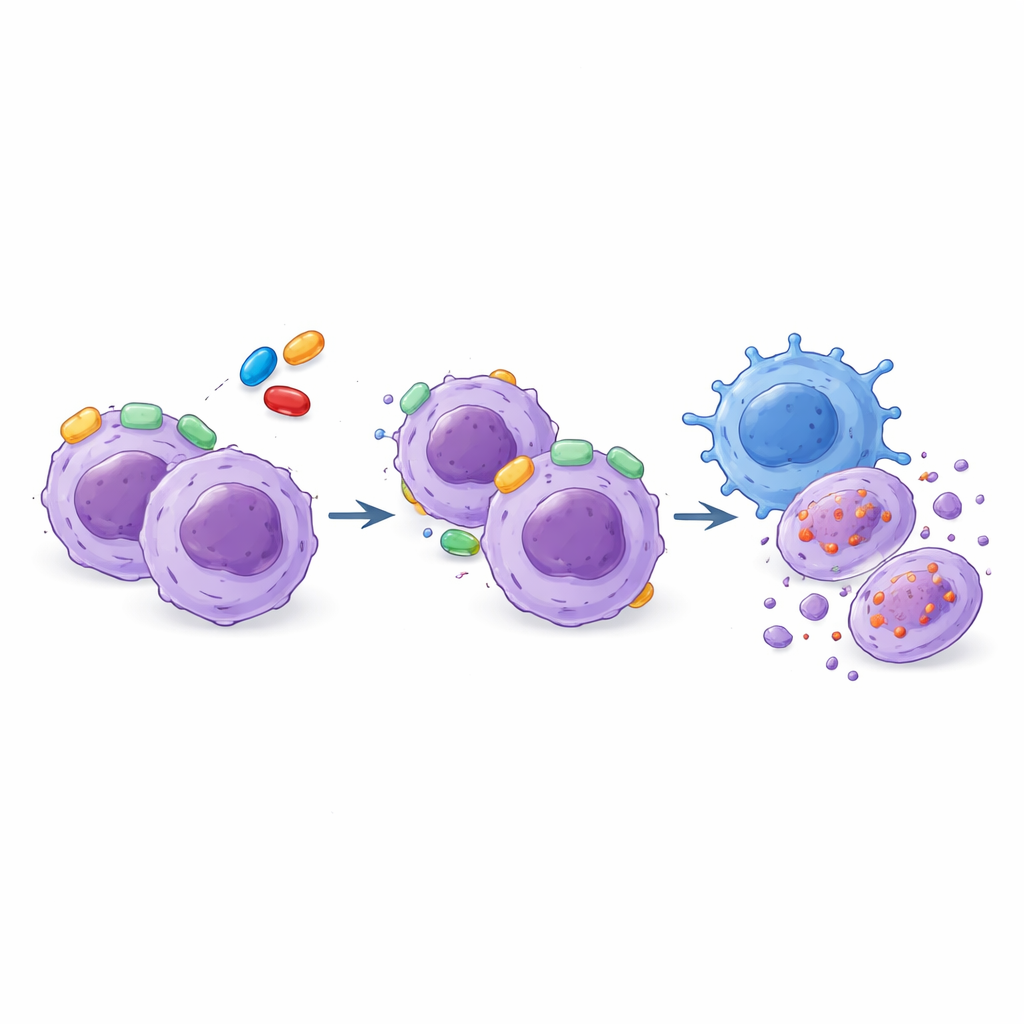
用靶向药物增强免疫攻击
该研究还探索了一种互补策略:利用自然杀伤(NK)细胞,这是一类能够在无需事先识别训练的情况下识别并摧毁癌细胞的免疫细胞。T‑ALL 样本对 NK 细胞的敏感性差异很大,但这种模式并不简单地与它们对 BH3‑模拟物的反应相一致,这意味着免疫攻击提供了独立的治疗途径。研究人员发现,让白血病细胞暴露于 NK 细胞会改变其内部的死亡调控布线,常常增加对 BCL‑XL 的依赖。重要的是,NK 细胞本身在很大程度上不受 BCL‑2/BCL‑XL 药物 AZD4320 的影响。当 AZD4320 与 NK 细胞联合使用时,在细胞系和来源于患者的样本中,白血病细胞的杀伤效果始终优于任何单一方法,显示出至少为加成的益处。
这对未来患者意味着什么
总体而言,这项工作表明,通过精确靶向其生存蛋白——尤其是 BCL‑XL——可以将许多 T‑ALL 细胞推向自我毁灭,并且组合不同的 BH3‑模拟物能在本来顽固的样本中克服耐药。结果还表明,将这些“智能”药物与基于 NK 细胞的免疫疗法配对,可能在不损害实施治疗所需的免疫细胞的情况下进一步削弱白血病并提高杀伤效果。尽管这些结果来自实验室和动物模型而非临床试验,但它们为在高风险或复发的 T‑ALL 患者中测试联合 BH3‑模拟物与 NK 细胞疗法提供了坚实的科学基础,长期希望能带来更有效且毒性更低的治疗选择。
引用: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
关键词: T 细胞急性淋巴细胞白血病, BH3 模拟物治疗, BCL-XL 抑制, 自然杀伤细胞免疫治疗, 以凋亡为靶的治疗