Clear Sky Science · pl
Potencjał terapeutyczny mimetyków BH3 i immunoterapii z udziałem komórek NK w T-ALL
Nowe sposoby wspomagania organizmu w walce z trudnym rakiem krwi
Ostra białaczka limfoblastyczna komórek T (T‑ALL) to agresywny nowotwór krwi, który dotyka głównie dzieci i młodych dorosłych i jest często leczony intensywną chemioterapią. Choć te terapie mogą wyleczyć wielu pacjentów, wiążą się też z poważnymi działaniami niepożądanymi i nie działają u wszystkich, zwłaszcza po nawrocie choroby. Badanie to analizuje dwie nowsze, bardziej ukierunkowane strategie — „inteligentne” leki, które prowokują komórki nowotworowe do samozniszczenia, oraz komórki układu odpornościowego polujące na guzy — aby ocenić, czy mogą one oferować bezpieczniejsze i skuteczniejsze opcje dla osób z T‑ALL.
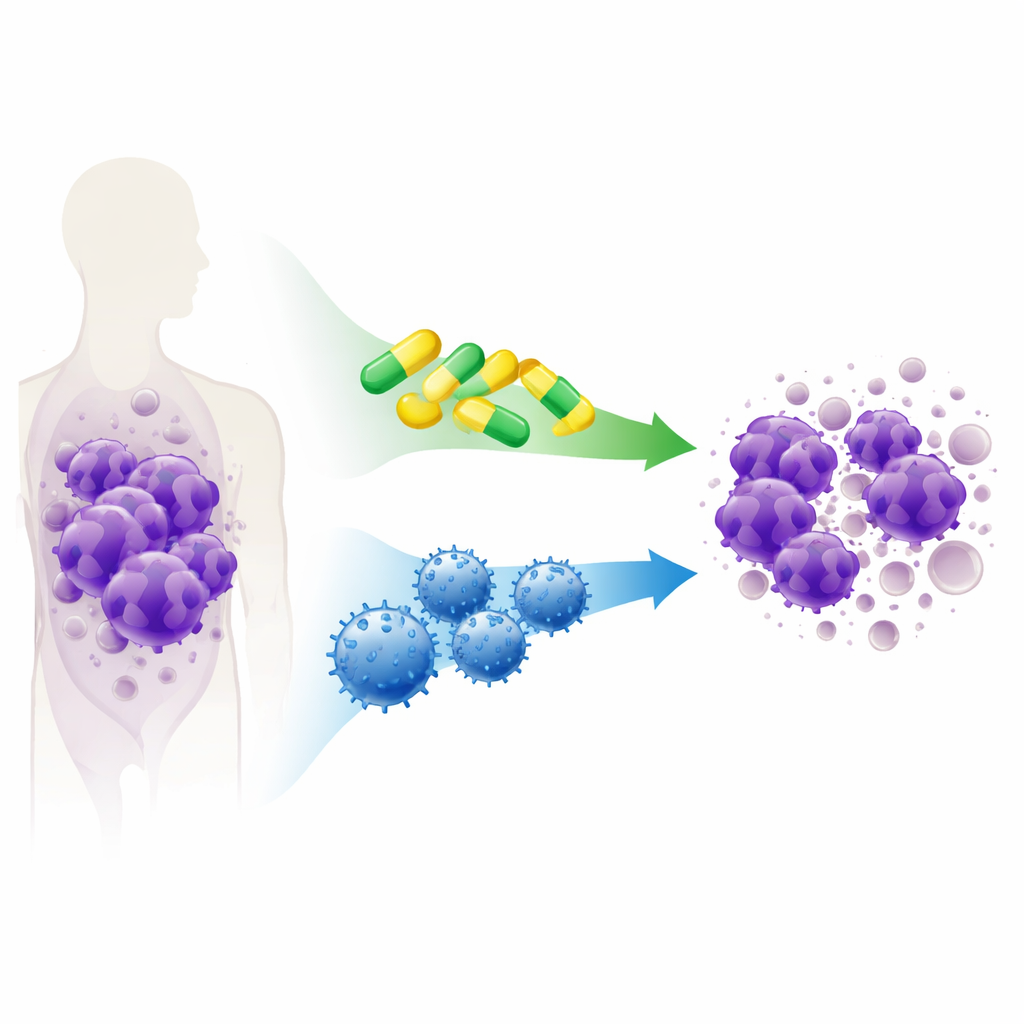
Jak rak omija mechanizmy śmierci komórkowej
Komórki nowotworowe często unikają śmierci przez przejęcie kontroli nad wbudowanym mechanizmem „samobójstwa” komórki — systemem bezpieczeństwa, który zwykle usuwa uszkodzone lub niebezpieczne komórki. W T‑ALL ucieczka ta opiera się na grupie białek pełniących rolę ochroniarzy, które zapobiegają uruchomieniu autodestrukcji. Badacze testowali kilka eksperymentalnych i zatwierdzonych leków nazywanych mimetykami BH3, zaprojektowanych tak, by unieszkodliwiać tych ochroniarzy i przywracać równowagę w kierunku śmierci komórki. Na liniach komórkowych T‑ALL i w próbkach białaczki pochodzących od pacjentów hodowanych u myszy badali leki blokujące różne białka‑ochroniarzy (BCL‑2, BCL‑XL i MCL‑1), stosowane osobno i w kombinacjach.
Które „inteligentne” leki działają najlepiej?
Zespół stwierdził, że nie wszystkie raki T‑ALL polegają na tym samym białku przetrwania, co miało istotne przełożenie na odpowiedź na lek. Podtyp wysokiego ryzyka zwany wczesnym prekursorem limfocytów T (ETP‑ALL) był szczególnie wrażliwy na blokowanie BCL‑2, co potwierdza wcześniejsze wskazówki, że komórki te silnie zależą od tego białka. Natomiast większość typowych próbek T‑ALL była oporna na samodzielne blokowanie BCL‑2 oraz na inhibitor MCL‑1, ale wiele z nich było wyraźnie wrażliwych na blokowanie BCL‑XL. Lek o podwójnym działaniu na BCL‑2 i BCL‑XL, AZD4320, wykazał silną aktywność w wielu przypadkach, szczególnie gdy profil białkowy komórek białaczkowych sugerował zależność od tych celów. Badacze zastosowali funkcjonalny test zwany BH3‑profiling, który mierzy, jak blisko komórki są uruchomienia autodestrukcji, i pokazali, że to badanie może przewidywać, który lek lub ich kombinacja ma największe szanse działać.
Łączenie sygnałów śmierci, by przełamać oporność
Gdy naukowcy przyjrzeli się dokładniej, jak komórki białaczki reagują w czasie, zauważyli, że blokowanie jednego białka przetrwania często powoduje przestawienie zależności komórek na inne, trochę jak zmiana ochroniarzy. Na przykład przy stosowaniu samego leku podwójnego na BCL‑2/BCL‑XL komórki często przełączały się na zależność od MCL‑1, co mogło osłabić działanie leku. Poprzez skojarzenie AZD4320 z inhibitorem MCL‑1 badacze zablokowali tę drogę ucieczki. Zarówno w liniach komórkowych, jak i w próbkach pochodzących od pacjentów, które wcześniej były oporne, kombinacja wywołała silne i często synergistyczne zabijanie komórek białaczkowych przy relatywnie niskich dawkach, sugerując, że starannie zaprojektowane połączenia mogą być skuteczniejsze i być może bezpieczniejsze niż zwiększanie dawek pojedynczych leków.
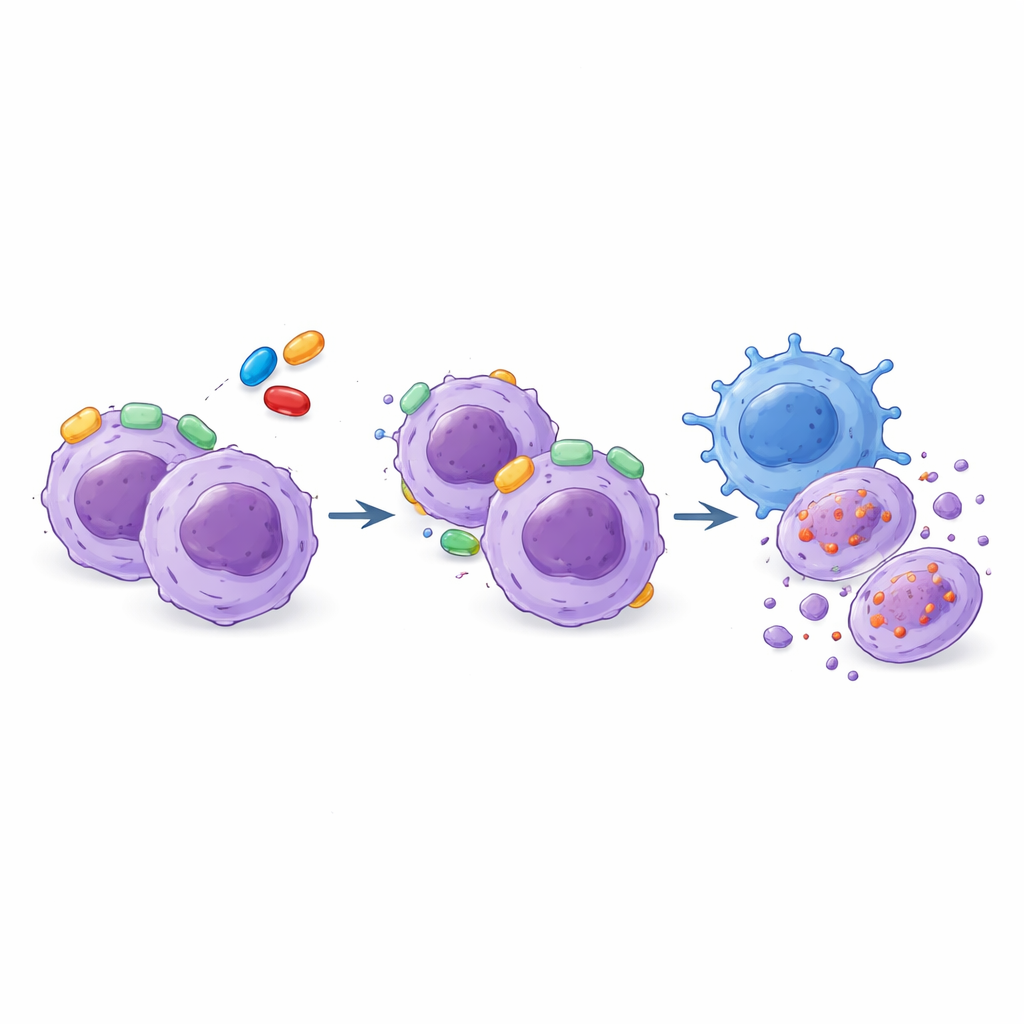
Wzmacnianie ataku odpornościowego za pomocą leków ukierunkowanych
Badanie zbadało także strategię uzupełniającą: wykorzystanie komórek natural killer (NK), rodzaju komórek układu odpornościowego, które potrafią rozpoznawać i niszczyć komórki nowotworowe bez wcześniejszego przeszkolenia. Próbki T‑ALL wykazywały szerokie spektrum wrażliwości na komórki NK, ale ten wzorzec nie był po prostu odbiciem ich reakcji na mimetyki BH3, co oznacza, że atak immunologiczny stanowi niezależną linię terapii. Badacze stwierdzili, że ekspozycja komórek białaczkowych na komórki NK zmieniała ich wewnętrzne „okablowanie” kontroli śmierci, często zwiększając zależność od BCL‑XL. Co ważne, same komórki NK były w dużej mierze niepodatne na lek AZD4320 blokujący BCL‑2/BCL‑XL. W połączeniu AZD4320 i komórek NK zabijanie komórek białaczkowych było konsekwentnie większe niż przy zastosowaniu którejkolwiek z metod osobno, zarówno w liniach komórkowych, jak i w próbkach pacjentów, wskazując na przynajmniej efekt addytywny.
Co to może znaczyć dla przyszłych pacjentów
Podsumowując, praca pokazuje, że wiele komórek T‑ALL można zmusić do autodestrukcji przez precyzyjne ukierunkowanie ich białek przetrwania, szczególnie BCL‑XL, oraz że łączenie różnych mimetyków BH3 może przełamać oporność w uporczywych próbkach. Wyniki sugerują także, że skojarzenie tych „inteligentnych” leków z immunoterapią opartą na komórkach NK może dodatkowo osłabić białaczkę i poprawić efektywność zabijania bez uszkadzania komórek odpornościowych niezbędnych do terapii. Choć wyniki pochodzą z badań laboratoryjnych i modeli zwierzęcych, a nie z badań klinicznych, dostarczają silnych podstaw naukowych do testowania skojarzonych terapii mimetykami BH3 i komórkami NK u pacjentów z wysokim ryzykiem lub nawrotem T‑ALL, z długoterminową nadzieją na skuteczniejsze i mniej toksyczne opcje leczenia.
Cytowanie: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
Słowa kluczowe: ostra limfoblastyczna białaczka limfocytów T, terapia mimetykami BH3, hamowanie BCL-XL, immunoterapia komórek natural killer, leczenie ukierunkowane na apoptozę