Clear Sky Science · ar
الإمكانات العلاجية لمحاكيات BH3 والمناعة المعتمدة على الخلايا القاتلة الطبيعية في اللوكيميا اللمفاوية الحادة من خلايا T
طرق جديدة لمساعدة الجسم على محاربة سرطان دم عنيد
اللوكيميا اللمفاوية الحادة من خلايا T (T‑ALL) هي سرطان دم عدواني يؤثر بشكل أساسي على الأطفال والشباب وغالباً ما يُعالج بكيمياء مكثفة. وبينما تستطيع هذه العلاجات شفاء العديد من المرضى، فإنها تسبب آثاراً جانبية خطيرة ولا تكون فعالة للجميع، لا سيما بعد الانتكاس. تستعرض هذه الدراسة استراتيجيتيْن أحدث وأكثر استهدافاً — أدوية ذكية تدفع الخلايا السرطانية إلى الانتحار المبرمج وخلايا مناعية تصطاد الأورام — لمعرفة ما إذا كان بالإمكان أن توفر خيارات أكثر أماناً وفعالية للأشخاص المصابين بـ T‑ALL.
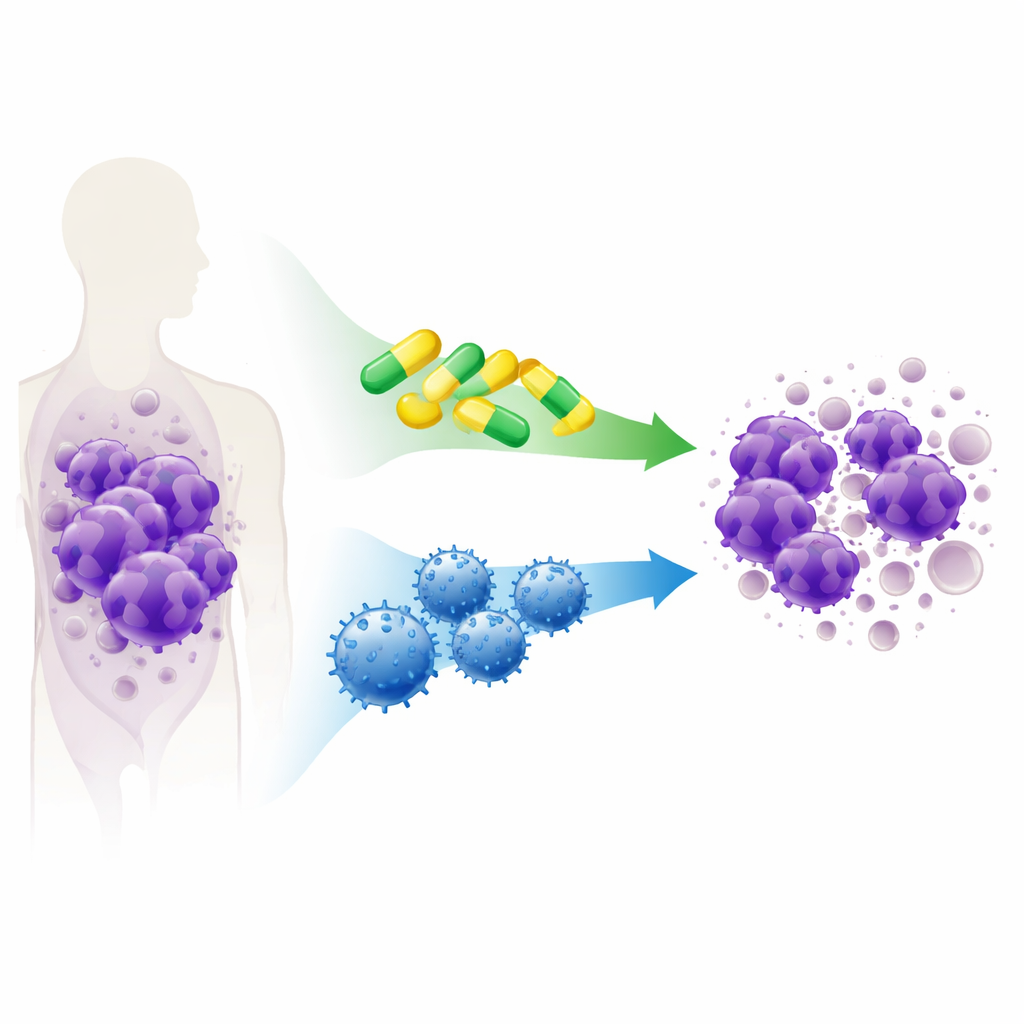
فهم حيل السرطان للبقاء
غالباً ما تتجنب الخلايا السرطانية الموت من خلال اختطاف آلية «الانتحار» المدمجة في الخلية، وهي منظومة أمان تزيل عادة الخلايا التالفة أو الخطرة. في T‑ALL، يعتمد هذا الهروب على مجموعة من البروتينات التي تعمل مثل الحراس الشخصيين، ممانعة الخلية عن تفعيل آلية الانتحار. اختبر الباحثون عدة أدوية تجريبية ومعتمدة تُسمى محاكيات BH3، مصممة لتعطيل هؤلاء الحراس وإعادة التوازن نحو موت الخلية. باستخدام خطوط خلايا T‑ALL المختبرية وعينات اللوكيميا المزروعة في الفئران من مرضى حقيقيين، فحصوا أدوية تحجب بروتينات الحراسة المختلفة (BCL‑2 وBCL‑XL وMCL‑1) منفردة وبالاشتراك.
أي الأدوية الذكية هي الأفضل؟
وجد الفريق أن ليست كل سرطانات T‑ALL تعتمد على نفس بروتين البقاء، وكان لذلك أثر كبير على استجابة الدواء. كان نوع عالي المخاطر يُسمى اللوكيميا مبكرة المستخلصات اللمفاوية T (ETP‑ALL) عرضة بشكل خاص لحجب BCL‑2، متوافقاً مع دلائل سابقة أن هذه الخلايا تعتمد بشدة على هذا البروتين. في المقابل، كانت معظم عينات T‑ALL النمطية مقاومة لـ BCL‑2 ولمثبط MCL‑1 بمفرده، لكن العديد منها كان حساساً جداً لحجب BCL‑XL. أظهر دواء ذو فعل مزدوج يستهدف كلا من BCL‑2 وBCL‑XL، AZD4320، نشاطاً قوياً في العديد من الحالات، خصوصاً عندما أشارت أنماط البروتين في خلايا اللوكيميا إلى اعتماد على هذين الهدفين. استخدم الباحثون اختباراً وظيفياً يُدعى BH3‑profiling، الذي يقيس مدى اقتراب الخلايا من تفعيل الانتحار المبرمج، وأظهر أن هذا الاختبار يمكن أن يتنبأ بالأدوية أو تركيبات الأدوية الأكثر احتمالاً للنجاح.
دمج إشارات الموت لتجاوز المقاومة
عندما نظر العلماء عن كثب في كيفية استجابة خلايا اللوكيميا مع مرور الوقت، رأوا أن حجب بروتين بقاء واحد غالباً ما يدفع الخلايا إلى تغيير اعتمادها إلى بروتين آخر، أشبه بتبديل الحراس الشخصيين. على سبيل المثال، عندما استُخدم الدواء المزدوج BCL‑2/BCL‑XL بمفرده، تحولت الخلايا في كثير من الأحيان إلى الاعتماد على MCL‑1، وهو ما قد يضعف تأثير الدواء. من خلال إقران AZD4320 بمثبط MCL‑1، قطع الباحثون هذا طريق الهروب. في كل من خطوط الخلايا والعينات المشتقة من مرضى كانت مقاومة بخلاف ذلك، تسبب هذا الجمع في قتل قوي وغالباً متآزر لخلايا اللوكيميا بجرعات منخفضة نسبياً، مما يشير إلى أن التركيبات المصممة بعناية قد تكون أقوى وربما أكثر أماناً من دفع دواء واحد إلى مستويات أعلى.
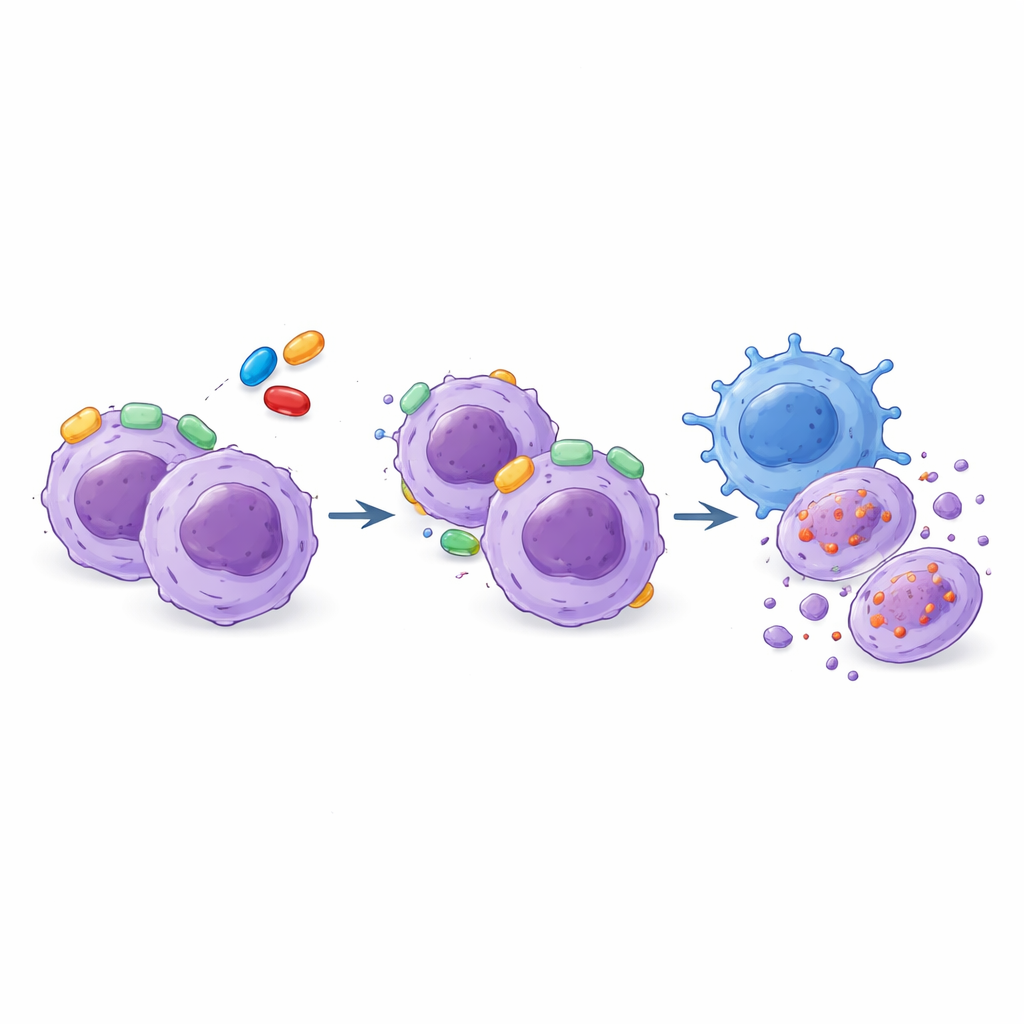
تعزيز الهجوم المناعي بالأدوية المستهدفة
استكشفت الدراسة أيضاً استراتيجية مكملة: استخدام الخلايا القاتلة الطبيعية (NK)، وهي نوع من الخلايا المناعية القادرة على التعرف على الخلايا السرطانية وتدميرها دون تدريب مسبق. أظهرت عينات T‑ALL مدى واسعاً من الحساسية لخلايا NK، لكن هذا النمط لم يعكس ببساطة استجابتها لمحاكيات BH3، بمعنى أن الهجوم المناعي يقدم خط علاج مستقل. وجد الباحثون أن تعرّض خلايا اللوكيميا لخلايا NK يغير أسلاك التحكم بالموت داخلها، غالباً ما يزيد اعتمادها على BCL‑XL. ومن المهم أن خلايا NK نفسها كانت إلى حد كبير غير متأثرة بالدواء AZD4320 الذي يستهدف BCL‑2/BCL‑XL. عندما جُمِع AZD4320 مع خلايا NK، كان قتل خلايا اللوكيميا أكبر باستمرار من أي من النهجين وحده في كل من خطوط الخلايا والعينات المشتقة من المرضى، مشيراً إلى فوائد مضافة على الأقل.
ماذا قد يعني هذا لمرضى المستقبل
بالمجمل، تُظهر هذه الأعمال أن العديد من خلايا T‑ALL يمكن إجبارها على الانتحار المبرمج من خلال استهداف بروتينات بقائها بدقة، خاصة BCL‑XL، وأن دمج أدوية محاكيات BH3 المختلفة يمكن أن يتغلب على المقاومة في عينات عنيدة بخلاف ذلك. وتشير النتائج أيضاً إلى أن إقران هذه الأدوية الذكية بمناعة معتمدة على خلايا NK قد يضعف اللوكيميا أكثر ويحسّن القتل دون الإضرار بالخلايا المناعية اللازمة للعلاج. ورغم أن هذه النتائج مستمدة من نماذج مخبرية وحيوانية وليست من تجارب سريرية بعد، فإنها توفر أساساً علمياً قوياً لاختبار علاجات مجمعة تعتمد على محاكيات BH3 وخلايا NK في مرضى T‑ALL المعرضين لخطر عالٍ أو المنتكسين، مع أمل طويل الأمد في خيارات علاجية أكثر فعالية وأقل سمية.
الاستشهاد: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
الكلمات المفتاحية: اللوكيميا اللمفاوية الحادة من خلايا T, علاج بمحاكيات BH3, مثبط BCL-XL, مناعة الخلايا القاتلة الطبيعية, علاج يستهدف الموت المبرمج