Clear Sky Science · tr
T-ALL’de BH3-mimetiklerin ve NK hücre aracılı immünoterapinin terapötik potansiyeli
Zorlu Bir Kanserle Mücadelede Vücudun Yardımını Artırmanın Yeni Yolları
T hücre akut lenfoblastik lösemi (T‑ALL), çoğunlukla çocukları ve genç yetişkinleri etkileyen agresif bir kanserdir ve sıklıkla yoğun kemoterapi ile tedavi edilir. Bu tedaviler birçok hastayı iyileştirebilse de ciddi yan etkilere yol açar ve özellikle nüks durumunda herkeste etkili olmaz. Bu çalışma, kansere kendi kendini yok etme sinyalini tetikleyen hedefe yönelik ilaçlar ile tümörleri avlayan bağışıklık hücrelerini içeren iki daha yeni, daha hedeflenmiş stratejinin T‑ALL hastaları için daha güvenli ve etkili seçenekler sunup sunamayacağını araştırıyor.
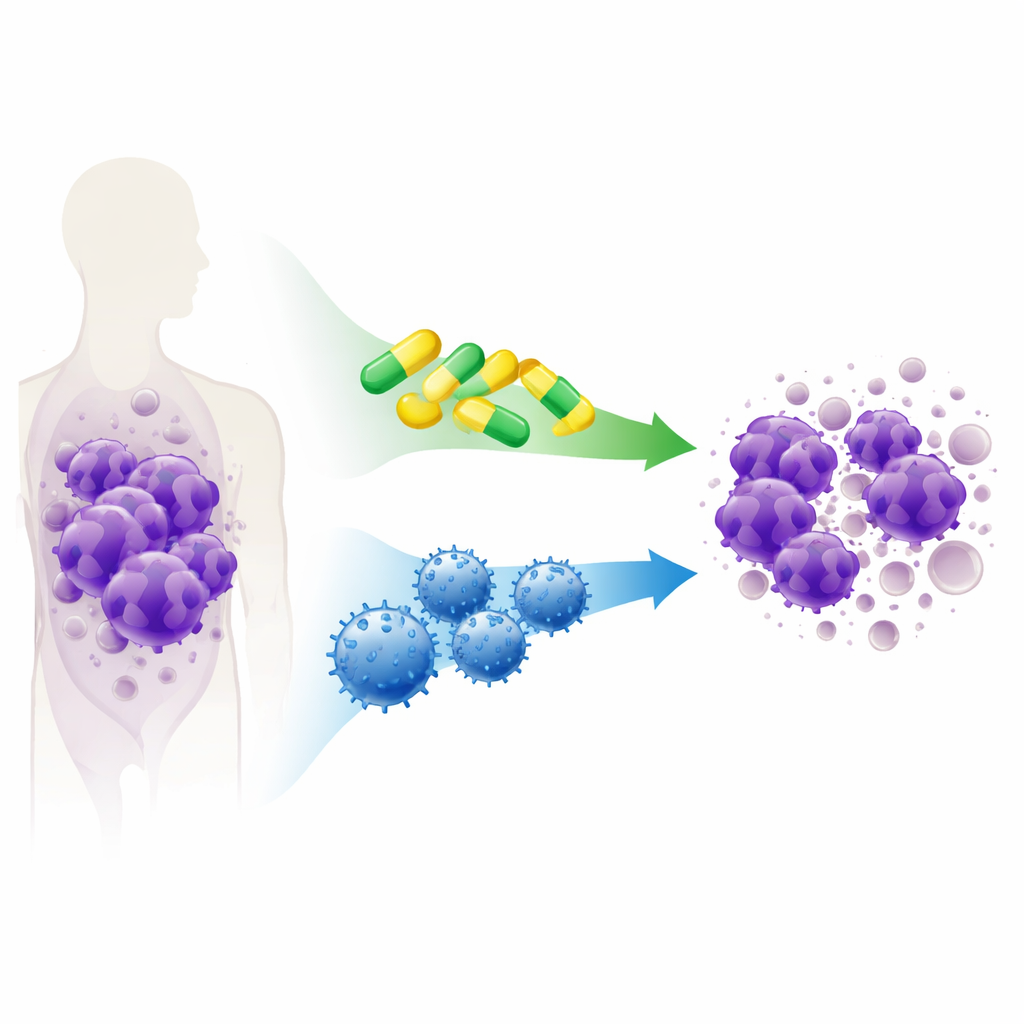
Kanserin Hayatta Kalma Hilelerini Anlamak
Kanser hücreleri sıklıkla hücrenin yerleşik “intihar” mekanizmasını ele geçirerek ölümden kaçınır; bu güvenlik sistemi normalde hasarlı veya tehlikeli hücreleri ortadan kaldırır. T‑ALL’de bu kaçış, hücrenin kendini yok etmesini engelleyen koruyucu bir grup proteine dayanır. Araştırmacılar, bu koruyucu proteinleri etkisiz hale getirmeyi ve dengeyi tekrar hücre ölümüne kaydırmayı amaçlayan deneysel ve onaylı birkaç BH3‑mimetik ilacı test ettiler. Laboratuvar T‑ALL hücre hatları ve gerçek hasta örneklerinden farelerde büyütülen lösemi örnekleri kullanarak farklı koruyucu proteinleri (BCL‑2, BCL‑XL ve MCL‑1) tek başına ve kombinasyon halinde bloke eden ilaçları incelediler.
Hangi Akıllı İlaçlar En İyi İşe Yarıyor?
Çalışma, tüm T‑ALL kanserlerinin aynı hayatta kalma proteinine dayanmadığını ve bunun ilaç yanıtı için büyük önem taşıdığını ortaya koydu. Early T‑cell precursor (ETP) ALL olarak bilinen yüksek riskli bir alt tip, BCL‑2’nin bloke edilmesine özellikle duyarlıydı; bu, bu hücrelerin büyük oranda bu proteine bağımlı olduğuna dair önceki ipuçlarıyla uyumluydu. Buna karşılık, çoğu tipik T‑ALL örneği tek başına BCL‑2’ye ve MCL‑1 inhibitörüne dirençliydi, ancak birçoğu BCL‑XL’in bloke edilmesine oldukça hassastı. Hem BCL‑2 hem BCL‑XL’i hedef alan çift etkili bir ilaç olan AZD4320, özellikle lösemi hücrelerinin protein desenleri bu hedeflere dayandığını gösterdiğinde birçok vakada güçlü etkinlik gösterdi. Araştırmacılar, hücrelerin kendini yok etmeye ne kadar yakın olduğunu ölçen BH3‑profiling adındaki fonksiyonel testi kullandı ve bu testin hangi ilacın veya ilaç karışımının en olası şekilde işe yarayacağını öngörebileceğini gösterdi.
Direnci Yenmek İçin Ölüm Sinyallerini Birleştirmek
Bilim insanları lösemi hücrelerinin zamana bağlı yanıtlarını daha yakından incelediklerinde, tek bir hayatta kalma proteininin bloke edilmesinin sıklıkla hücrelerin bağımlılığını başka bir proteine kaydırdığını gördüler; bu, adeta koruma görevini değiştirmek gibiydi. Örneğin, çift BCL‑2/BCL‑XL ilacı tek başına kullanıldığında hücreler çoğunlukla MCL‑1’e yöneliyordu ve bu da ilacın etkisini azaltabiliyordu. AZD4320’yi bir MCL‑1 inhibitörü ile eşleştirerek araştırmacılar bu kaçış yolunu kestiler. Hem hücre hatlarında hem de aksi halde dirençli olan hasta kökenli örneklerde, bu kombinasyon nispeten düşük dozlarda güçlü ve sıklıkla sinerjik lösemi hücresi öldürmesi sağladı; bu da dikkatle tasarlanmış kombinasyonların tek ilaçları daha yüksek dozlara zorlamaktan daha güçlü ve muhtemelen daha güvenli olabileceğini düşündürüyor.
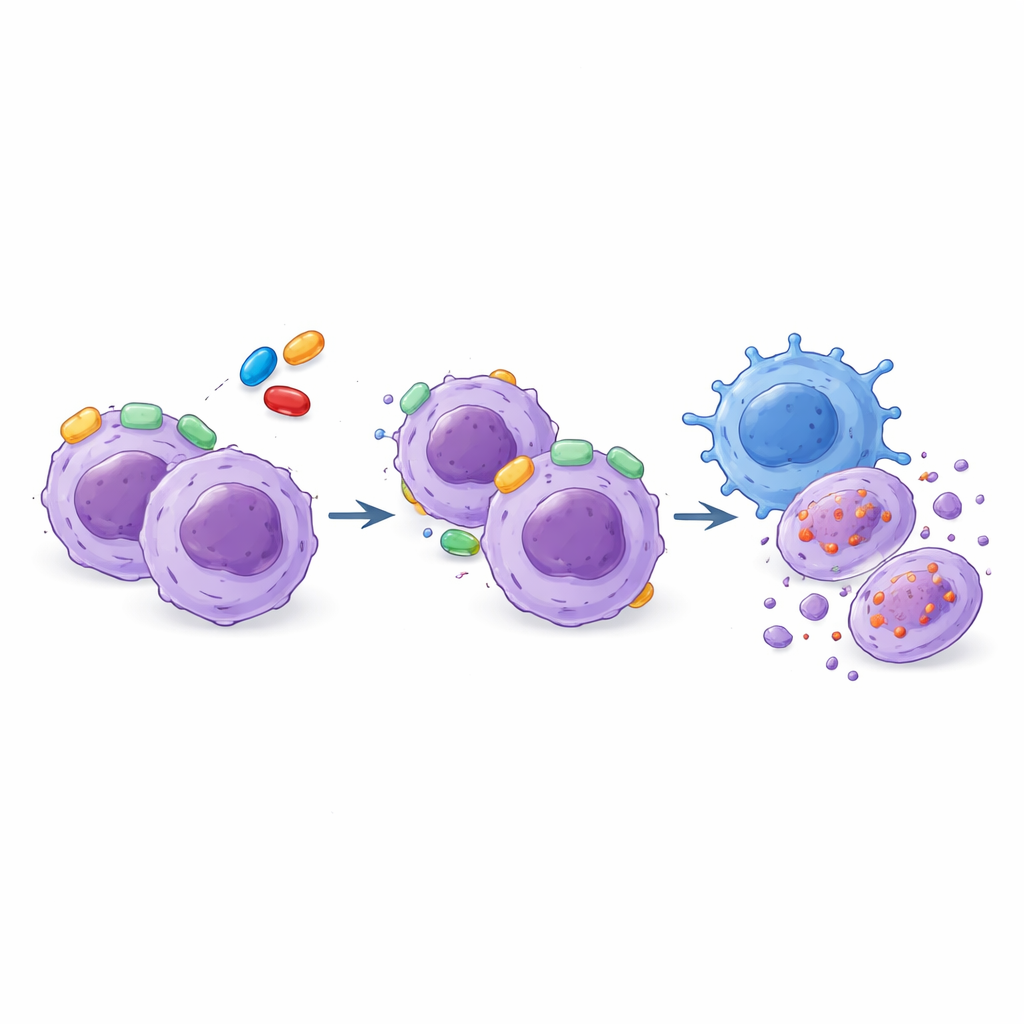
Hedefe Yönelik İlaçlarla Bağışıklık Saldırısını Güçlendirmek
Çalışma ayrıca tamamlayıcı bir stratejiyi de inceledi: önceden eğitime gerek duymadan kanser hücrelerini tanıyıp yok edebilen bir bağışıklık hücresi türü olan doğal öldürücü (NK) hücrelerini kullanmak. T‑ALL örnekleri NK hücrelerine karşı geniş bir duyarlılık aralığı gösterdi, ancak bu desen BH3‑mimetiklere yanıtlarını basitçe yansıtmıyordu; bu da bağışıklık saldırısının bağımsız bir tedavi hattı sunduğunu gösteriyor. Araştırmacılar, NK hücrelerine maruz kalan lösemi hücrelerinin içsel ölüm kontrol devrelerinin değiştiğini ve sıklıkla BCL‑XL’e olan bağımlılığın arttığını buldular. Önemli olarak, NK hücreleri kendileri büyük ölçüde BCL‑2/BCL‑XL ilacı AZD4320’den etkilenmedi. AZD4320 ile NK hücreleri birlikte kullanıldığında, hem hücre hatlarında hem de hasta kökenli örneklerde lösemi hücresi öldürmesi tek başına her bir yaklaşımdan daha sürekli olarak yüksekti; en azından toplanan (additif) faydalar sağlandığı görüldü.
Bu Gelecekteki Hastalar İçin Ne Anlama Gelebilir
Toplu olarak, bu çalışma birçok T‑ALL hücresinin özellikle BCL‑XL’i hedefleyerek hayatta kalma proteinlerini hassas biçimde devre dışı bırakıldığında kendi kendine yok olmaya zorlanabileceğini ve farklı BH3‑mimetik ilaçların kombinasyonunun aksi halde inatçı olan örneklerde direnci aşabileceğini gösteriyor. Bulgular ayrıca bu akıllı ilaçları NK hücre tabanlı immünoterapi ile eşleştirmenin lösemiyi daha da zayıflatabileceğini ve tedavi için gerekli bağışıklık hücrelerine zarar vermeden öldürmeyi iyileştirebileceğini öne sürüyor. Bu sonuçlar laboratuvar ve hayvan modellerinden gelmekle birlikte klinik çalışmalardan değil, yüksek riskli veya nüks etmiş T‑ALL hastalarında kombine BH3‑mimetik ve NK hücre tedavilerinin test edilmesi için güçlü bir bilimsel temel sunuyor; uzun vadeli hedef daha etkili ve daha az toksik tedavi seçenekleri sağlamaktır.
Atıf: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
Anahtar kelimeler: T hücre akut lenfoblastik lösemi, BH3-mimetik tedavi, BCL-XL inhibisyonu, doğal öldürücü hücre immünoterapisi, apoptoza yönelik tedavi