Clear Sky Science · ru
Терапевтический потенциал BH3‑миметиков и NK‑клеточно‑опосредованной иммунотерапии при Т‑ALL
Новые способы помочь организму бороться с агрессивным раком крови
Т‑клеточный острый лимфобластный лейкоз (T‑ALL) — это агрессивный рак крови, который в основном поражает детей и молодых взрослых и часто лечится интенсивной химиотерапией. Хотя такие методы излечивают многих пациентов, они вызывают тяжёлые побочные эффекты и не всегда эффективны, особенно после рецидива. В этом исследовании изучаются два более целенаправленных подхода — умные препараты, которые заставляют раковые клетки самоуничтожаться, и иммунные клетки, поражающие опухоли — чтобы понять, могут ли они предложить более безопасные и эффективные варианты для больных T‑ALL.
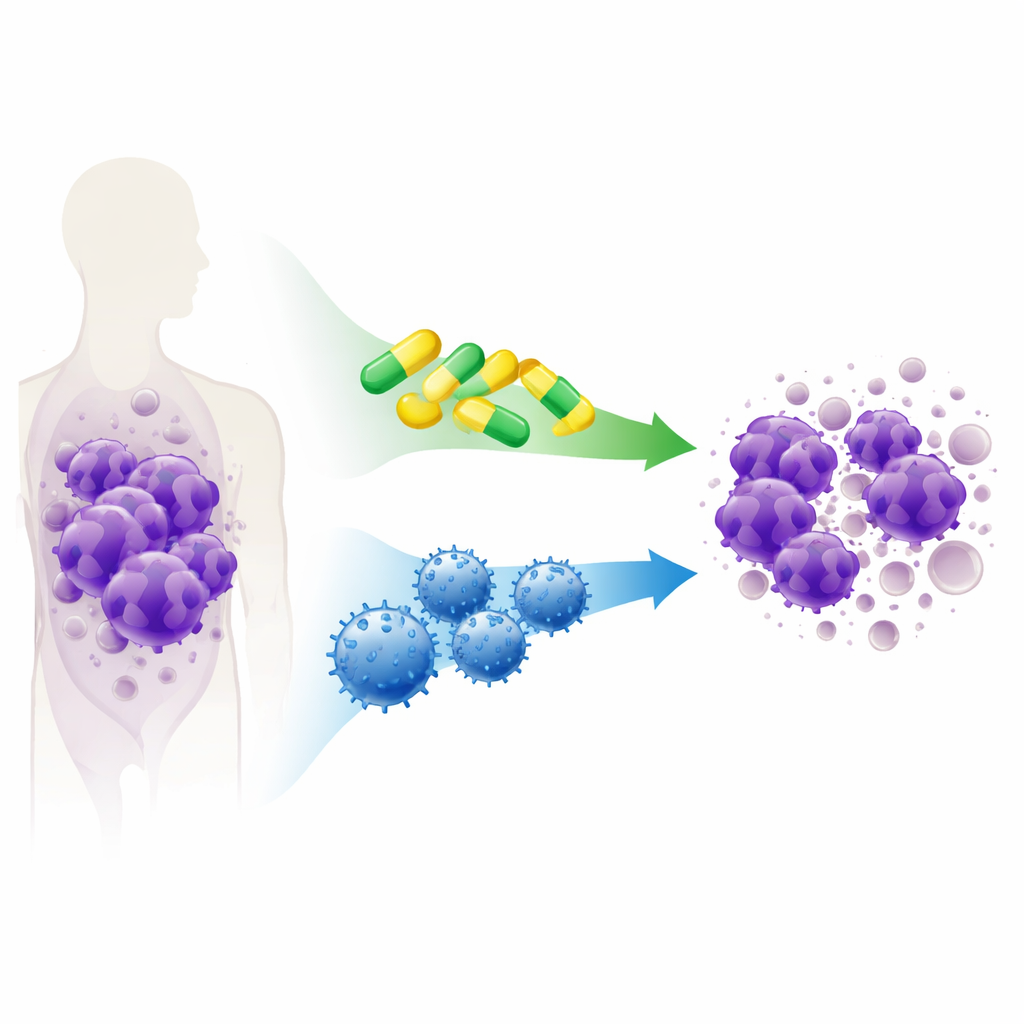
Понимание трюков выживания рака
Раковые клетки часто избегают гибели, захватывая встроенный «механизм самоубийства» клетки — систему безопасности, которая обычно удаляет повреждённые или опасные клетки. В T‑ALL это уклонение опирается на группу белков, действующих как телохранители, мешающие запуску самоуничтожения. Исследователи протестировали несколько экспериментальных и одобренных препаратов, называемых BH3‑миметиками, которые разработаны для выведения этих телохранителей из строя и восстановления баланса в пользу гибели клетки. Используя лабораторные линии клеток T‑ALL и образцы лейкемии, выращенные в мышах от реальных пациентов, они оценивали препараты, блокирующие разные белки‑телохранители (BCL‑2, BCL‑XL и MCL‑1) по отдельности и в комбинации.
Какие «умные» препараты работают лучше всего?
Команда обнаружила, что не все T‑ALL зависят от одного и того же белка выживания, и это существенно влияло на ответ на лекарства. Высокорискованный подтип, называемый ранним T‑клеточным предшественником (ETP) ALL, оказался особенно уязвим к блокаде BCL‑2, что согласуется с предыдущими предположениями о сильной зависимости этих клеток от данного белка. Напротив, большинство типичных образцов T‑ALL были устойчивы к BCL‑2 и к ингибитору MCL‑1 при монотерапии, но многие оказались чувствительны к блокаде BCL‑XL. Двухдействующий препарат, воздействующий на BCL‑2 и BCL‑XL, AZD4320, продемонстрировал высокую активность во многих случаях, особенно когда профиль белков лейкозных клеток указывал на зависимость от этих мишеней. Исследователи использовали функциональный тест BH3‑профилирование, который измеряет, насколько близки клетки к запуску самоуничтожения, и показали, что этот анализ может предсказать, какой препарат или их сочетание наиболее вероятно сработают.
Комбинация сигналов смерти для преодоления резистентности
При более тщательном изучении реакции лейкозных клеток во времени исследователи заметили, что блокада одного белка выживания часто заставляла клетки переключаться на зависимость от другого, словно меняя телохранителей. Например, при использовании одного только двухцелевого препарата BCL‑2/BCL‑XL клетки часто переходили к опоре на MCL‑1, что могло ослаблять эффект лекарства. Сочетание AZD4320 с ингибитором MCL‑1 перекрывало этот путь ухода. В клеточных линиях и образцах, полученных от пациентов и иначе резистентных, комбинация вызывала сильное и зачастую синергетическое уничтожение лейкозных клеток при относительно низких дозах, что указывает на то, что тщательно подобранные сочетания могут быть более мощными и, возможно, безопаснее, чем повышение дозы одного препарата.
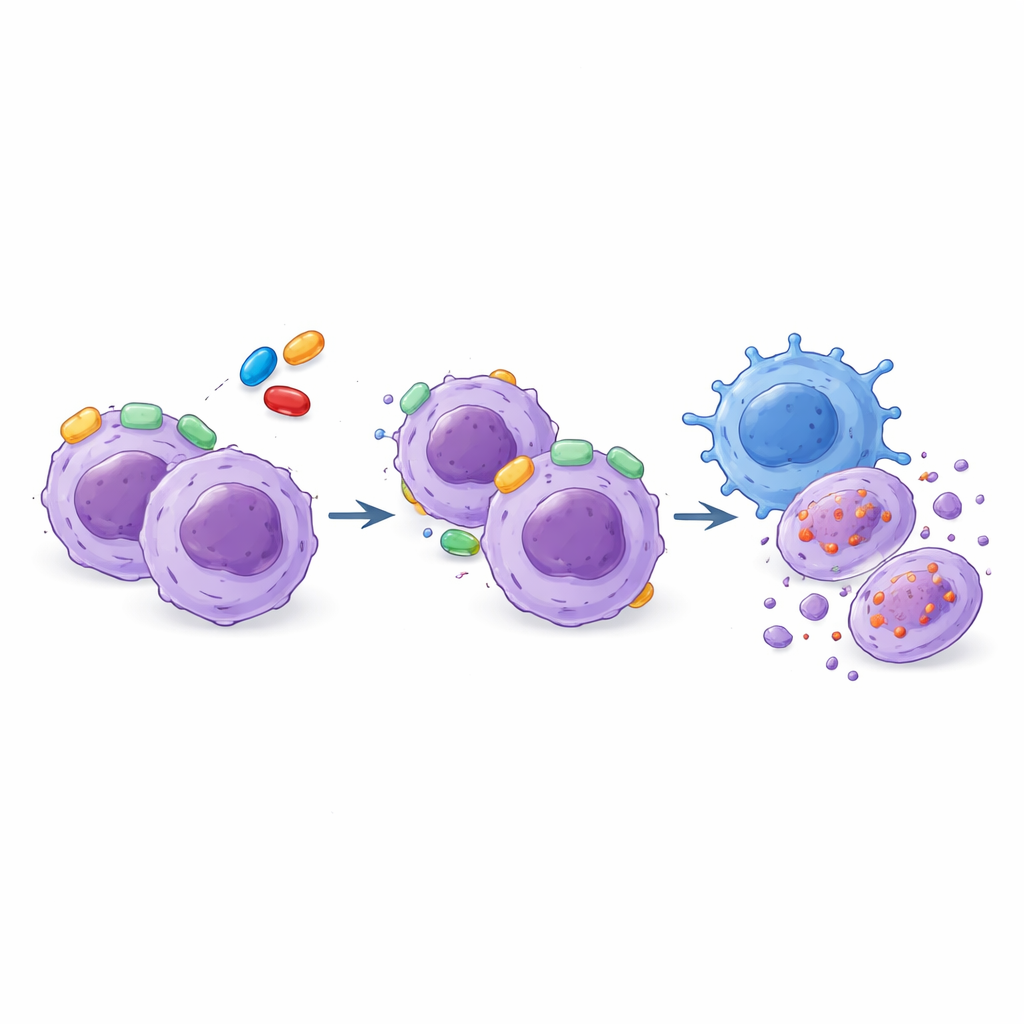
Усиление иммунной атаки с помощью целенаправленных препаратов
Исследование также рассмотрело дополнительную стратегию: использование натуральных киллеров (NK‑клеток), типа иммунных клеток, которые могут распознавать и уничтожать раковые клетки без предварительной подготовки. Образцы T‑ALL демонстрировали широкий диапазон чувствительности к NK‑клеткам, но этот паттерн не просто повторял их ответ на BH3‑миметики, что означает — иммунная атака представляет отдельную терапевтическую линию. Исследователи обнаружили, что воздействие NK‑клеток на лейкозные клетки меняет их внутреннюю схему контроля смерти, часто повышая зависимость от BCL‑XL. Важно, что сами NK‑клетки в значительной мере не затрагивались двухцелевым препаратом AZD4320. При комбинировании AZD4320 с NK‑клетками уничтожение лейкозных клеток было последовательно выше, чем при каждом из подходов по‑отдельности, как в клеточных линиях, так и в образцах от пациентов, что указывает как минимум на аддитивный эффект.
Что это может значить для будущих пациентов
В целом работа показывает, что многие клетки T‑ALL можно заставить к самоуничтожению при точечном нацеливании на их белки выживания, особенно BCL‑XL, и что комбинация разных BH3‑миметиков может преодолеть резистентность в стойких образцах. Результаты также предполагают, что сопряжение этих «умных» препаратов с NK‑клеточно‑основанной иммунотерапией может дополнительно ослабить лейкоз и усилить убийство клеток, не повреждая при этом иммунные клетки, необходимые для лечения. Хотя эти результаты получены на лабораторных и животных моделях, а не в клинических испытаниях, они дают прочную научную основу для проверки сочетанных BH3‑миметиков и NK‑клеточных терапий у пациентов с высокорискованным или рецидивирующим T‑ALL, с долгосрочной надеждой на более эффективные и менее токсичные варианты лечения.
Цитирование: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
Ключевые слова: Т‑клеточный острый лимфобластный лейкоз, терапия BH3‑миметиками, ингибиция BCL‑XL, иммунотерапия натуральными киллерами, лечение, нацеленное на апоптоз