Clear Sky Science · it
Potenziale terapeutico dei mimetici BH3 e dell’immunoterapia mediata da cellule NK nella T-ALL
Nuove strade per aiutare l’organismo a combattere un tumore del sangue difficile
La leucemia linfoblastica acuta a cellule T (T‑ALL) è un tumore ematologico aggressivo che colpisce soprattutto bambini e giovani adulti ed è spesso trattato con chemioterapie intensive. Pur potendo guarire molti pazienti, questi trattamenti causano effetti collaterali importanti e non sono efficaci per tutti, soprattutto dopo una recidiva. Questo studio esplora due strategie più recenti e mirate — farmaci intelligenti che inducono l’autodistruzione delle cellule tumorali e cellule immunitarie che cacciano i tumori — per valutare se possano offrire opzioni più sicure ed efficaci per le persone con T‑ALL.
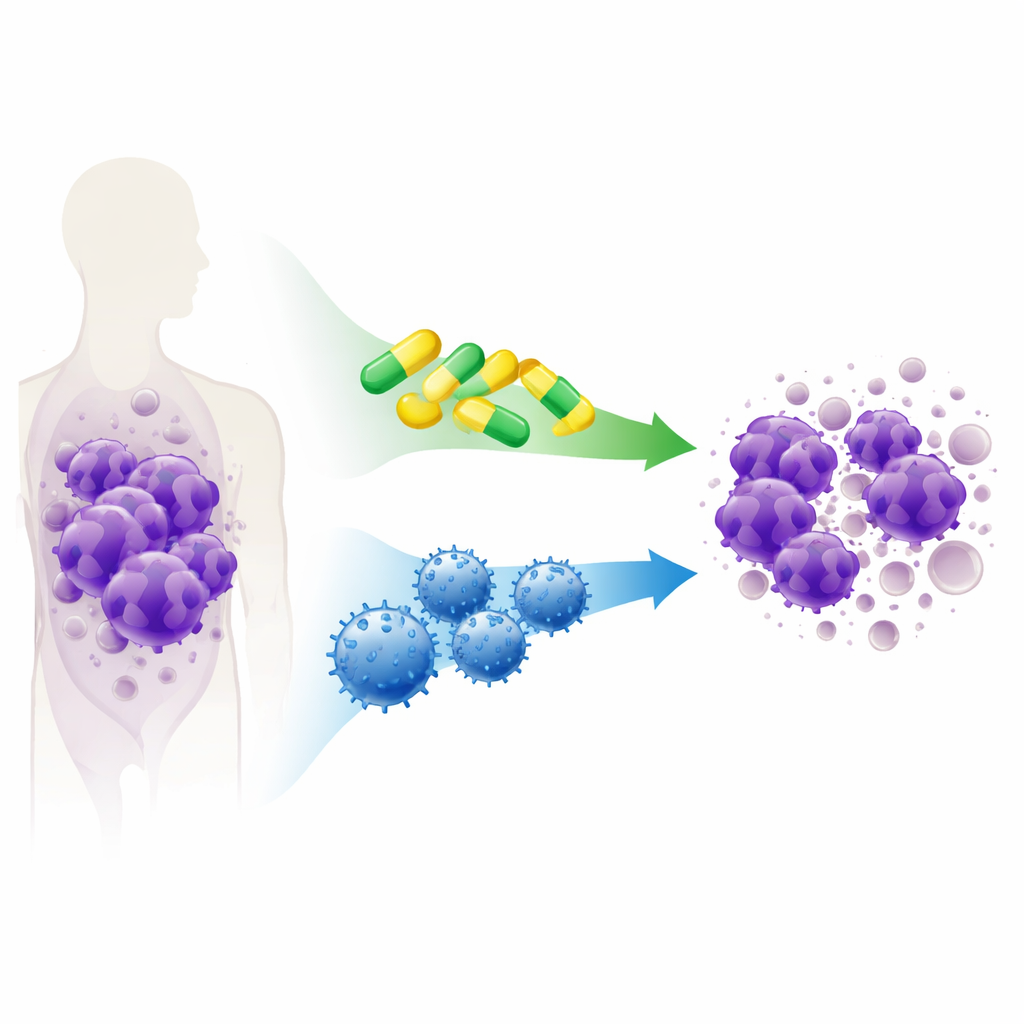
Capire i trucchi che usano le cellule tumorali per sopravvivere
Le cellule tumorali spesso sfuggono alla morte dirottando il meccanismo cellulare di “suicidio”, un sistema di sicurezza che normalmente rimuove cellule danneggiate o pericolose. Nella T‑ALL questa fuga si basa su un gruppo di proteine che agiscono come guardie del corpo, impedendo alla cellula di attivare l’autodistruzione. I ricercatori hanno testato diversi farmaci sperimentali e approvati chiamati mimetici BH3, progettati per disarmare queste guardie del corpo e riportare l’equilibrio verso la morte cellulare. Utilizzando linee cellulari di T‑ALL in laboratorio e campioni di leucemia impiantati in topi a partire da pazienti reali, hanno esaminato farmaci che bloccano diverse proteine‑guardiane (BCL‑2, BCL‑XL e MCL‑1) da soli e in combinazione.
Quali farmaci mirati funzionano meglio?
Il gruppo ha scoperto che non tutte le T‑ALL dipendono dalla stessa proteina di sopravvivenza, e questo ha un grande impatto sulla risposta ai farmaci. Un sottotipo ad alto rischio chiamato early T‑cell precursor (ETP) ALL era particolarmente vulnerabile al blocco di BCL‑2, in linea con indicazioni precedenti che queste cellule dipendono fortemente da quella proteina. Al contrario, la maggior parte dei campioni di T‑ALL tipici risultava resistente a BCL‑2 e al singolo inibitore di MCL‑1, ma molti erano sensibili al blocco di BCL‑XL. Un farmaco ad azione duale che colpisce sia BCL‑2 sia BCL‑XL, AZD4320, ha mostrato forte attività in molti casi, soprattutto quando il profilo proteico delle cellule leucemiche suggeriva tale dipendenza. I ricercatori hanno utilizzato un test funzionale chiamato BH3‑profiling, che misura quanto le cellule siano vicine all’attivazione dell’autodistruzione, dimostrando che questo saggio può prevedere quale farmaco o combinazione sia più probabile che funzioni.
Combinare i segnali di morte per superare la resistenza
Analizzando più a fondo la risposta delle cellule leucemiche nel tempo, gli scienziati hanno osservato che il blocco di una proteina di sopravvivenza spesso induceva le cellule a spostare la loro dipendenza su un’altra, un po’ come cambiare guardie del corpo. Per esempio, quando il farmaco duale BCL‑2/BCL‑XL veniva usato da solo, le cellule spesso passavano a dipendere da MCL‑1, il che poteva attenuarne l’effetto. Associando AZD4320 a un inibitore di MCL‑1, i ricercatori hanno chiuso questa via di fuga. Sia nelle linee cellulari sia nei campioni derivati da pazienti altrimenti resistenti, la combinazione ha determinato un’uccisione marcata e spesso sinergica delle cellule leucemiche a dosi relativamente basse, suggerendo che combinazioni progettate con cura potrebbero essere più potenti e forse più sicure rispetto a spingere un singolo farmaco a dosi maggiori.
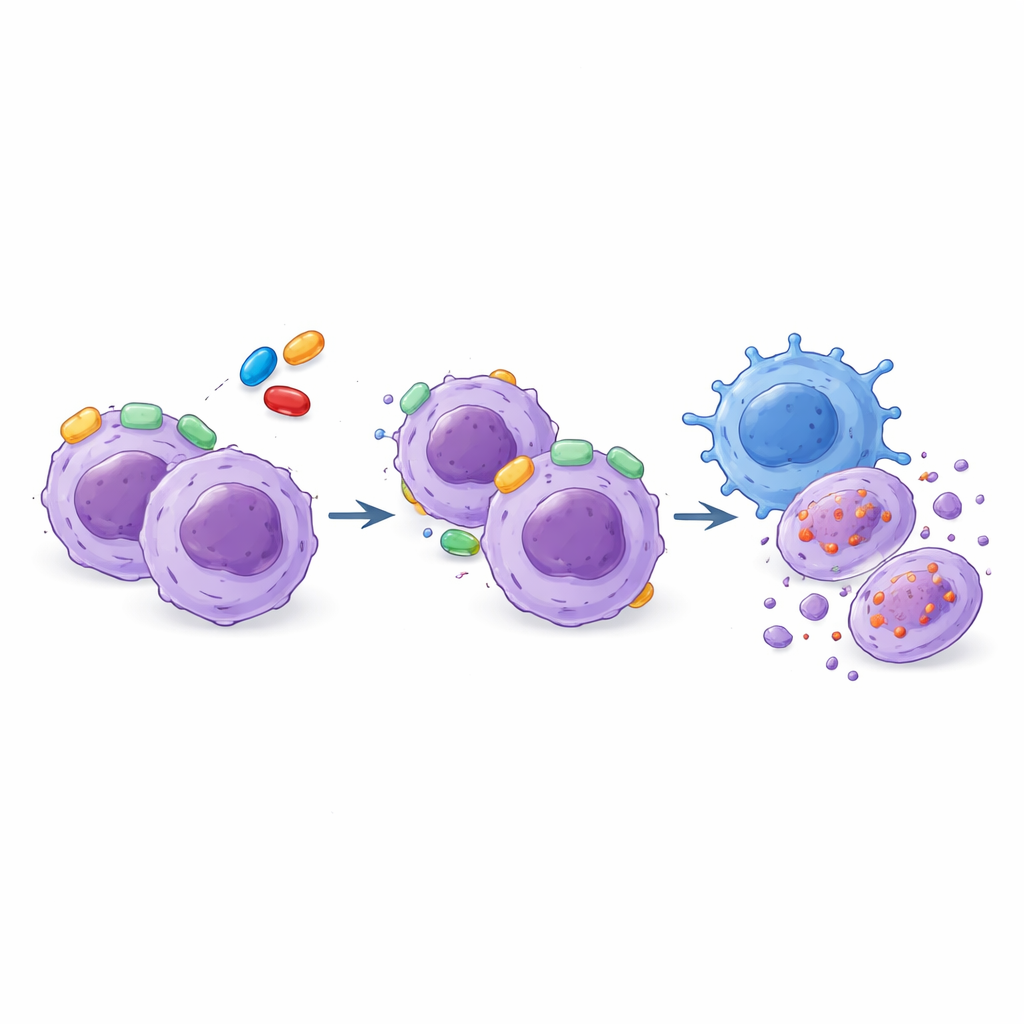
Rafforzare l’attacco immunitario con farmaci mirati
Lo studio ha inoltre esplorato una strategia complementare: l’utilizzo delle cellule natural killer (NK), un tipo di cellula immunitaria in grado di riconoscere e distruggere cellule tumorali senza addestramento precedente. I campioni di T‑ALL mostravano una vasta gamma di sensibilità alle NK, ma questo schema non rispecchiava semplicemente la loro risposta ai mimetici BH3, il che significa che l’attacco immunitario offre una linea terapeutica indipendente. I ricercatori hanno osservato che l’esposizione delle cellule leucemiche alle NK modificava il loro wiring interno dei controlli della morte, aumentando spesso la dipendenza da BCL‑XL. È importante che le stesse cellule NK fossero in larga parte non influenzate dal farmaco BCL‑2/BCL‑XL AZD4320. Quando AZD4320 è stato combinato con le NK, l’uccisione delle cellule leucemiche è risultata costantemente maggiore rispetto a ciascun approccio da solo, sia nelle linee cellulari sia nei campioni derivati da pazienti, indicando benefici almeno additivi.
Cosa potrebbe significare per i pazienti futuri
Nel complesso, il lavoro mostra che molte cellule di T‑ALL possono essere costrette all’autodistruzione colpendo con precisione le loro proteine di sopravvivenza, in particolare BCL‑XL, e che combinare diversi mimetici BH3 può superare la resistenza in campioni altrimenti refrattari. I risultati suggeriscono anche che associare questi farmaci “intelligenti” con l’immunoterapia basata su cellule NK potrebbe indebolire ulteriormente la leucemia e migliorare l’uccisione senza danneggiare le cellule immunitarie necessarie al trattamento. Pur essendo risultati provenienti da modelli di laboratorio e animali anziché da trial clinici, forniscono una solida base scientifica per testare in pazienti con T‑ALL ad alto rischio o recidivata terapie combinate di mimetici BH3 e cellule NK, con la speranza a lungo termine di opzioni terapeutiche più efficaci e meno tossiche.
Citazione: Fortner, C., Niedermayer, A., Bäuerle, M.M. et al. Therapeutic potential of BH3-mimetics and NK cell-mediated immunotherapy in T-ALL. Cell Death Dis 17, 387 (2026). https://doi.org/10.1038/s41419-026-08698-x
Parole chiave: Leucemia linfoblastica acuta a cellule T, Terapia con mimetici BH3, Inibizione di BCL-XL, Immunoterapia con cellule natural killer, Trattamento mirato all’apoptosi