Clear Sky Science · zh
CDX2通过上调NUPR1在II–III期结直肠癌中赋予抗铁死亡能力
这对结肠癌患者意味着什么
许多II–III期结肠癌患者面临一个艰难抉择:化疗可降低癌症复发的风险,但同时会带来严重副作用。医生注意到含有高水平CDX2蛋白的肿瘤通常侵袭性较低,但这些肿瘤往往对化疗反应较差。本研究探讨了这一悖论的原因,并揭示了某些结肠癌细胞用来躲避一种新型、与铁相关的细胞死亡方式的隐蔽生存策略。
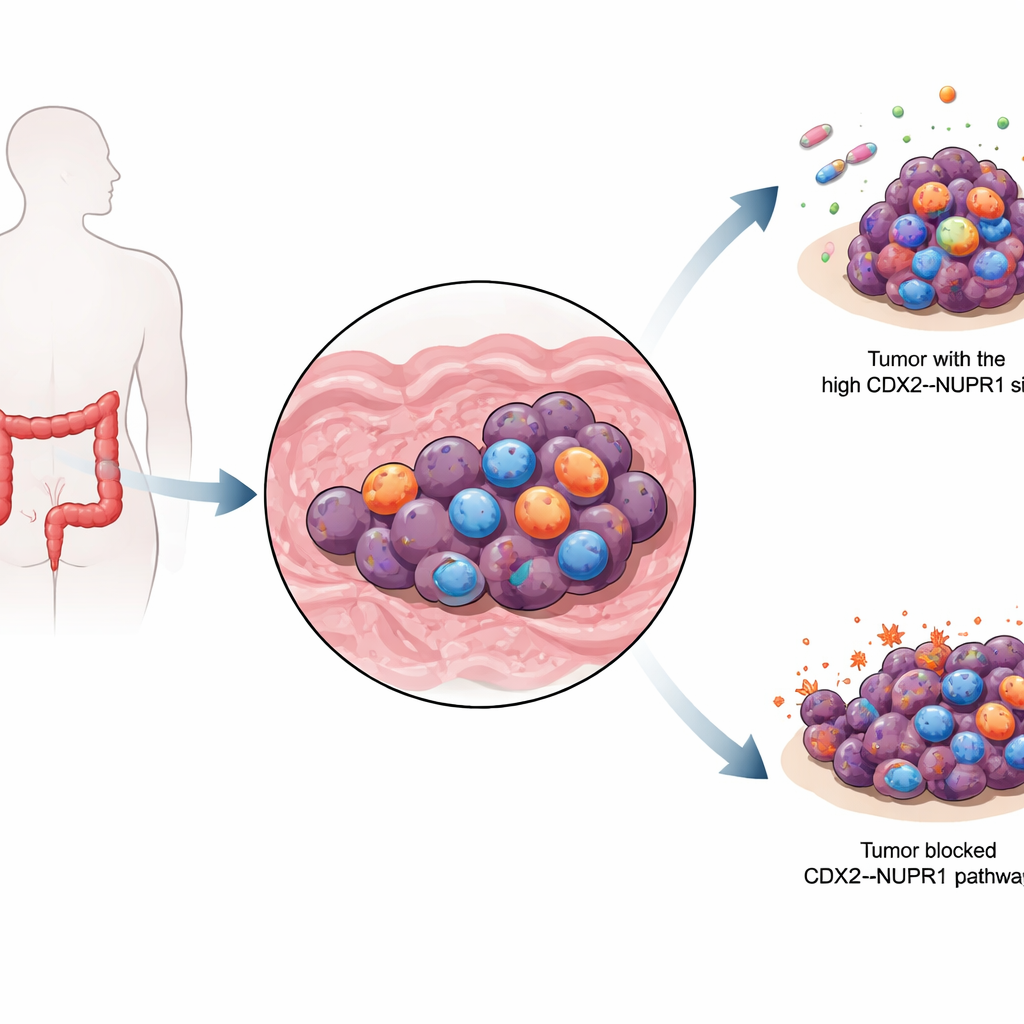
癌细胞的铁脆弱性
癌细胞对铁的需求异常旺盛:铁有助于其生长,但若积累过多也会致命。当铁与细胞膜中的脂质反应时,会触发一种称为铁死亡(ferroptosis)的细胞死亡形式,这与更常见的程序性细胞死亡——凋亡不同。由于许多耐药癌细胞仍依赖铁,研究者对能促使其发生铁死亡的药物充满兴趣。但肿瘤可以进化出针对这一过程的防御,从而削弱常规化疗和诱导铁死亡药物的效果。
CDX2在结肠肿瘤中的双重角色
CDX2是一种维持肠道上皮细胞健康与身份的蛋白。在结肠肿瘤中丧失CDX2通常与更具侵袭性和更差的生存率相关。然而令人费解的是,保留CDX2的患者从化疗中获益往往更少。为探明这一矛盾,作者在多种人类结肠癌细胞系和小鼠肿瘤模型中操纵了CDX2表达。他们发现,增加CDX2使癌细胞对5‑氟尿嘧啶和奥沙利铂等常用药物更难杀死;相反,降低CDX2则使肿瘤对治疗更敏感并在治疗下更易缩小。
阻断细胞死亡的压力反应开关
进一步研究中,团队通过基因表达分析和数百例患者的组织样本锁定了另一种蛋白NUPR1,其在II–III期结肠癌中与CDX2水平密切相关。NUPR1是一种帮助细胞应对损伤(包括氧化应激)的应激反应因子。研究者证明,CDX2可直接结合NUPR1基因的调控区并激活其表达。当NUPR1水平升高时,癌细胞内铁的积累减少、产生活性含氧分子减少,脂质和DNA损伤的标志也降低——这些都是铁死亡抵抗的特征。如果去除NUPR1,CDX2就无法再保护细胞免受铁死亡;相反,在缺乏CDX2的细胞中恢复NUPR1则重新带回了耐受性。
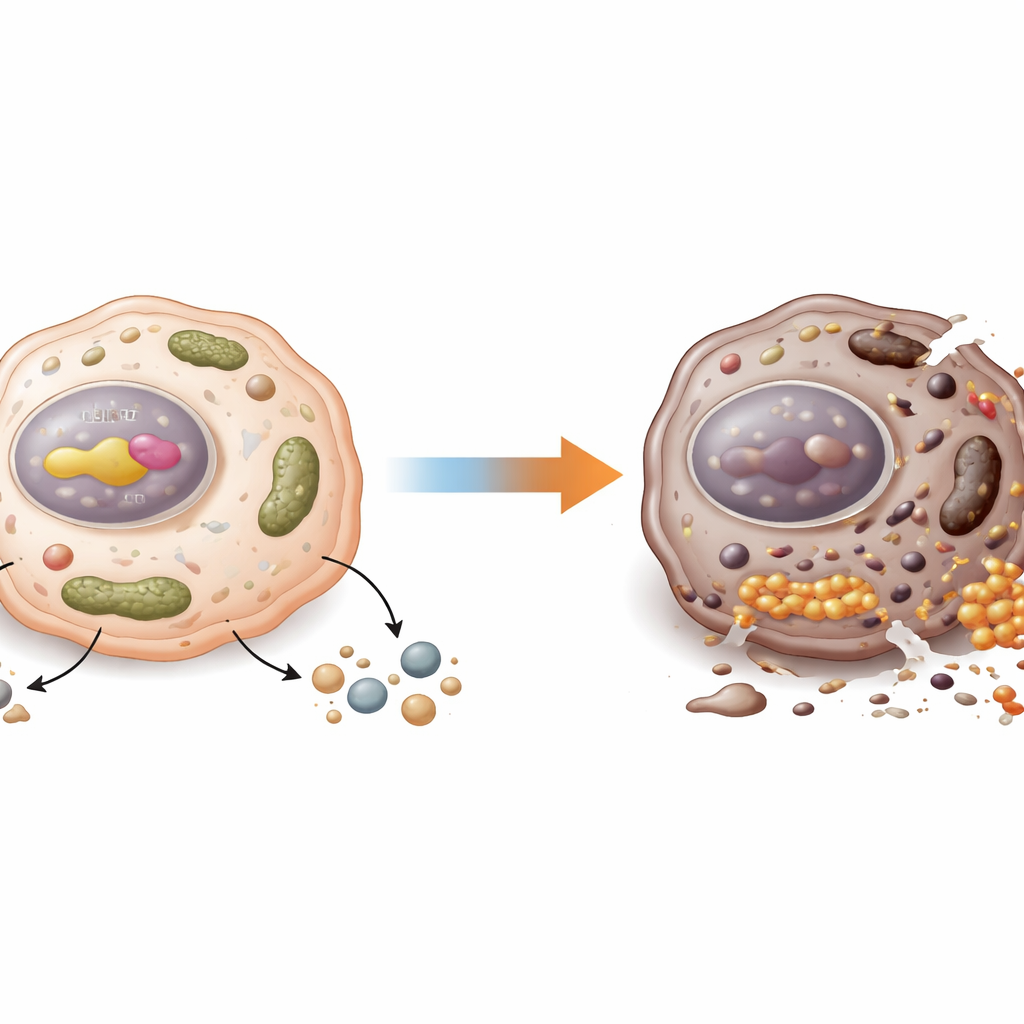
将护盾变为阿喀琉斯之踵
这些分子学发现随后在小鼠中得到验证。缺失CDX2或NUPR1的肿瘤对一种名为IKE的诱导铁死亡化合物反应更好,表现为更多的铁和脂质损伤并比对照肿瘤缩小更多。研究团队还使用了来源于患者的肿瘤移植模型以模拟真实世界的结肠癌。在高CDX2和高NUPR1的肿瘤中,加入NUPR1的小分子抑制剂(ZZW‑115)使5‑氟尿嘧啶的标准化疗更为有效,并在癌细胞内增强了类似铁死亡的特征。在低CDX2和低NUPR1的肿瘤中,同样的抑制剂几乎没有额外益处,这表明该策略最有希望用于特定亚组的患者。
这对未来治疗可能意味着什么
简言之,该研究表明许多CDX2阳性的结肠癌借助一种以NUPR1为主的内在护盾躲避铁驱动的细胞死亡。通过关闭这一护盾——无论是基因手段还是像ZZW‑115这样的药物——医生可能重新暴露癌细胞,使其对化疗和诱导铁死亡的药物恢复致死敏感性。尽管仍需在人体中做更多工作,但研究结果表明,对肿瘤进行CDX2和NUPR1检测,可能有助于识别那些最有可能从刻意促使癌细胞发生铁死亡的治疗中获益的患者,而不是让肿瘤悄然抵抗并复发。
引用: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
关键词: 结肠癌, CDX2, 铁死亡, NUPR1, 化疗耐药