Clear Sky Science · fr
CDX2 confère une résistance à la ferroptose dans le cancer du côlon de stade II–III via la surexpression de NUPR1
Pourquoi c’est important pour les personnes atteintes d’un cancer du côlon
De nombreux patients atteints d’un cancer du côlon de stade II–III font face à un difficile compromis : la chimiothérapie peut réduire le risque de récidive, mais entraîne aussi des effets secondaires importants. Les cliniciens savent que les tumeurs exprimant fortement une protéine appelée CDX2 ont souvent un comportement moins agressif, et pourtant ces mêmes tumeurs répondent moins bien à la chimiothérapie. Cette étude explore l’origine de ce paradoxe et révèle un stratagème de survie caché que certaines cellules du cancer du côlon utilisent pour échapper à une forme de mort cellulaire liée au fer, récemment décrite.
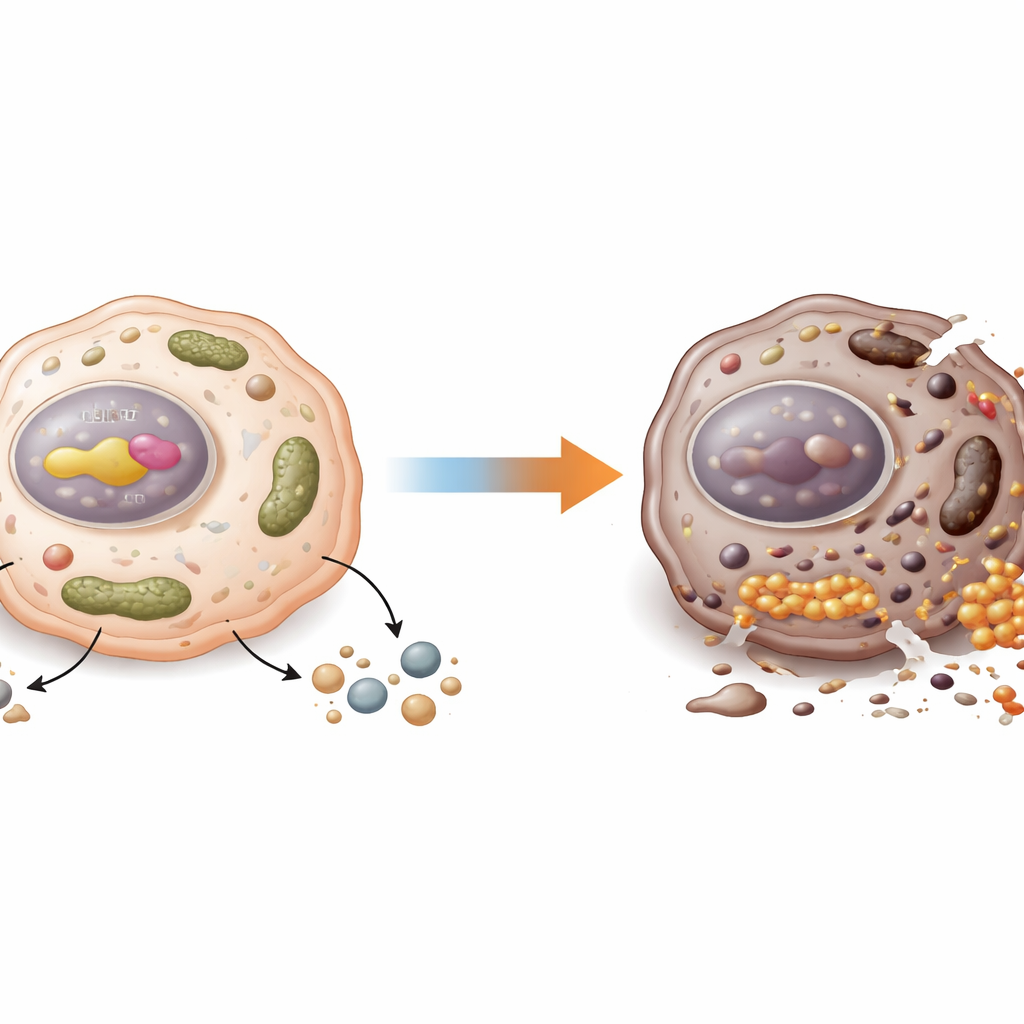
La vulnérabilité au fer d’une cellule cancéreuse
Les cellules cancéreuses sont anormalement avides de fer, un métal qui favorise leur croissance mais qui peut aussi les détruire s’il s’accumule trop. Quand le fer réagit avec les lipides des membranes cellulaires, il peut déclencher une forme de mort cellulaire appelée ferroptose, distincte du programme suicidaire mieux connu qu’est l’apoptose. Parce que de nombreuses cellules cancéreuses résistantes aux médicaments dépendent encore du fer, les chercheurs s’intéressent aux médicaments qui les poussent vers la ferroptose. Mais les tumeurs peuvent évoluer et développer des défenses contre ce processus, atténuant l’effet de la chimiothérapie standard comme des agents inducteurs de ferroptose.
La double vie de CDX2 dans les tumeurs du côlon
CDX2 est une protéine qui contribue normalement au maintien de l’intégrité et de l’identité des cellules qui tapissent l’intestin. La perte de CDX2 dans les tumeurs du côlon est souvent associée à une maladie plus agressive et à un pronostic plus mauvais. Pourtant, de façon troublante, les patients dont les tumeurs conservent CDX2 tirent parfois moins de bénéfice de la chimiothérapie. Pour sonder cette contradiction, les auteurs ont manipulé CDX2 dans plusieurs lignées cellulaires humaines de cancer du côlon et dans des modèles tumoraux murins. Ils ont constaté qu’une augmentation de CDX2 rendait les cellules cancéreuses plus difficiles à éliminer avec des médicaments courants comme le 5‑fluorouracile et l’oxaliplatine, tandis que la diminution de CDX2 avait l’effet inverse : les tumeurs devenaient plus sensibles et se réduisaient davantage sous traitement.
Un commutateur de réponse au stress qui bloque la mort cellulaire
En creusant davantage, l’équipe a utilisé des analyses d’expression génique et des échantillons tissulaires de centaines de patients pour identifier une autre protéine, NUPR1, qui corrélait étroitement avec les niveaux de CDX2 dans les cancers du côlon de stade II–III. NUPR1 est un facteur de réponse au stress qui aide les cellules à faire face aux dommages, y compris au stress oxydatif. Les chercheurs ont montré que CDX2 se lie directement à la région régulatrice du gène NUPR1 et l’active. Lorsque NUPR1 est augmenté, les cellules cancéreuses accumulent moins de fer, produisent moins de molécules oxydantes délétères et présentent moins de signes de dommages lipidiques et d’ADN — autant de caractéristiques d’une résistance à la ferroptose. Si NUPR1 est supprimé, CDX2 ne peut plus protéger les cellules de la ferroptose ; inversement, restaurer NUPR1 dans des cellules déficientes en CDX2 rétablit leur résistance.
Transformer le bouclier en talon d’Achille
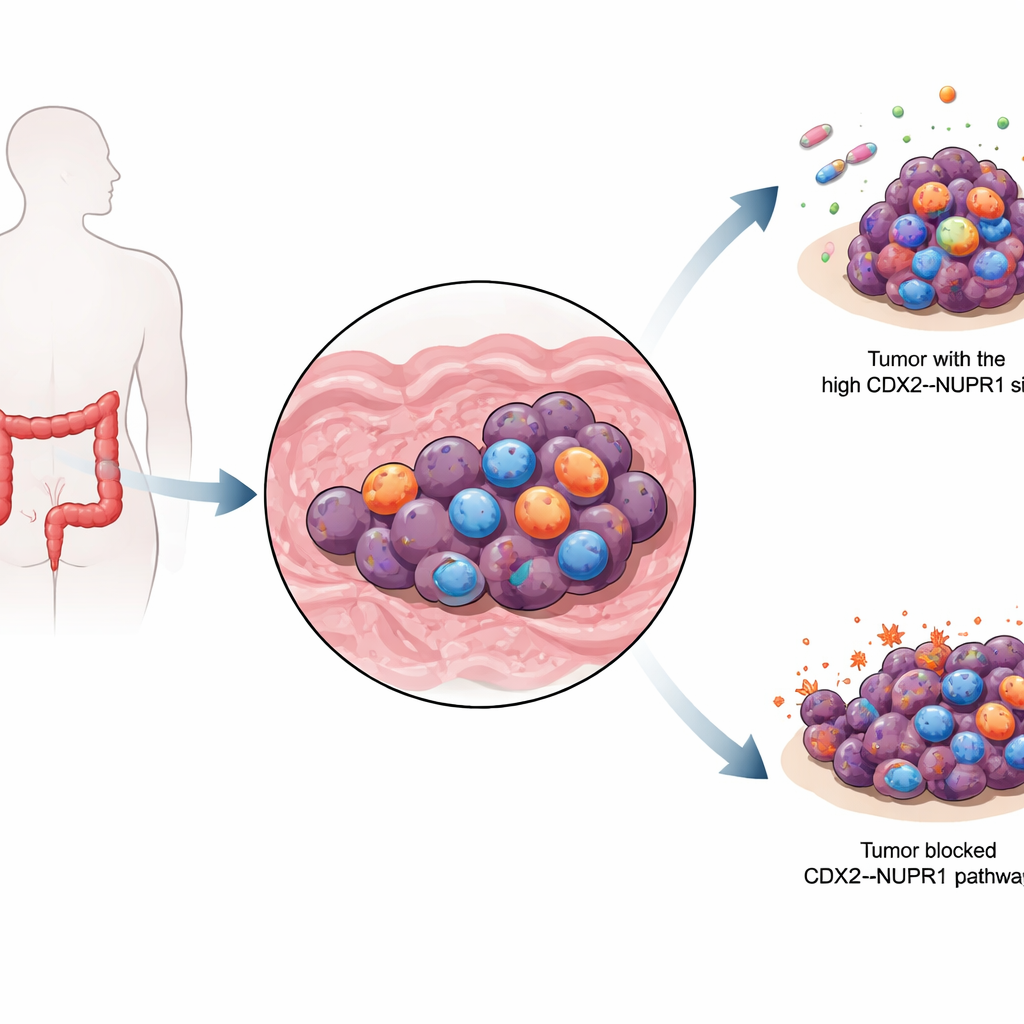
Ces découvertes moléculaires ont été testées chez la souris. Les tumeurs dépourvues de CDX2 ou de NUPR1 répondaient beaucoup mieux à un composé inducteur de ferroptose appelé IKE, accumulant davantage de fer et de lésions lipidiques et se réduisant plus que les tumeurs témoins. L’équipe a aussi utilisé des greffes tumorales dérivées de patients pour reproduire des cancers du côlon tels qu’ils se présentent dans la réalité. Dans les tumeurs exprimant fortement CDX2 et NUPR1, l’ajout d’un inhibiteur de petite molécule de NUPR1 (ZZW‑115) rendait la chimiothérapie standard au 5‑fluorouracile bien plus efficace et renforçait les caractéristiques de type ferroptose à l’intérieur des cellules cancéreuses. Dans les tumeurs à faible CDX2 et NUPR1, le même inhibiteur apportait peu d’avantage, suggérant que cette stratégie est surtout prometteuse pour un sous‑groupe spécifique de patients.
Ce que cela pourrait signifier pour les traitements futurs
En résumé, l’étude montre que de nombreux cancers du côlon CDX2‑positifs se cachent derrière un bouclier intégré contre la mort cellulaire induite par le fer, et que ce bouclier est en grande partie alimenté par NUPR1. En désactivant ce bouclier — génétiquement ou avec un médicament comme ZZW‑115 — il pourrait être possible de réexposer les cellules cancéreuses au potentiel létal de la chimiothérapie et des agents inducteurs de ferroptose. Bien que des essais supplémentaires chez l’humain soient nécessaires, les résultats suggèrent que doser CDX2 et NUPR1 dans les tumeurs pourrait aider à identifier les patients les plus susceptibles de bénéficier de traitements visant délibérément à pousser les cellules cancéreuses vers la ferroptose plutôt que de les laisser résister et récidiver.
Citation: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
Mots-clés: cancer du côlon, CDX2, ferroptose, NUPR1, résistance à la chimiothérapie