Clear Sky Science · nl
CDX2 geeft ferroptoseresistentie in stadium II–III colonkanker via opregulatie van NUPR1
Waarom dit belangrijk is voor mensen met dikkedarmkanker
Veel patiënten met stadium II–III dikkedarmkanker staan voor een lastige afweging: chemotherapie kan de kans op terugkeer van de tumor verkleinen, maar gaat ook gepaard met ernstige bijwerkingen. Artsen weten dat tumoren met hoge niveaus van een eiwit genaamd CDX2 vaak minder agressief zijn, maar dezezelfde tumoren reageren paradoxaal genoeg juist slechter op chemotherapie. Deze studie onderzoekt waarom die tegenstelling bestaat en onthult een verborgen overlevingstruc die sommige darmkankercellen gebruiken om een nieuwere, ijzergerelateerde vorm van celdood te ontwijken.
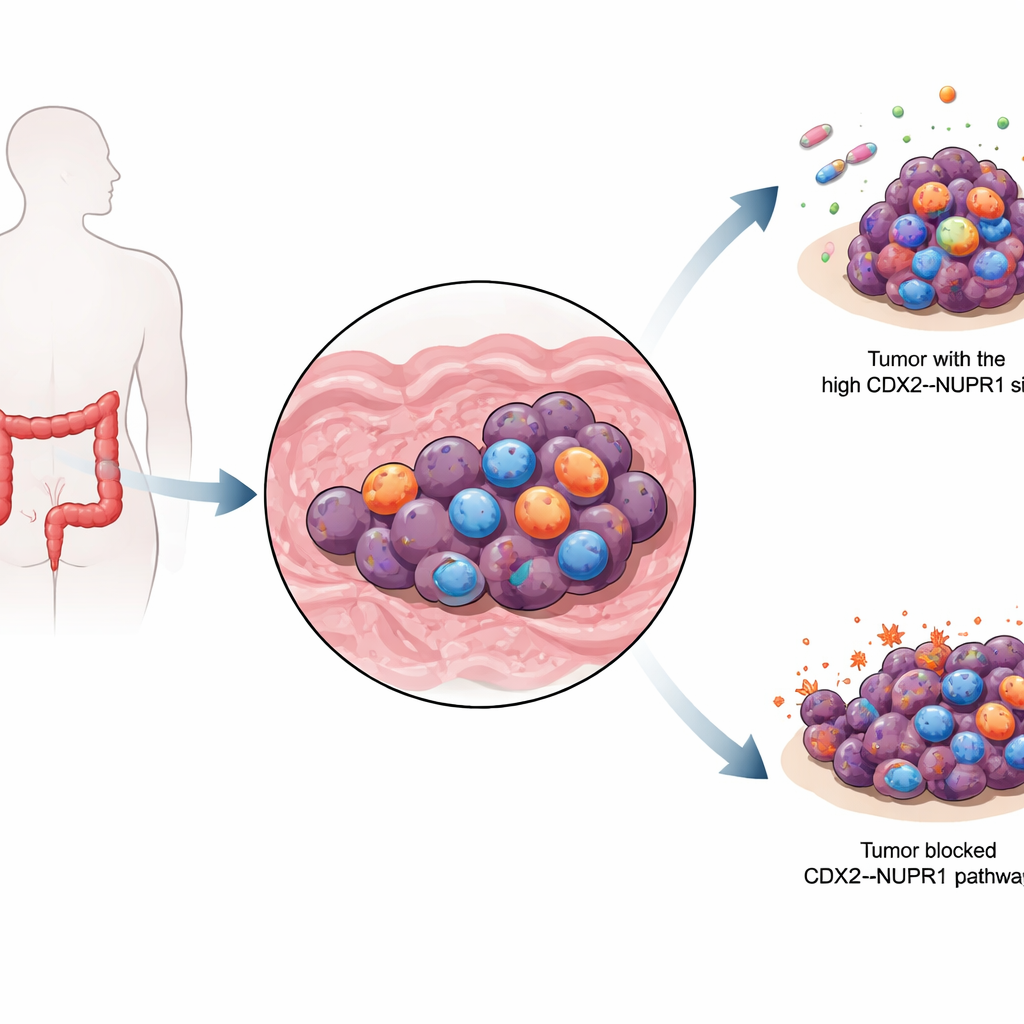
De ijzervluchtigheid van een kankercel
Kankercellen hebben een ongewoon grote honger naar ijzer, een metaal dat hun groei ondersteunt maar hen ook kan vernietigen als het zich te veel ophoopt. Wanneer ijzer reageert met vetten in celmembranen kan dat een type celdood activeren dat ferroptose wordt genoemd, dat verschilt van het beter bekende zelfmoordprogramma apoptose. Omdat veel medicijnresistente kankercellen nog steeds afhankelijk zijn van ijzer, zijn onderzoekers enthousiast over middelen die hen in ferroptose duwen. Maar tumoren kunnen afweermechanismen ontwikkelen tegen dit proces, waardoor zowel standaardchemotherapie als ferroptose‑inducerende middelen minder effectief zijn.
Het dubbele gezicht van CDX2 in colon‑tumoren
CDX2 is een eiwit dat normaal gesproken helpt de gezondheid en identiteit van de darmbekleding te behouden. Verlies van CDX2 in colon‑tumoren wordt vaak geassocieerd met agressiever ziekteverloop en slechtere overleving. Toch profiteren patiënten wier tumoren CDX2 behouden paradoxaal genoeg minder van chemotherapie. Om deze contradictie te doorgronden manipuleerden de auteurs CDX2 in meerdere menselijke colonkankercellijnen en in muismodellen. Ze vonden dat verhoging van CDX2 kankercellen moeilijker doodde met gangbare middelen zoals 5‑fluorouracil en oxaliplatin, terwijl verlaging van CDX2 het omgekeerde effect gaf: tumoren werden gevoeliger en krimpten meer onder behandeling.
Een stressrespons‑schakelaar die celdood blokkeert
Dieper gravend gebruikten de onderzoekers genexpressieanalyses en weefselmonsters van honderden patiënten om een ander eiwit te identificeren, NUPR1, dat sterk samenhing met CDX2‑niveaus in stadium II–III colonkankers. NUPR1 is een stressresponsfactor die cellen helpt omgaan met schade, inclusief oxidatieve stress. De onderzoekers toonden aan dat CDX2 direct bindt aan het regelgebied van het NUPR1‑gen en het activeert. Wanneer NUPR1‑niveaus stegen, stapelden kankercellen minder ijzer op, produceerden ze minder schadelijke zuurstofgebonden moleculen en toonden ze minder tekenen van lipide‑ en DNA‑schade — allemaal kenmerken van ferroptoseresistentie. Als NUPR1 werd verwijderd, kon CDX2 cellen niet langer tegen ferroptose beschermen; omgekeerd bracht herstel van NUPR1 in CDX2‑deficiënte cellen die resistentie terug.
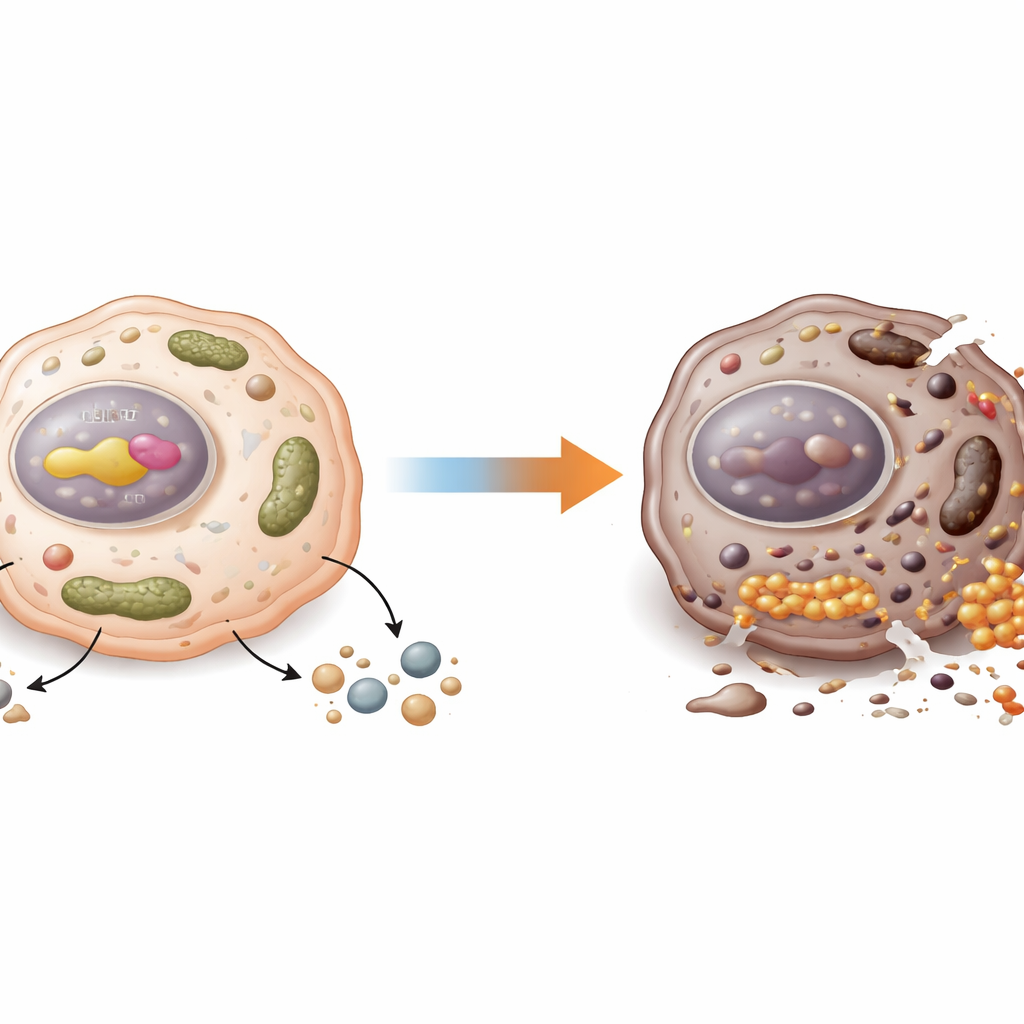
Het schild veranderen in een achilleshiel
Deze moleculaire inzichten werden vervolgens in muizen getest. Tumoren zonder CDX2 of NUPR1 reageerden veel beter op een ferroptose‑inducerend middel genaamd IKE, ze stapelden meer ijzer en lipideschade op en krimpten meer dan controletumoren. Het team gebruikte ook tumoren van patiënten (patiënt‑afgeleide xenografts) om echte klinische kankers na te bootsen. In tumoren met hoge CDX2‑ en NUPR1‑niveaus maakte toevoegen van een kleine‑molecuulremmer van NUPR1 (ZZW‑115) standaardchemotherapie met 5‑fluorouracil veel effectiever en versterkte het ferroptose‑achtige kenmerken in de kankercellen. In tumoren met lage CDX2‑ en NUPR1‑niveaus leverde diezelfde remmer weinig voordeel op, wat suggereert dat deze strategie het meest veelbelovend is voor een specifieke subgroep patiënten.
Wat dit kan betekenen voor toekomstige behandeling
Kort gezegd laat de studie zien dat veel CDX2‑positieve colonkankers zich verbergen achter een ingebouwd schild tegen ijzergedreven celdood, en dat dit schild grotendeels door NUPR1 wordt aangedreven. Door dit schild uit te schakelen — genetisch of met een middel als ZZW‑115 — kunnen artsen mogelijk kankercellen opnieuw blootstellen aan het dodelijke potentieel van zowel chemotherapie als ferroptose‑inducerende middelen. Hoewel er meer onderzoek bij mensen nodig is, suggereren de bevindingen dat het testen van tumoren op CDX2 en NUPR1 kan helpen die patiënten te identificeren die het meest waarschijnlijk profiteren van behandelingen die kankercellen doelbewust in ferroptose duwen in plaats van ze stilletjes resistent te laten worden en terug te laten keren.
Bronvermelding: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
Trefwoorden: dikkedarmkanker, CDX2, ferroptose, NUPR1, chemotherapie‑resistentie