Clear Sky Science · ru
CDX2 обеспечивает устойчивость к ферроптозу при раке толстой кишки стадии II–III за счёт повышения экспрессии NUPR1
Почему это важно для людей с раком толстой кишки
Многим пациентам с раком толстой кишки стадии II–III приходится выбирать между снижением риска рецидива и серьёзными побочными эффектами химиотерапии. Врачи заметили, что опухоли с высоким уровнем белка CDX2 часто ведут себя менее агрессивно, но при этом такие же опухоли хуже реагируют на химиотерапию. В этом исследовании объясняют, почему существует такой парадокс, и обнаруживают скрытый приём выживания, с помощью которого некоторые раковые клетки толстой кишки уклоняются от нового, связанного с железом типа гибели клеток.
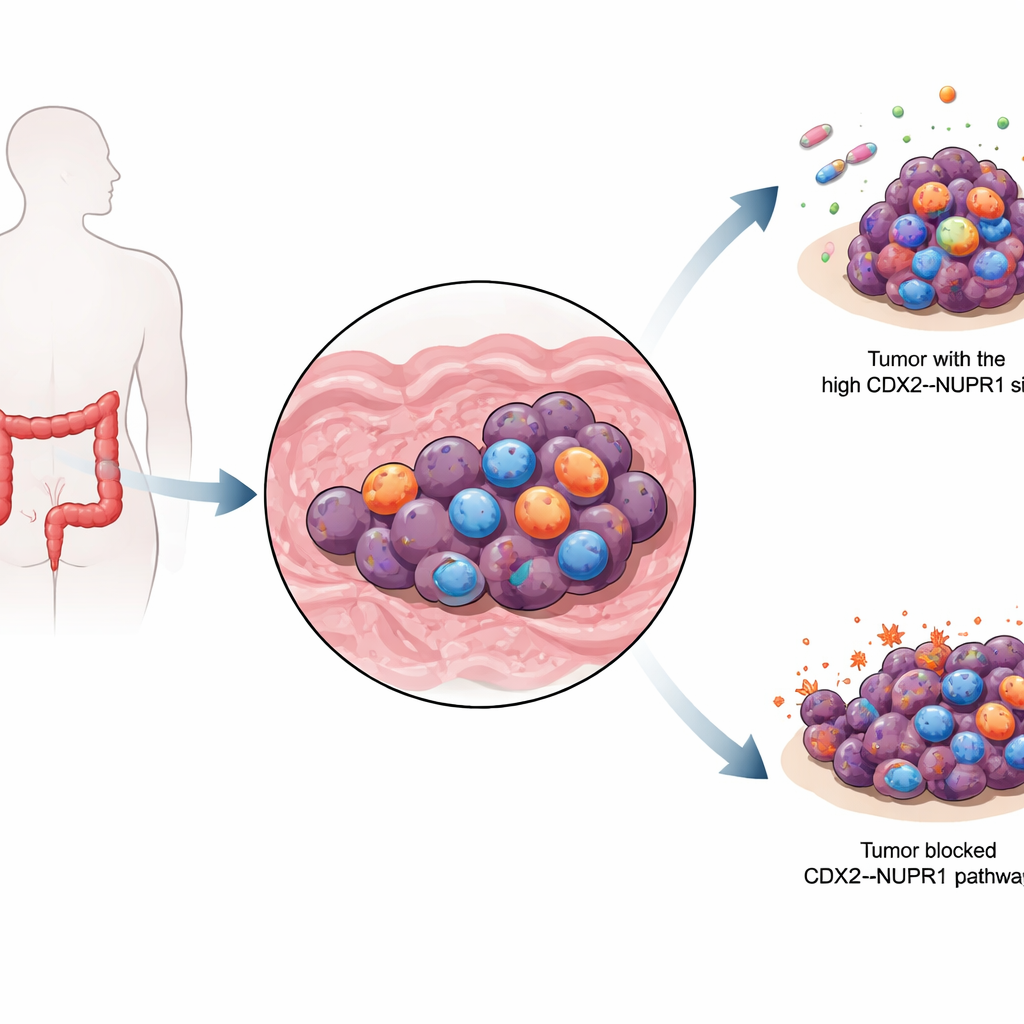
Железная уязвимость раковой клетки
Раковые клетки необычно нуждаются в железе — металле, который помогает им расти, но при избыточном накоплении может и убить их. Когда железо реагирует с жирами в мембранах клеток, это может запустить тип гибели клеток, известный как ферроптоз, отличающийся от более известной программы самоубийства — апоптоза. Поскольку многие лекарственно-устойчивые раковые клетки по‑прежнему зависят от железа, учёных воодушевляют препараты, которые заставляют их вступать в ферроптоз. Но опухоли могут выработать защиту против этого процесса, ослабляя эффект как стандартной химиотерапии, так и индуцирующих ферроптоз препаратов.
Двойная роль CDX2 в опухолях толстой кишки
CDX2 — это белок, который в норме поддерживает здоровье и идентичность клеток, выстилающих кишечник. Потеря CDX2 в опухолях толстой кишки часто связана с более агрессивным течением и худшим выживанием. Тем не менее, что интригует, пациенты с опухолями, сохраняющими CDX2, могут получать меньше пользы от химиотерапии. Чтобы разобраться в этом противоречии, авторы изменяли уровни CDX2 в нескольких линиях человеческих клеток рака толстой кишки и в мышиных моделях опухоли. Они обнаружили, что повышение CDX2 делает клетки труднееубиваемыми стандартными препаратами, такими как 5‑фторурацил и оксалиплатин, тогда как снижение CDX2 имело обратный эффект: опухоли становились более чувствительными и сильнее уменьшались при лечении.
Переключатель стресс‑ответа, блокирующий гибель клеток
Углубляясь, команда использовала анализы экспрессии генов и образцы тканей сотен пациентов, чтобы сосредоточиться на другом белке — NUPR1, который оказался тесно связан с уровнями CDX2 в раке толстой кишки стадий II–III. NUPR1 — это фактор ответной реакции на стресс, помогающий клеткам справляться с повреждениями, включая оксидативный стресс. Исследователи показали, что CDX2 напрямую связывается с регуляторной областью гена NUPR1 и включает его. При повышении NUPR1 раковые клетки накапливали меньше железа, производили меньше повреждающих молекул на основе кислорода и демонстрировали меньшие признаки повреждения липидов и ДНК — все признаки устойчивости к ферроптозу. Если NUPR1 удаляли, CDX2 больше не мог защищать клетки от ферроптоза; наоборот, восстановление NUPR1 в клетках с дефицитом CDX2 возвращало им устойчивость.
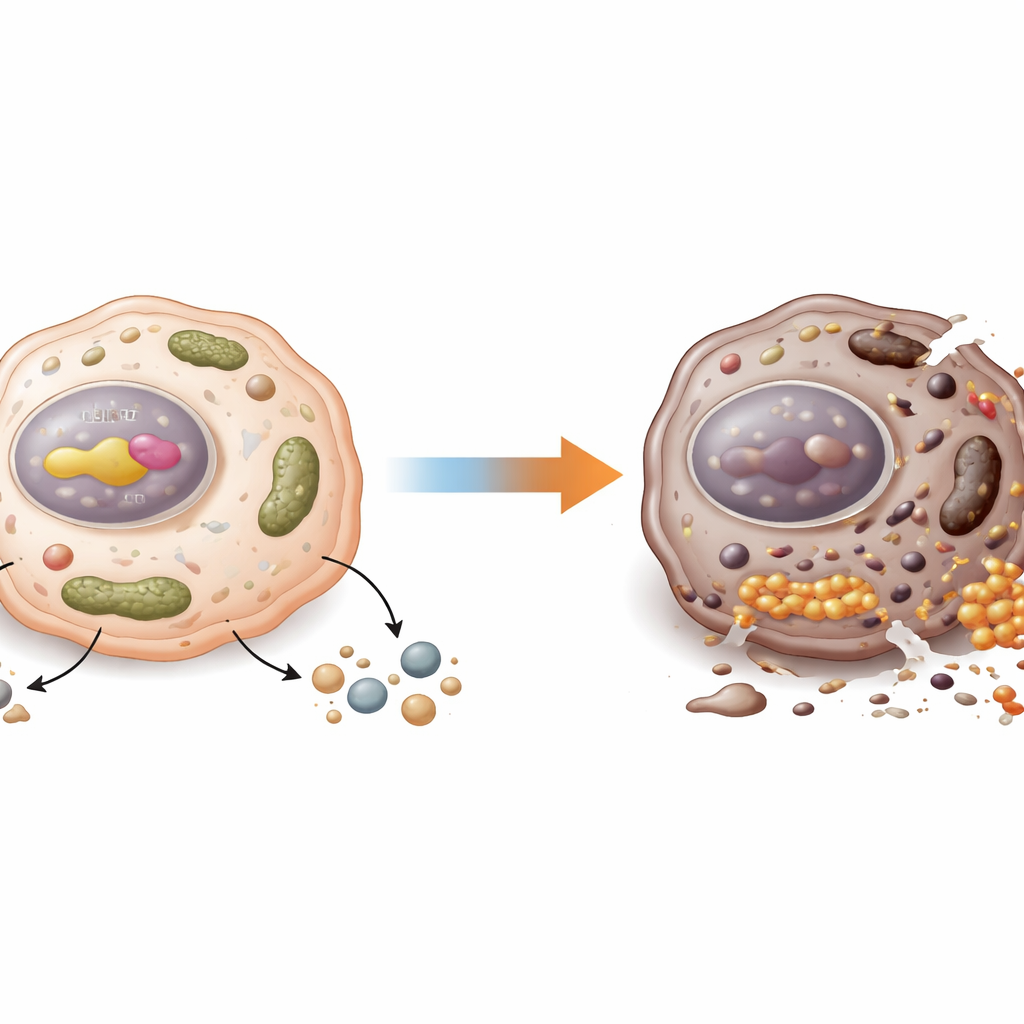
Как щит становится ахиллесовой пятой
Эти молекулярные выводы затем проверили на мышах. Опухоли без CDX2 или NUPR1 гораздо лучше реагировали на соединение, индуцирующее ферроптоз, называемое IKE: в них накапливалось больше железа и поражений липидов, и они сильнее уменьшались по сравнению с контрольными опухолями. Команда также использовала трансплантаты опухолей от пациентов, чтобы смоделировать реальные случаи рака толстой кишки. В опухолях с высоким CDX2 и NUPR1 добавление малой молекулы‑ингибитора NUPR1 (ZZW‑115) сделало стандартную химиотерапию 5‑фторурацилом значительно более эффективной и усилило признаки, схожие с ферроптозом, в самих раковых клетках. В опухолях с низкими уровнями CDX2 и NUPR1 тот же ингибитор давал мало эффекта, что указывает на то, что стратегия наиболее перспективна для определённой подгруппы пациентов.
Что это может означать для будущего лечения
Проще говоря, исследование показывает, что многие CDX2‑положительные опухоли толстой кишки укрываются за встроенным щитом против железо‑опосредованной гибели клеток, и этот щит во многом обеспечивается NUPR1. Выключив этот щит — генетически или с помощью препарата вроде ZZW‑115 — врачи, возможно, смогут вновь подвергнуть раковые клетки губительному воздействию как химиотерапии, так и ферроптоз‑индуцирующих агентов. Хотя требуется больше исследований на людях, результаты указывают на то, что тестирование опухолей на CDX2 и NUPR1 может помочь выявить тех пациентов, которые с наибольшей вероятностью получат пользу от методов лечения, намеренно доводящих раковые клетки до ферроптоза, вместо того чтобы позволять им молча сопротивляться и возвращаться.
Цитирование: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
Ключевые слова: рак толстой кишки, CDX2, ферроптоз, NUPR1, резистентность к химиотерапии