Clear Sky Science · pl
CDX2 nadaje oporność na ferroptoza w raku jelita grubego w stadium II–III poprzez zwiększenie ekspresji NUPR1
Dlaczego to ma znaczenie dla osób z rakiem jelita grubego
Wielu pacjentów ze stadiami II–III raka jelita grubego stoi przed trudnym wyborem: chemioterapia może zmniejszyć ryzyko nawrotu choroby, ale wiąże się też z poważnymi skutkami ubocznymi. Lekarze wiedzą, że guzy o wysokim poziomie białka CDX2 często zachowują się mniej agresywnie, a mimo to te same guzy zwykle gorzej reagują na chemioterapię. To badanie bada przyczynę tej zagadki i ujawnia ukrytą strategię przetrwania, której niektóre komórki raka jelita używają, by uchylić się przed nowym, żelazozależnym mechanizmem śmierci komórki.
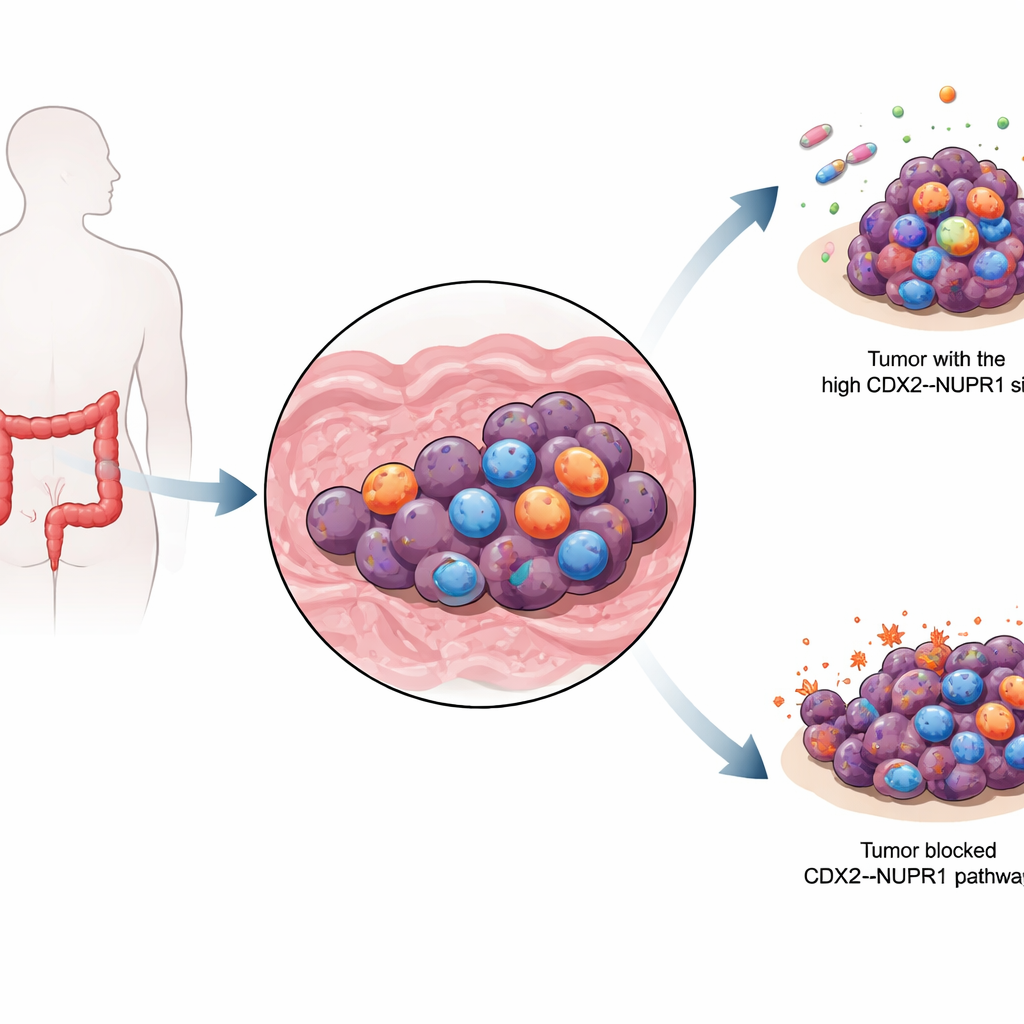
Żelazna słabość komórki nowotworowej
Komórki nowotworowe są wyjątkowo żądne żelaza — metalu, który wspiera ich wzrost, a jednocześnie może je zniszczyć, gdy nagromadzi się w nadmiarze. Kiedy żelazo reaguje z tłuszczami w błonach komórkowych, może wywołać rodzaj śmierci komórki znany jako ferroptoza, różny od lepiej poznanego programu samobójczego zwanego apoptozą. Ponieważ wiele komórek opornych na leki wciąż polega na żelazie, badacze z zainteresowaniem patrzą na leki, które wymuszają u nich ferroptozę. Jednak guzy mogą wykształcać mechanizmy obronne przeciwko temu procesowi, tłumiąc skuteczność zarówno standardowej chemioterapii, jak i leków indukujących ferroptozę.
Podwójne oblicze CDX2 w guzach jelita
CDX2 to białko, które normalnie pomaga utrzymać zdrowie i tożsamość komórek wyściełających jelito. Utrata CDX2 w guzach jelita często wiąże się z bardziej agresywną chorobą i gorszym przeżyciem. Paradoksalnie jednak pacjenci, których guzy zachowują CDX2, mogą czerpać mniejszą korzyść z chemioterapii. Aby zbadać tę sprzeczność, autorzy manipulowali poziomami CDX2 w kilku ludzkich liniach komórkowych raka jelita oraz w modelach mysi. Stwierdzili, że zwiększenie CDX2 utrudniało zabijanie komórek przez standardowe leki, takie jak 5‑fluorouracyl i oksaliplatyna, podczas gdy obniżenie CDX2 działało odwrotnie: guzy stawały się bardziej wrażliwe i bardziej się kurczyły pod wpływem terapii.
Przełącznik odpowiedzi na stres blokujący śmierć komórki
Bliższe badania z użyciem analiz ekspresji genów i próbek tkanek od setek pacjentów skierowały uwagę na inne białko, NUPR1, które ściśle korelowało z poziomami CDX2 w raku jelita w stadium II–III. NUPR1 jest czynnikiem odpowiedzi na stres, pomagającym komórkom radzić sobie z uszkodzeniami, w tym ze stresem oksydacyjnym. Badacze pokazali, że CDX2 bezpośrednio wiąże się z regionem kontrolnym genu NUPR1 i go uruchamia. Kiedy poziomy NUPR1 rosły, komórki nowotworowe gromadziły mniej żelaza, produkowały mniej szkodliwych rodników tlenowych i wykazywały niższe oznaki uszkodzeń lipidów i DNA — wszystkie cechy wskazujące na oporność na ferroptozę. Jeśli NUPR1 został usunięty, CDX2 nie mogło już chronić komórek przed ferroptozą; odwrotnie, przywrócenie NUPR1 w komórkach pozbawionych CDX2 odtwarzało ich oporność.
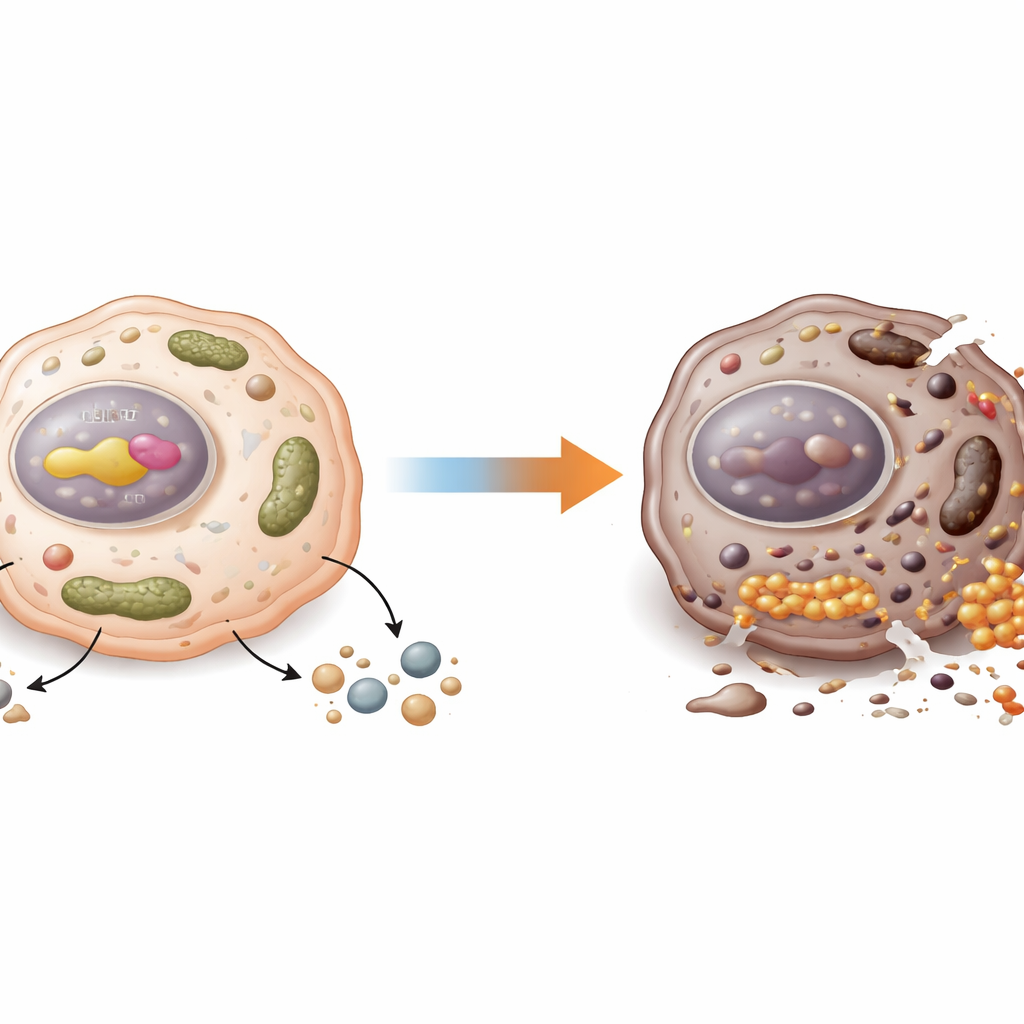
Przekształcenie tarczy w piętę Achillesa
Te molekularne obserwacje sprawdzono następnie na myszach. Guzy pozbawione CDX2 lub NUPR1 reagowały znacznie lepiej na związek indukujący ferroptozę o nazwie IKE, gromadząc więcej żelaza i uszkodzeń lipidów oraz kurcząc się bardziej niż guzy kontrolne. Zespół użył też przeszczepów guzów pochodzących od pacjentów, by naśladować rzeczywiste przypadki raka jelita. W guzach z wysokim CDX2 i NUPR1 dodanie małocząsteczkowego inhibitora NUPR1 (ZZW‑115) znacznie zwiększyło skuteczność standardowej chemioterapii z 5‑fluorouracylem i nasiliło cechy podobne do ferroptozy w komórkach nowotworowych. W guzach z niskim CDX2 i NUPR1 ten sam inhibitor przyniósł niewielką korzyść, co sugeruje, że strategia ta ma największy potencjał w konkretnej podgrupie pacjentów.
Co to może znaczyć dla przyszłego leczenia
Mówiąc krótko, badanie pokazuje, że wiele nowotworów jelita z pozytywną ekspresją CDX2 ukrywa się za wbudowaną tarczą przeciwko żelazozależnej śmierci komórki, a tarcza ta jest w dużej mierze napędzana przez NUPR1. Wyłączenie tej tarczy — genetycznie lub za pomocą leku takiego jak ZZW‑115 — może pozwolić lekarzom ponownie wystawić komórki nowotworowe na zabójczy potencjał zarówno chemioterapii, jak i czynników indukujących ferroptozę. Chociaż potrzeba więcej badań klinicznych, wyniki sugerują, że badanie guzów pod kątem CDX2 i NUPR1 mogłoby pomóc zidentyfikować pacjentów, którzy najwięcej zyskają na terapiach celowo prowokujących ferroptozę, zamiast pozwalać komórkom cicho opierać się i nawracać.
Cytowanie: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
Słowa kluczowe: rak jelita grubego, CDX2, ferroptoza, NUPR1, oporność na chemioterapię