Clear Sky Science · de
CDX2 verleiht Stadien‑II‑III‑Kolonkarzinomen Ferroptose‑Resistenz über die Hochregulierung von NUPR1
Warum das für Menschen mit Darmkrebs wichtig ist
Viele Patientinnen und Patienten mit Stadium‑II–III‑Kolonkarzinom stehen vor einem schwierigen Abwägungsproblem: Chemotherapie kann das Rückfallrisiko verringern, bringt aber auch erhebliche Nebenwirkungen mit sich. Ärzte wissen, dass Tumoren mit hohen Mengen des Proteins CDX2 oft weniger aggressiv verlaufen, doch gerade diese Tumoren sprechen tendenziell schlechter auf Chemotherapie an. Diese Studie untersucht, warum dieses Paradoxon besteht, und deckt einen verborgenen Überlebensmechanismus auf, den manche Darmkrebszellen nutzen, um einer neueren, eisen‑verknüpften Form des Zelltods zu entgehen.
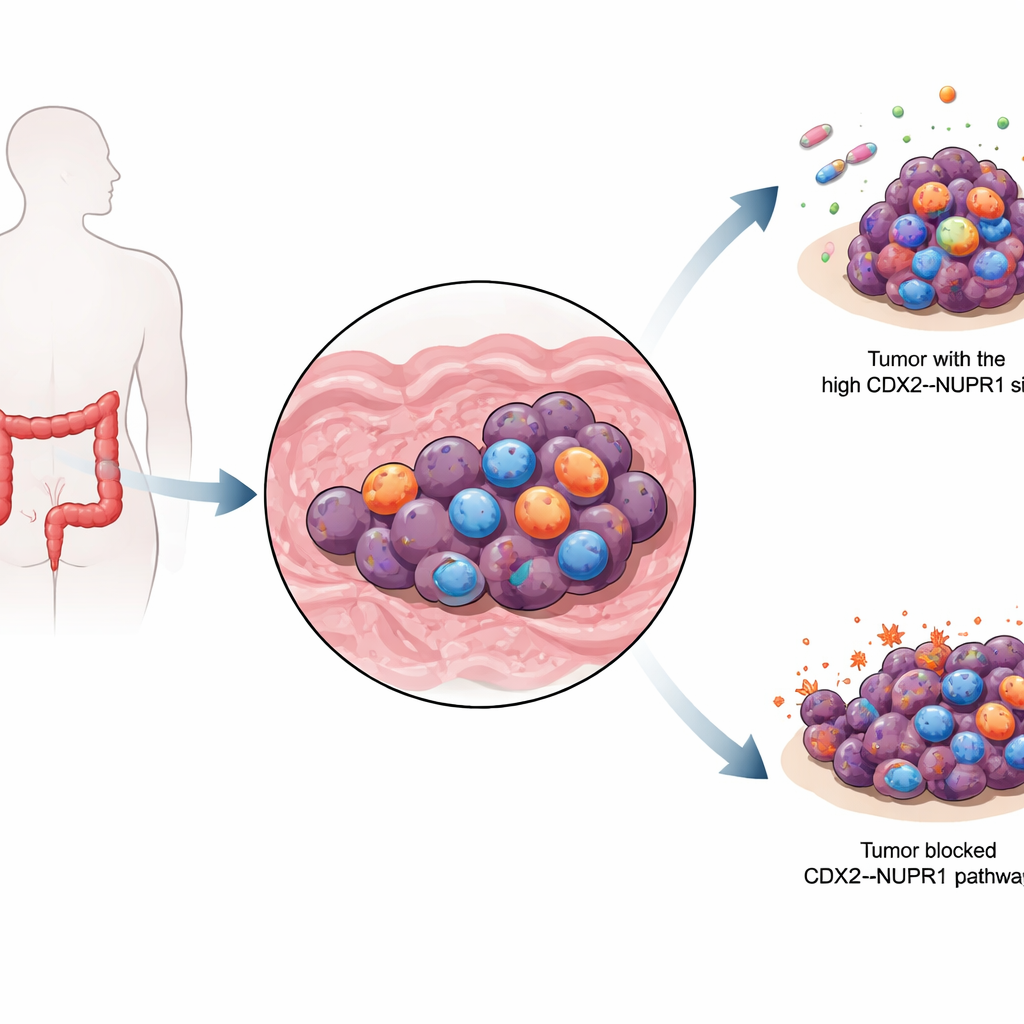
Die Eisen‑Schwachstelle einer Krebszelle
Krebszellen sind ungewöhnlich eisenhungrig: Das Metall hilft ihrem Wachstum, kann sich aber bei Überladung auch destruktiv auswirken. Wenn Eisen mit Fetten in Zellmembranen reagiert, kann es eine Form des Zelltods auslösen, die als Ferroptose bekannt ist und sich von dem besser bekannten Selbstmordprogramm Apoptose unterscheidet. Weil viele medikamentenresistente Krebszellen weiterhin auf Eisen angewiesen sind, wecken Wirkstoffe, die sie in die Ferroptose treiben, großes Interesse. Tumoren können jedoch Abwehrmechanismen gegen diesen Prozess entwickeln, was sowohl die Wirkung der Standardchemotherapie als auch von Ferroptose‑induzierenden Wirkstoffen abschwächt.
Das doppelte Gesicht von CDX2 in Kolontumoren
CDX2 ist ein Protein, das normalerweise die Gesundheit und Identität der Zellen der Darmschleimhaut erhält. Der Verlust von CDX2 in Kolontumoren wird oft mit aggressiverem Krankheitsverlauf und schlechterer Überlebensrate assoziiert. Rätselhaft ist jedoch, dass Patienten mit CDX2‑erhaltenden Tumoren weniger von einer Chemotherapie zu profitieren scheinen. Um diesem Widerspruch nachzugehen, manipulierten die Autorinnen und Autoren CDX2 in mehreren menschlichen Kolonkarzinom‑Zelllinien und in Maus‑Tumormodellen. Sie fanden heraus, dass eine Erhöhung von CDX2 Krebszellen weniger anfällig für gängige Wirkstoffe wie 5‑Fluorouracil und Oxaliplatin machte, während eine Reduktion von CDX2 den entgegengesetzten Effekt hatte: Tumoren wurden empfindlicher und schrumpften unter Behandlung stärker.
Ein Stressantwort‑Schalter, der den Zelltod blockiert
Bei genaueren Untersuchungen nutzte das Team Genexpressionsanalysen und Gewebeproben von Hunderten Patienten, um ein weiteres Protein zu identifizieren: NUPR1, das in Stadien‑II–III‑Kolonkarzinomen eng mit CDX2‑Spiegeln korrelierte. NUPR1 ist ein Stressantwortfaktor, der Zellen hilft, mit Schäden umzugehen, einschließlich oxidativem Stress. Die Forschenden zeigten, dass CDX2 direkt an die Kontrollregion des NUPR1‑Gens bindet und dessen Expression aktiviert. Mit steigenden NUPR1‑Spiegeln akkumulierten Krebszellen weniger Eisen, produzierten weniger schädliche sauerstoffbasierte Moleküle und wiesen geringere Anzeichen von Lipid‑ und DNA‑Schädigungen auf — alles Kennzeichen einer Ferroptose‑Resistenz. Wurde NUPR1 entfernt, konnte CDX2 die Zellen nicht mehr vor Ferroptose schützen; umgekehrt stellte die Wiederherstellung von NUPR1 in CDX2‑defizienten Zellen deren Resistenz wieder her.
Den Schild zum Achillesferse machen
Diese molekularen Erkenntnisse wurden anschließend in Mäusen getestet. Tumoren ohne CDX2 oder NUPR1 sprachen deutlich besser auf eine Ferroptose‑induzierende Verbindung namens IKE an: Sie akkumulierten mehr Eisen und Lipidschäden und schrumpften stärker als Kontrolltumoren. Das Team verwendete außerdem tumorgenommene Patiententransplantate, um reale Kolonkarzinome zu simulieren. In Tumoren mit hohem CDX2‑ und NUPR1‑Gehalt machte die Zugabe eines kleinen Molekülinhibitors von NUPR1 (ZZW‑115) die Standardchemotherapie mit 5‑Fluorouracil deutlich wirksamer und verstärkte Ferroptose‑ähnliche Merkmale in den Krebszellen. In Tumoren mit niedrigem CDX2‑ und NUPR1‑Spiegel brachte derselbe Inhibitor kaum zusätzlichen Nutzen, was darauf hindeutet, dass diese Strategie besonders vielversprechend für eine bestimmte Untergruppe von Patientinnen und Patienten ist.
Was das für künftige Behandlungen bedeuten könnte
Kurz gesagt zeigt die Studie, dass viele CDX2‑positive Kolonkarzinome sich hinter einem eingebauten Schild gegen eisengetriebenen Zelltod verstecken, und dass dieser Schild weitgehend von NUPR1 betrieben wird. Schaltet man diesen Schild aus — genetisch oder mit einem Wirkstoff wie ZZW‑115 —, könnten Ärztinnen und Ärzte Krebszellen erneut der tödlichen Wirkung sowohl der Chemotherapie als auch von Ferroptose‑induzierenden Agenzien aussetzen. Zwar sind weitere Studien am Menschen nötig, doch legen die Ergebnisse nahe, dass die Bestimmung von CDX2 und NUPR1 in Tumoren helfen könnte, jene Patientinnen und Patienten zu identifizieren, die am ehesten von Behandlungen profitieren, die Krebszellen gezielt in die Ferroptose treiben, anstatt sie stillschweigend widerstandsfähig werden und zurückkehren zu lassen.
Zitation: Yu, J., Mu, M., Zhao, C. et al. CDX2 confers ferroptosis resistance in stage II-III colon cancer via upregulation of NUPR1. Cell Death Dis 17, 308 (2026). https://doi.org/10.1038/s41419-026-08412-x
Schlüsselwörter: Darmkrebs, CDX2, Ferroptose, NUPR1, Chemotherapie‑Resistenz