Clear Sky Science · zh
间充质干细胞移植加间歇性θ爆刺激后,慢性中风猕猴出现强劲神经发生
为长期中风幸存者带来新希望
许多中风幸存者会在臂或腿上留下持续性无力,在最初几个月之后恢复常常停滞不前。这项在猴子身上的研究探索了一种新颖的两步治疗方法,旨在“唤醒”大脑自我修复的能力,即便在中风发生多年后也能起效。通过将移植的干细胞与对颅骨施加的温和磁脉冲相结合,研究者表明一个看似稳定且受损的大脑可以再次产生新的神经细胞并重建有助于运动的连接。
为何慢性中风难以治疗
中风会切断脑部局部的血供,导致神经细胞死亡,并在控制运动、语言或其他功能的区域留下瘢痕。标准康复在前六个月效果最佳,此时大脑的可塑性天然最高。之后患者进入慢性阶段,改善显著放缓,许多人因此残留永久性功能缺损。现有工具如磁刺激可以带来有限益处,但其效果往往会减弱。来自骨髓或脐带等组织的干细胞在平抑炎症和支持幸存神经元方面显示出潜力,但它们很少能长期扎根或完全恢复功能。本研究检验了这两种方法合用是否会比单独使用更为有效。
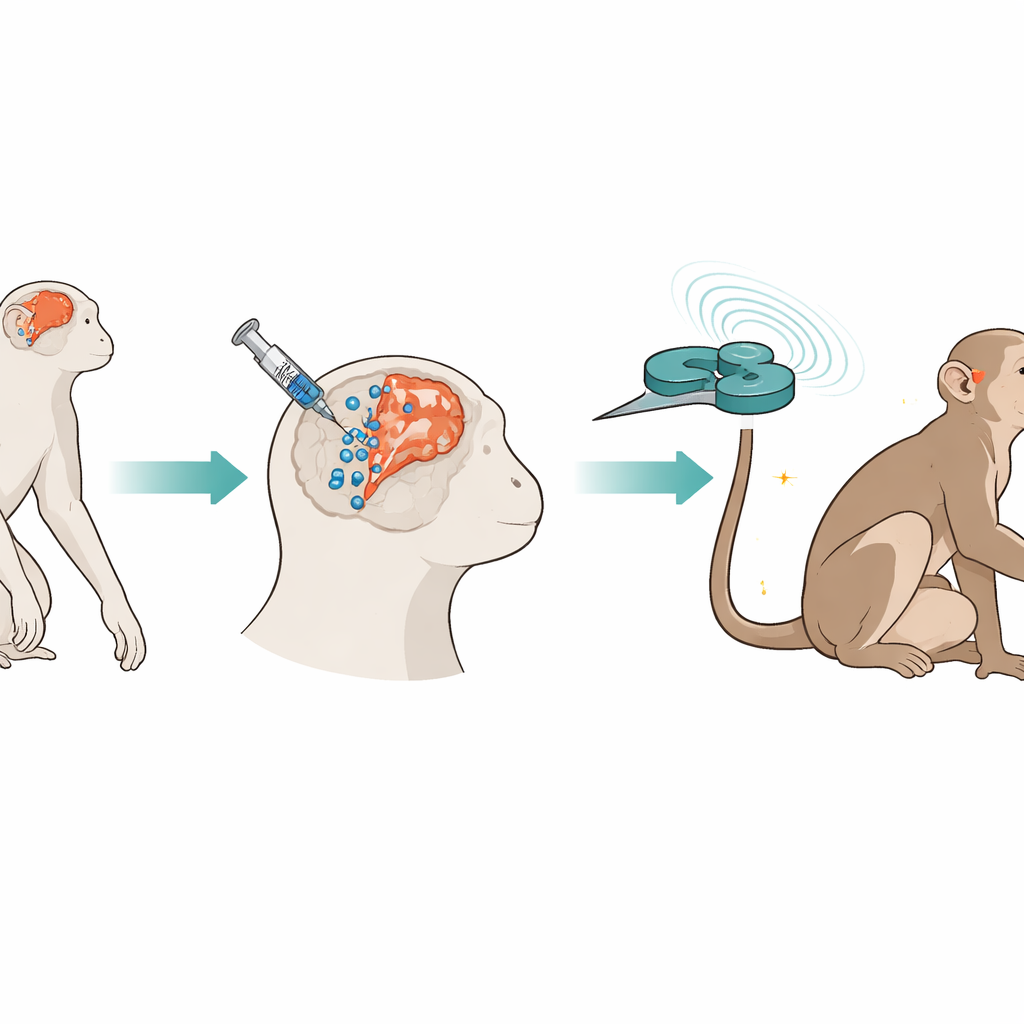
构建两步修复策略
研究者使用了食蟹猴(猕猴的一种),其大脑和中风反应类似于人类。在有意阻断脑动脉造成长期中风两年后,他们通过立体定向注射将来源于人体脐带的间充质干细胞注入损伤区周围的多个位点以及一条邻近的富含干细胞的区域。为便于随时间追踪,细胞被标记上微小铁颗粒和荧光标签,可通过磁共振成像和显微镜观察。一周后,团队开始施加间歇性θ爆刺激,这是一种通过八字线圈置于受损运动皮层上方发出的快速磁脉冲模式。该刺激每周五天,持续17周,同时对动物的运动、脑活动和血液化学进行监测。
更强的运动能力与更健康的脑信号
在治疗前,猴子受影响的前肢在如攀登小阶梯取食或从复杂的盒子中拉出零食等任务上已达到表现平台期。联合治疗后,它们的分数有所提高:成功率上升,完成时间缩短,以前无力的肢体被更频繁地使用。电生理检测显示,从受损脑侧触发肌肉反应所需的刺激更少,沿运动通路的信号传导更快,暗示接线有所修复。脑成像也呼应了这些变化。功能性磁共振显示受损的运动皮层变得更为活跃并与邻近区域更好地同步,运动相关区域之间的交流强度增强。扩散成像显示携带信号的白质“电缆”变得更有序,而磁共振波谱显示的脑化学物质变化则与神经元更健康、膜修复更好及能量利用改善相一致。
唤醒大脑自身的干细胞
研究结束时,移植的干细胞仍然存在于中风部位附近,证实了其异常持久的存活。对血液和脑组织的详尽蛋白质分析显示,治疗提升了与神经生长、突触形成和炎症减少相关的分子,同时显著激活了与神经发生——新神经元产生——和趋化性(细胞引导移动)相关的通路。在受伤半球,团队发现大量携带神经干细胞标志的细胞,而在未受伤半球这些细胞大多缺乏,并且出现了处于早期阶段、开始呈现神经特征的神经元。一个关键角色似乎是趋化因子CXCL12,这是一种由移植干细胞产生的信号分子。其受体存在于大脑自身的干细胞上,体外实验显示磁刺激促使干细胞分泌更多CXCL12及其他引导因子。这提示一种连锁反应:磁脉冲促使移植细胞释放更强的“化学信标”,把来自附近龛室的本地干细胞吸引到受损区域,在那里它们开始转变为新的神经元。
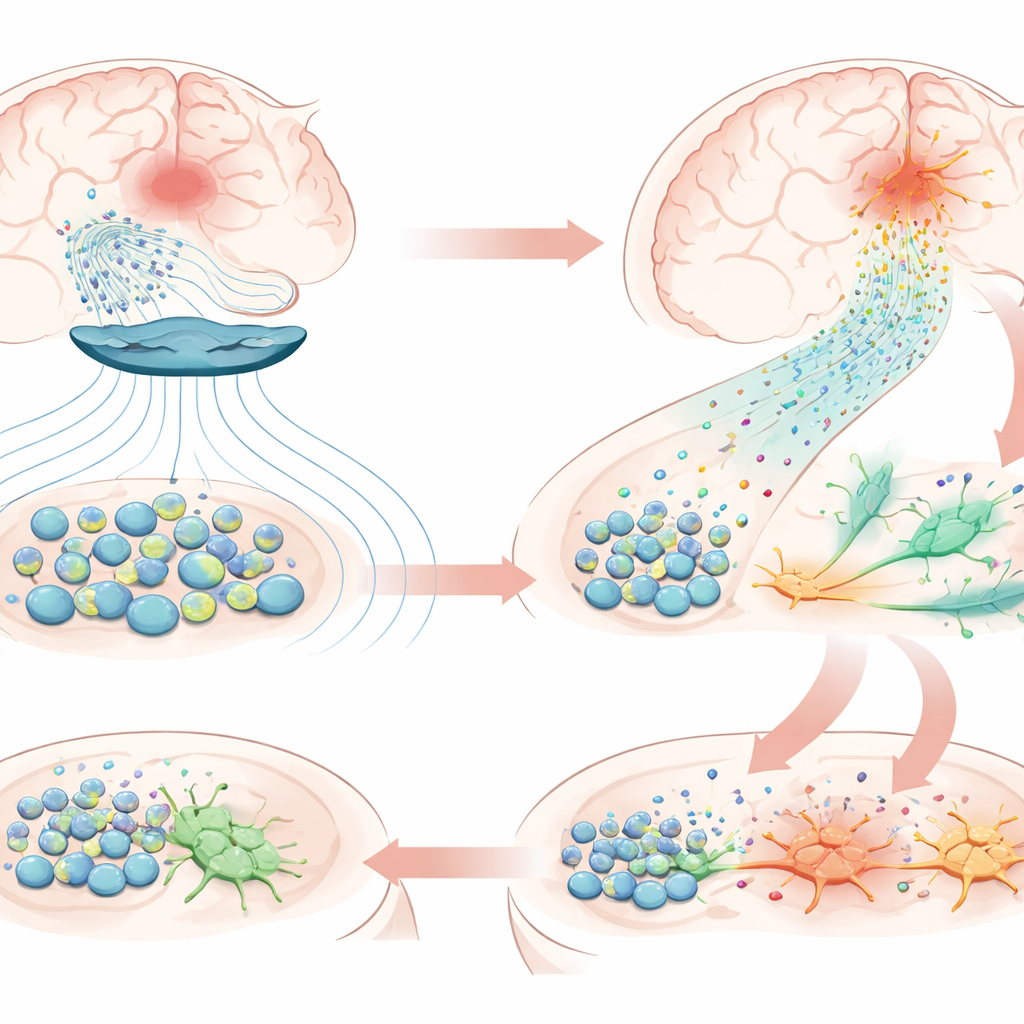
这对未来患者可能意味着什么
对于忍受长期中风致残的人来说,这项工作提供了一个谨慎乐观的信息:即便是慢性损伤的大脑也可能并非无可挽回。在猴子身上,干细胞移植与模式化磁刺激的组合不仅微调了现有回路——它似乎重启了大脑自身的新神经元“工厂”,并引导这些新神经元重建受损区域,伴随可测量的运动改善。尽管在将这一策略广泛应用于人之前还需要更大规模的研究、严格的安全性检测以及更少侵入性的细胞输送方法,但这项研究勾勒出一条清晰的路线图:通过将提供生长信号的生物疗法与重塑活动模式的物理疗法配对,有可能将中风恢复的时间窗口延长到以往认为固定的范围之外。
引用: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
关键词: 慢性中风, 干细胞疗法, 脑刺激, 神经发生, 非人灵长类