Clear Sky Science · de
Robuste Neurogenese bei chronischen Schlaganfall-Affen nach Transplantation mesenchymaler Stammzellen plus intermittierender Theta-Burst-Stimulation
Neue Hoffnung für Langzeit-Schlaganfallüberlebende
Viele Menschen, die einen Schlaganfall überleben, behalten eine dauerhafte Schwäche in Arm oder Bein, und nach den ersten Monaten stagniert die Erholung häufig. Diese Studie an Affen untersucht eine erfinderische zweiteilige Behandlung, die darauf abzielt, die Fähigkeit des Gehirns zur Selbstreparatur wieder „aufzuwecken“, selbst Jahre nach einem Schlaganfall. Durch die Kombination transplantierter Stammzellen mit sanften Magnetimpulsen auf den Schädel zeigen die Forschenden, dass ein scheinbar stabil geschädigtes Gehirn erneut neue Nervenzellen bilden und Verbindungen wiederaufbauen kann, die die Bewegung verbessern.
Warum chronische Schlaganfälle so schwer zu behandeln sind
Ein Schlaganfall unterbricht die Blutversorgung von Hirnarealen, tötet Nervenzellen ab und hinterlässt eine vernarbte Region, die Bewegung, Sprache oder andere Funktionen steuert. Standardrehabilitation wirkt am besten in den ersten sechs Monaten, wenn das Gehirn von Natur aus am flexibelsten ist. Danach treten Patientinnen und Patienten in eine chronische Phase ein, in der Verbesserungen stark verlangsamen und viele mit bleibenden Einschränkungen zurückbleiben. Bestehende Werkzeuge wie die magnetische Hirnstimulation können mäßige Vorteile bringen, doch ihre Effekte neigen dazu, zu verblassen. Stammzellen, gewonnen aus Geweben wie Knochenmark oder Nabelschnur, haben vielversprechende Effekte bei der Beruhigung von Entzündungen und der Unterstützung überlebender Neuronen gezeigt, doch sie heften sich selten dauerhaft an oder stellen die Funktion vollständig wieder her. Diese Arbeit prüft, ob diese beiden Ansätze zusammen stärker wirken könnten als einzeln.
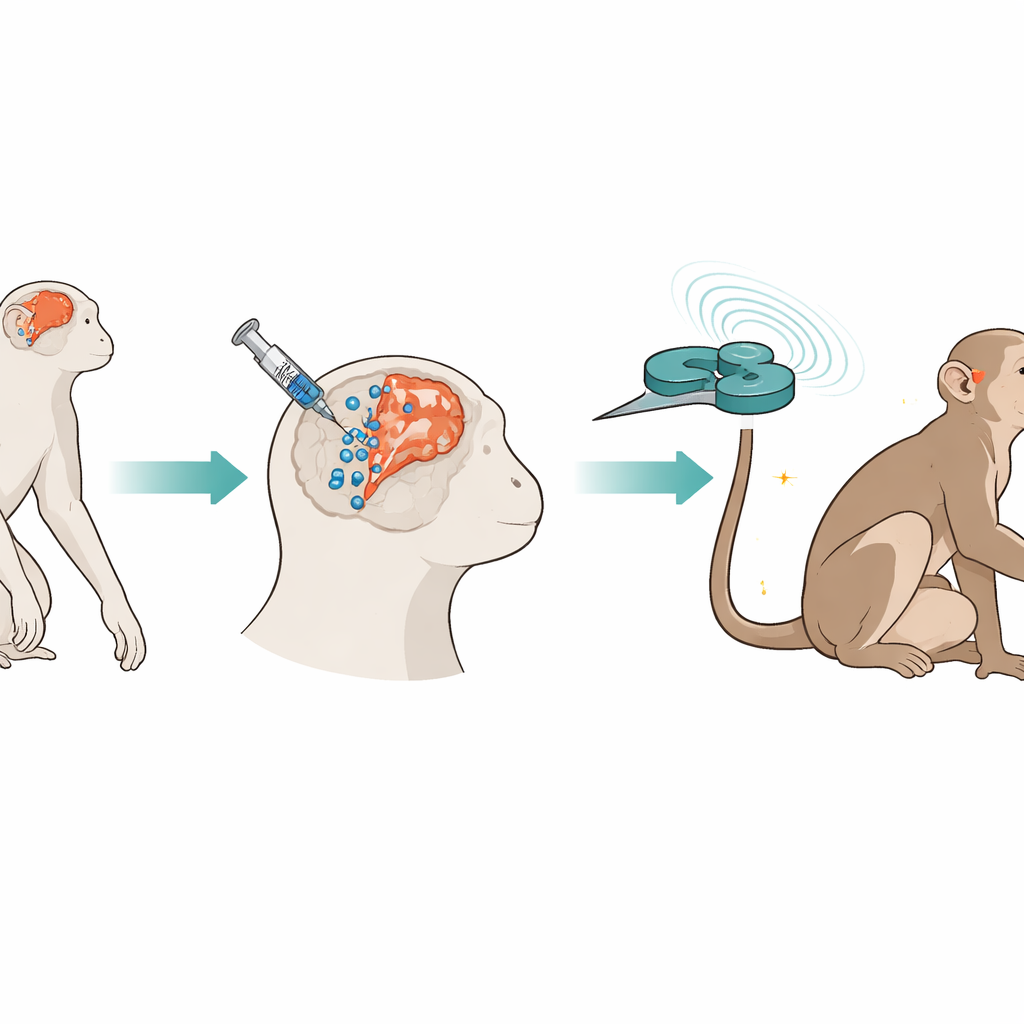
Aufbau einer zweistufigen Reparaturstrategie
Die Forschenden verwendeten Zynomolgusaffen, deren Gehirne und Schlaganfallreaktionen denen des Menschen ähneln. Zwei Jahre nachdem eine Hirnarterie absichtlich blockiert wurde, um einen langanhaltenden Schlaganfall zu erzeugen, injizierten sie stereotaktisch mesenchymale Stammzellen aus humaner Nabelschnur an mehreren Stellen rund um den beschädigten Bereich und entlang einer nahegelegenen, stammzellreichen Zone. Die Zellen wurden mit winzigen Eisenpartikeln und fluoreszenten Markern gekennzeichnet, damit sie über die Zeit per MRT und unter dem Mikroskop verfolgt werden konnten. Eine Woche später begann das Team mit intermittierender Theta-Burst-Stimulation, einem schnellen Muster magnetischer Impulse, das über eine Acht-Spulen-Anordnung über dem verletzten motorischen Kortex abgegeben wurde. Diese Stimulation erfolgte fünf Tage die Woche über 17 Wochen, während die Bewegung, die Gehirnaktivität und die Blutchemie der Tiere überwacht wurden.
Stärkere Bewegungen und gesündere Hirnsignale
Vor der Behandlung hatten die betroffenen Arme der Affen auf Aufgaben wie dem Hinaufklettern kleiner Treppen, um Futter zu holen, oder dem Herausziehen von Leckereien aus einer kniffligen Box ein Leistungspflaster erreicht. Nach der kombinierten Therapie verbesserten sich ihre Werte: die Erfolgsraten stiegen, die Abschlusszeiten sanken und die zuvor geschwächten Gliedmaßen wurden häufiger eingesetzt. Elektrische Tests zeigten, dass weniger Stimulation nötig war, um Muskelantworten von der verletzten Seite des Gehirns auszulösen, und Signale reisten schneller entlang motorischer Bahnen, was auf reparierte Verschaltungen hindeutet. Gehirnscans spiegelten diese Veränderungen wider. Funktionelle MRT zeigte, dass der geschädigte motorische Kortex aktiver wurde und besser mit benachbarten Regionen synchronisierte, während die Stärke der Kommunikation zwischen bewegungsrelevanten Bereichen zunahm. Diffusionsbildgebung deutete darauf hin, dass die weißen „Kabel“ für Signalübertragung geordneter wurden, und die Magnetresonanzspektroskopie zeigte Veränderungen in Gehirnchemikalien, die mit gesünderen Neuronen, besserer Membranreparatur und effizienterer Energieverwendung übereinstimmen.
Das Aufwecken der eigenen Stammzellen des Gehirns
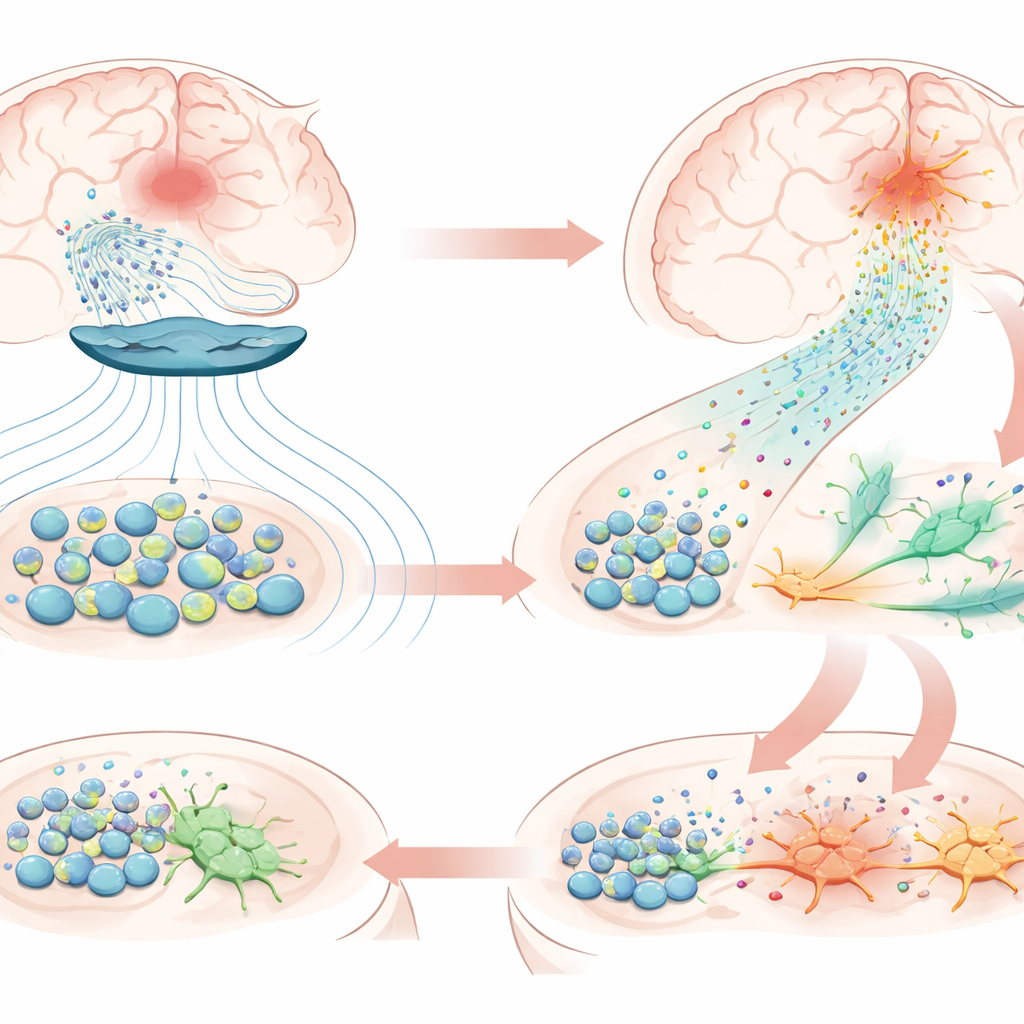
Am Ende der Studie waren die transplantierten Stammzellen noch in der Nähe der Schlaganfallstelle vorhanden, was eine ungewöhnlich lange Überlebensdauer bestätigte. Detaillierte Proteinanalysen von Blut und Hirngewebe zeigten, dass die Behandlung Moleküle erhöhte, die mit Nervenwachstum, Synapsenbildung und verminderter Entzündung verbunden sind, und zudem deutlich Signalwege aktivierte, die mit Neurogenese—der Entstehung neuer Neuronen—und Chemotaxis, der gerichteten Zellbewegung, verknüpft sind. In der verletzten Hemisphäre fand das Team reichlich Zellen mit Markern neuraler Stammzellen, die auf der unverletzten Seite weitgehend fehlten, sowie frühe Neuronen, die begannen, nervenähnliche Eigenschaften auszubilden. Ein Schlüsselspieler schien die Chemokin CXCL12 zu sein, ein Signalmolekül, das von den transplantierten Stammzellen produziert wurde. Seine Rezeptoren waren auf den eigenen Stammzellen des Gehirns vorhanden, und Laborexperimente zeigten, dass die magnetische Stimulation dazu führte, dass Stammzellen mehr CXCL12 und andere leitende Faktoren sezernierten. Das legt eine Kettenreaktion nahe: Magnetimpulse veranlassen transplantierte Zellen, stärkere „chemische Leuchtfeuer“ freizusetzen, die residente Stammzellen aus nahegelegenen Nischen in die beschädigte Zone locken, wo sie beginnen, sich in neue Neuronen zu verwandeln.
Was das für künftige Patientinnen und Patienten bedeuten könnte
Für Menschen mit langanhaltenden Schlaganfallbehinderungen liefert diese Arbeit eine vorsichtig optimistische Botschaft: Auch ein chronisch verletztes Gehirn muss nicht jenseits einer Reparatur liegen. Bei Affen tat die Kombination aus Stammzelltransplantaten und gemusterter Magnetstimulation mehr, als nur bestehende Schaltkreise feinzujustieren—sie schien die eigene Fabrik des Gehirns für neue Nervenzellen neu zu starten und diese beim Wiederaufbau beschädigter Bereiche zu leiten, mit messbaren Verbesserungen der Bewegung. Während größere Studien, sorgfältige Sicherheitstests und weniger invasive Methoden zur Zellapplikation notwendig sind, bevor diese Strategie breit am Menschen erprobt werden kann, bietet die Studie eine klare Blaupause. Indem eine biologische Therapie, die Wachstumssignale liefert, mit einer physikalischen Therapie gepaart wird, die Aktivitätsmuster umgestaltet, könnte es möglich sein, das Zeitfenster der Schlaganfallrecovery weit über das hinaus zu erweitern, was bisher als fest galt.
Zitation: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
Schlüsselwörter: chronischer Schlaganfall, Stammzelltherapie, Gehirnstimulation, Neurogenese, nichtmenschlicher Primat