Clear Sky Science · pl
Silna neurogeneza u małp z przewlekłym udarem po przeszczepie komórek macierzystych mezenchymalnych i przerywanej stymulacji theta-burst
Nowa nadzieja dla długoterminowych osób po udarze
Wiele osób, które przeżyły udar, pozostaje z trwałym osłabieniem ramienia lub nogi, a po pierwszych kilku miesiącach ich poprawa często ustaje. To badanie na małpach bada pomysłowe dwuczęściowe leczenie mające na celu „obudzenie” zdolności mózgu do samonaprawy, nawet wiele lat po udarze. Łącząc przeszczepione komórki macierzyste z delikatnymi impulsami magnetycznymi przykładającymi się do czaszki, badacze pokazują, że pozornie ustabilizowany, uszkodzony mózg może ponownie wytwarzać nowe komórki nerwowe i odbudowywać połączenia prowadzące do poprawy ruchu.
Dlaczego przewlekły udar jest tak trudny w leczeniu
Udar odcina dopływ krwi do części mózgu, powodując obumieranie komórek nerwowych i pozostawiając postarzały obszar odpowiedzialny za ruch, mowę lub inne funkcje. Standardowa rehabilitacja działa najlepiej w pierwszych sześciu miesiącach, gdy mózg jest naturalnie najbardziej plastyczny. Potem pacjenci wchodzą w fazę przewlekłą, w której poprawy spowalniają znacząco, pozostawiając wielu z trwałą niepełnosprawnością. Obecne narzędzia, takie jak magnetyczna stymulacja mózgu, mogą przynosić umiarkowane korzyści, ale ich efekty mają tendencję do wygasania. Komórki macierzyste pochodzące z tkanek, takich jak szpik kostny czy pępowina, wykazały obiecujące działanie w łagodzeniu zapalenia i wspieraniu ocalałych neuronów, lecz rzadko się na trwałe przyjmują lub w pełni przywracają funkcję. Niniejsza praca sprawdza, czy te dwa podejścia mogą być silniejsze razem niż każde z nich osobno.
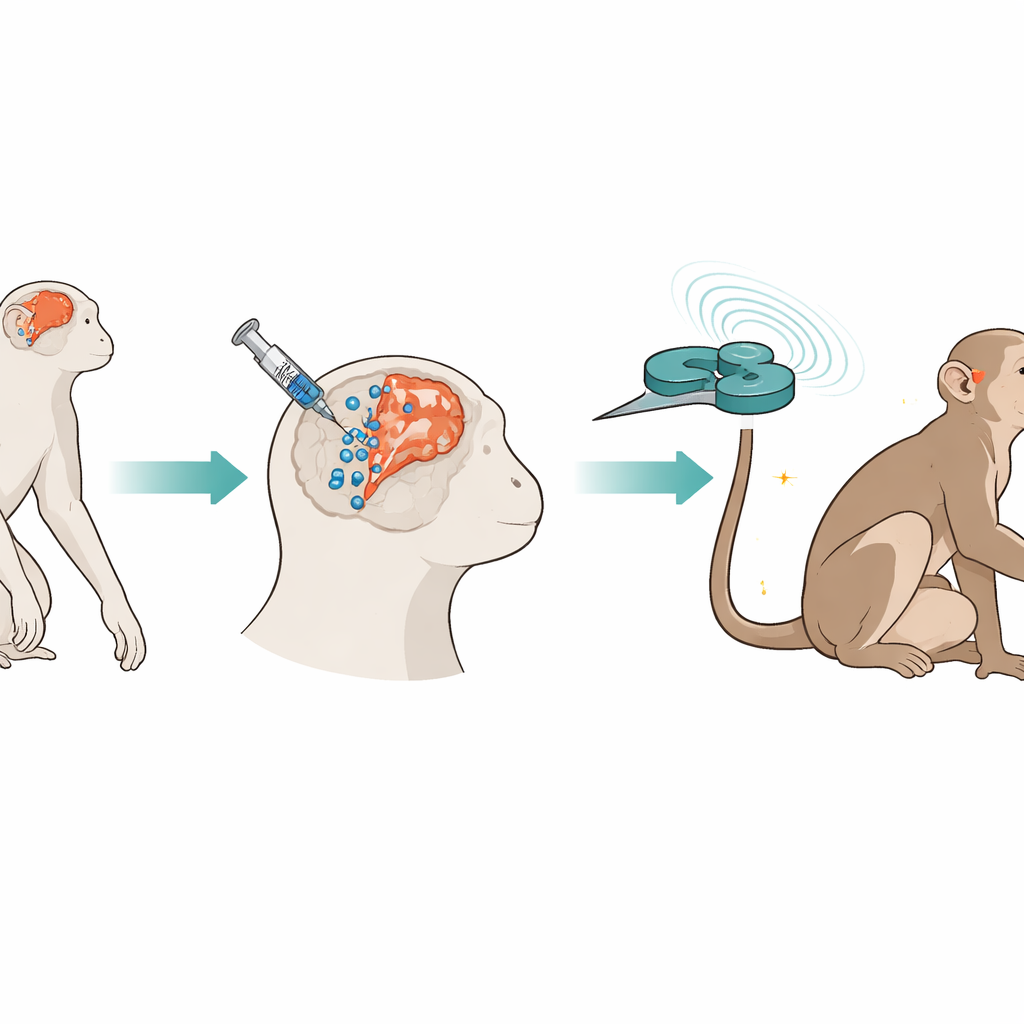
Budowanie strategii naprawczej w dwóch krokach
Badacze użyli makaków królewskich (cynomolgus), których mózgi i odpowiedzi na udar przypominają ludzkie. Dwa lata po celowym zablokowaniu tętnicy mózgowej w celu wywołania długotrwałego udaru, stereotaktycznie wstrzyknęli ludzkie mezenchymalne komórki macierzyste pochodzące z pępowiny do kilku miejsc wokół uszkodzonego obszaru oraz wzdłuż pobliskiej strefy bogatej w komórki macierzyste. Komórki oznakowano drobnymi cząstkami żelaza i znacznikami fluorescencyjnymi, by móc śledzić je w czasie za pomocą obrazowania MRI i pod mikroskopem. Tydzień później zespół rozpoczął stosowanie przerywanej stymulacji theta-burst, szybkiego wzorca impulsów magnetycznych dostarczanych przez cewkę w kształcie ósemki umieszczoną nad uszkodzoną korą ruchową. Stymulację prowadzono pięć dni w tygodniu przez 17 tygodni, podczas gdy monitorowano ruchy zwierząt, aktywność mózgu i parametry krwi.
Bardziej zdecydowane ruchy i zdrowsze sygnały mózgowe
Przed leczeniem zmanierowane kończyny małp osiągnęły plateau w zadaniach takich jak wspinanie się po małych schodkach po jedzenie czy wyciąganie smakołyków z trudnej do otwarcia skrzynki. Po terapii łączonej ich wyniki się poprawiły: wskaźniki sukcesu wzrosły, czasy wykonania skróciły się, a kiedyś osłabione kończyny zaczęto częściej używać. Badania elektrofizjologiczne wykazały, że do wywołania odpowiedzi mięśniowych z uszkodzonej strony mózgu potrzeba było mniejszej stymulacji, a sygnały przemieszczały się szybciej wzdłuż dróg ruchowych, co sugeruje naprawę okablowania. Obrazowanie mózgu potwierdziło te zmiany. Funkcjonalne MRI wykazało, że uszkodzona kora ruchowa stała się bardziej aktywna i lepiej zsynchronizowana z sąsiednimi regionami, podczas gdy siła komunikacji między obszarami związanymi z ruchem wzrosła. Obrazowanie dyfuzji sugerowało, że „kable” istoty białej przenoszące sygnały uporządkowały się bardziej, a spektroskopia magnetycznego rezonansu wykazała przesunięcia w chemii mózgu zgodne ze zdrowszymi neuronami, lepszą naprawą błon i poprawionym wykorzystaniem energii.
Obudzenie własnych komórek macierzystych mózgu
Po zakończeniu badania przeszczepione komórki macierzyste wciąż były obecne w pobliżu miejsca udaru, potwierdzając niezwykle długotrwałe przeżycie. Szczegółowe analizy białek we krwi i tkance mózgowej wykazały, że leczenie zwiększyło poziomy cząsteczek związanych z wzrostem nerwów, tworzeniem synaps i zmniejszeniem zapalenia, ale również silnie uruchomiło szlaki związane z neurogenezą — powstawaniem nowych neuronów — oraz chemotaksją, ukierunkowanym ruchem komórek. W uszkolonej półkuli zespół znalazł liczne komórki noszące markery komórek macierzystych nerwowych, które w dużej mierze nie występowały po stronie nieuszkodzonej, wraz z wczesnymi neuronami zaczynającymi przyjmować cechy komórek nerwowych. Kluczową rolę wydawał się odgrywać chemokin CXCL12, cząsteczka sygnałowa produkowana przez przeszczepione komórki macierzyste. Jej receptory występowały na własnych komórkach macierzystych mózgu, a eksperymenty laboratoryjne wykazały, że stymulacja magnetyczna pobudza komórki macierzyste do wydzielania większych ilości CXCL12 i innych czynników kierujących. Sugeruje to reakcję łańcuchową: impulsy magnetyczne skłaniają komórki przeszczepione do uwolnienia silniejszych „chemicznych sygnałów”, przyciągając rezydujące komórki macierzyste z pobliskich nisz do uszkodzonej strefy, gdzie zaczynają przekształcać się w nowe neurony.
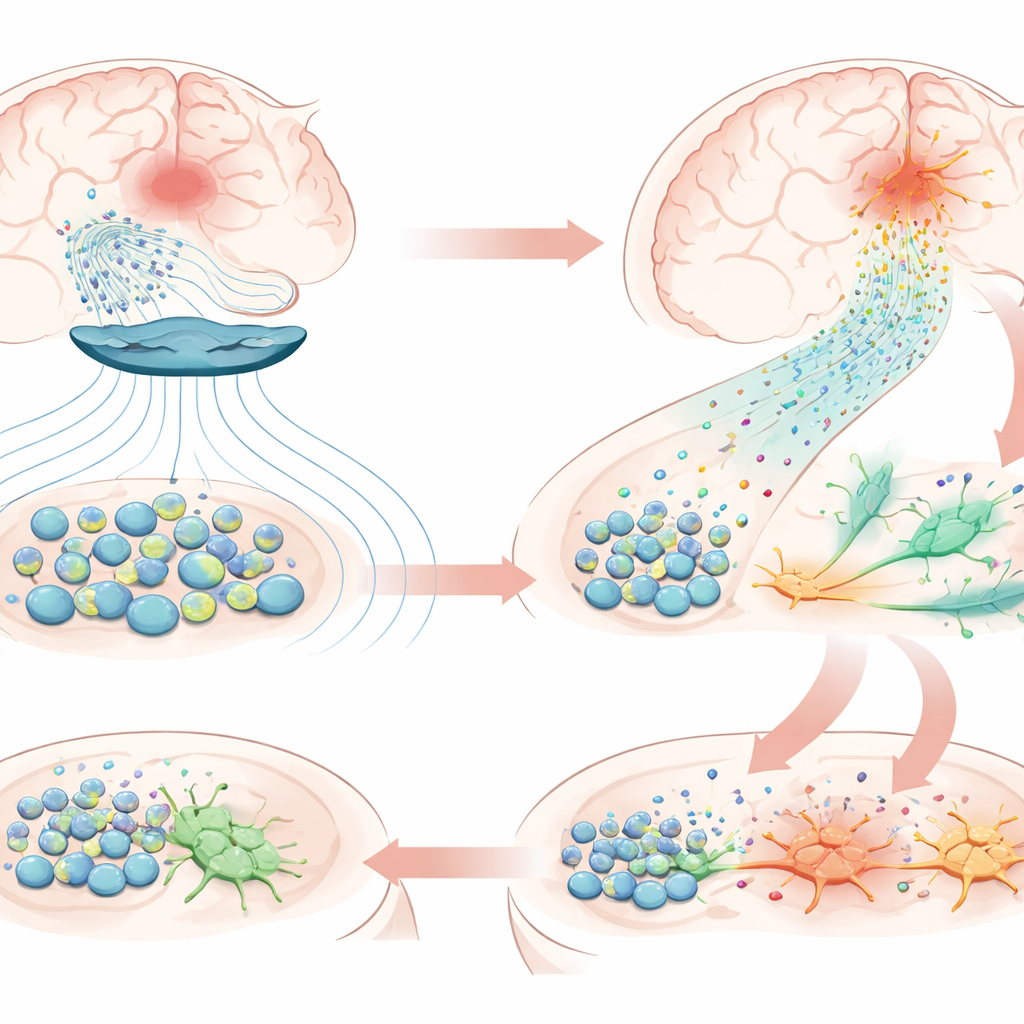
Co to może znaczyć dla przyszłych pacjentów
Dla osób żyjących z długotrwałymi następstwami udaru ta praca niesie ostrożnie optymistyczny przekaz: nawet przewlekle uszkodzony mózg może nie być poza zasięgiem naprawy. U małp połączenie przeszczepów komórek macierzystych i wzorcowej stymulacji magnetycznej zrobiło więcej niż dopracowało istniejące obwody — wydawało się ponownie uruchomić fabrykę mózgu produkującą nowe komórki nerwowe i kierować je do odbudowy uszkodzonych obszarów, co przełożyło się na wymierne poprawy ruchowe. Choć potrzebne będą większe badania, dokładne testy bezpieczeństwa i mniej inwazyjne metody podawania komórek, zanim tę strategię będzie można szeroko zastosować u ludzi, badanie wyznacza klarowny plan działania. Łącząc terapię biologiczną dostarczającą sygnały wzrostu z terapią fizyczną kształtującą wzorce aktywności, może być możliwe wydłużenie okna rehabilitacji po udarze znacznie poza to, co kiedyś uważano za granicę możliwości.
Cytowanie: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
Słowa kluczowe: przewlekły udar, terapia komórkami macierzystymi, stymulacja mózgu, neurogeneza, naczelne niebędące ludźmi