Clear Sky Science · sv
Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation
Nytt hopp för långtidsöverlevande efter stroke
Många som överlever en stroke blir kvar med bestående svaghet i en arm eller ett ben, och efter de första månaderna stagnerar ofta återhämtningen. Denna studie på apor undersöker en uppfinningsrik tvåstegsbehandling som syftar till att ”återväcka” hjärnans förmåga att reparera sig själv, även år efter en stroke. Genom att kombinera transplanterade stamceller med försiktiga magnetiska pulser över skallen visar forskarna att en till synes stabil, skadad hjärna åter kan bilda nya nervceller och återuppbygga förbindelser som förbättrar rörelseförmågan.
Varför kronisk stroke är så svår att behandla
Stroke avstänger blodflödet till delar av hjärnan, vilket dödar nervceller och lämnar ett ärrat område som styr rörelse, tal eller andra funktioner. Standardrehabilitering fungerar bäst under de första sex månaderna, när hjärnan naturligt är mest formbar. Därefter går patienterna in i en kronisk fas där förbättringar avtar drastiskt, vilket lämnar många med permanenta funktionsnedsättningar. Befintliga verktyg som magnetisk hjärnstimulering kan ge måttliga fördelar, men deras effekter tenderar att avta. Stamceller, hämtade från vävnader som benmärg eller navelsträng, har visat lovande effekter för att dämpa inflammation och stödja överlevande neuroner, men de slår sällan rot långsiktigt eller återställer funktion fullt ut. Detta arbete testar om dessa två angreppssätt kan vara starkare tillsammans än var och en för sig.
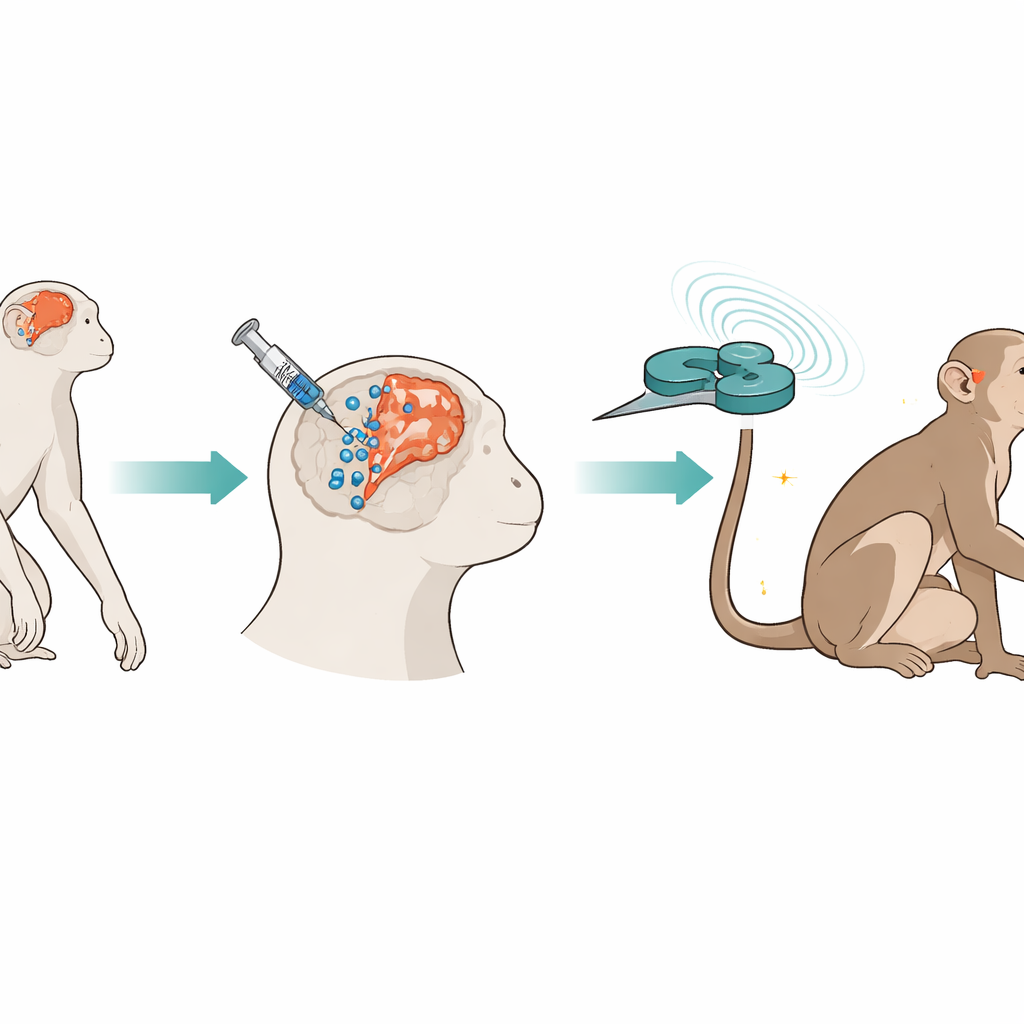
Att bygga en tvåstegs reparationsstrategi
Forskarna använde cynomolgusapor, vars hjärnor och strokereaktioner liknar människors. Två år efter att medvetet blockerat en hjärnartär för att skapa en långvarig stroke injicerade de stereotaktiskt humana navelsträngsderiverade mesenkymala stamceller i flera punkter runt det skadade området och längs en närliggande stamcellsrik zon. Cellerna märktes med små järnpartiklar och fluorescerande taggar så att de kunde följas över tid med MRT och i mikroskop. En vecka senare började teamet med intermittent theta-burst stimulation, ett snabbt mönster av magnetiska pulser levererade genom en åttformad spole placerad över den skadade motoriska cortex. Denna stimulering gavs fem dagar i veckan i 17 veckor medan djurens rörelser, hjärnaktivitet och blodkemi övervakades.
Starkare rörelser och friskare hjärnsignaler
Innan behandlingen hade apornas påverkade armar nått en prestationsplatå i uppgifter som att klättra små trappor för att hämta mat eller dra godisbitar ur en knepig låda. Efter den kombinerade terapin förbättrades deras resultat: framgångsgrader ökade, genomförandetiderna minskade och de tidigare försvagade lemmarna användes oftare. Elektriska tester visade att mindre stimulans krävdes för att utlösa muskelresponser från den skadade sidan av hjärnan, och signaler färdades snabbare längs motoriska banor, vilket antyder reparerade kopplingar. Hjärnavbildning speglade dessa förändringar. Funktionell MRT visade att den skadade motorcortex blev mer aktiv och bättre synkroniserad med närliggande regioner, samtidigt som kommunikationen mellan rörelserelaterade områden stärktes. Diffusionsavbildning antydde att de vita substansens ”kablar” som bär signaler blev mer ordnade, och magnetresonansspektroskopi visade förändringar i hjärnkemikalier som överensstämmer med friskare neuroner, bättre membranreparation och förbättrad energianvändning.
Att väcka hjärnans egna stamceller
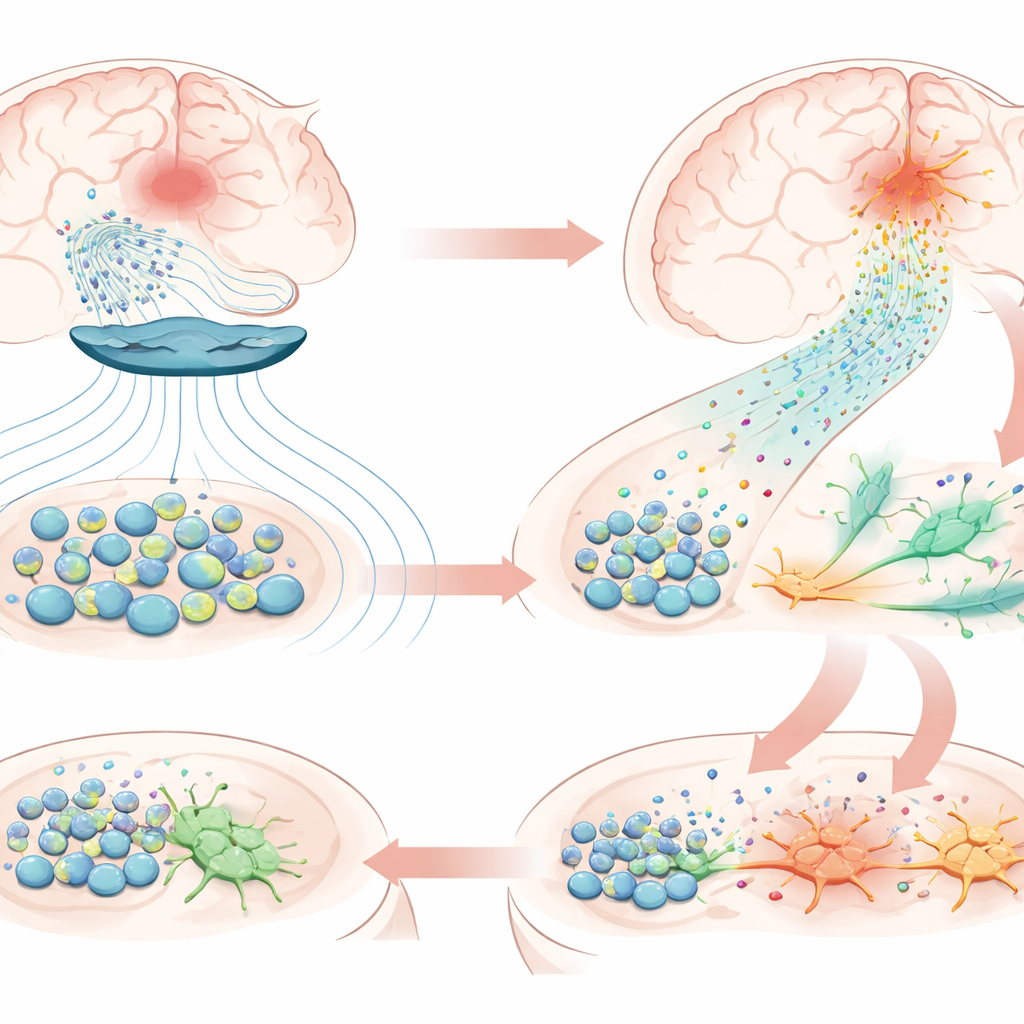
När studien avslutades fanns de transplanterade stamcellerna fortfarande kvar nära strokens centrum, vilket bekräftar ovanligt lång överlevnad. Detaljerade proteinundersökningar av blod och hjärnvävnad visade att behandlingen ökade molekyler kopplade till nervtillväxt, synapsbildning och minskad inflammation, men aktiverade också framträdande vägar kopplade till neurogenes — födelsen av nya neuroner — och kemotaxis, den riktade cellrörelsen. I den skadade hemisfären fann teamet rikliga celler med markörer för neurala stamceller, vilka i stort sett saknades på den oskadade sidan, tillsammans med tidiga neuroner som började anta nervliknande drag. En nyckelspelare verkade vara kemokinen CXCL12, en signalmolekyl som producerades av de transplanterade stamcellerna. Dess receptorer fanns på hjärnans egna stamceller, och laboratorieexperiment visade att magnetisk stimulering fick stamceller att utsöndra mer CXCL12 och andra vägledande faktorer. Detta tyder på en kedjereaktion: magnetiska pulser får transplanterade celler att släppa ut starkare ”kemiska fyrar”, som lockar residenta stamceller från närliggande nischer in i det skadade området, där de börjar omvandlas till nya neuroner.
Vad detta kan betyda för framtida patienter
För människor som lever med långvariga strokehandikapp ger detta arbete ett försiktigt optimistiskt budskap: även en kroniskt skadad hjärna kanske inte är bortom reparering. Hos apor gjorde kombinationen av stamcellstransplantat och mönstrad magnetstimulering mer än att finjustera existerande kretsar — den tycktes återstarta hjärnans egen fabrik för nya nervceller och vägleda dem in i att återbygga skadade områden, med mätbara förbättringar i rörelseförmåga. Medan det krävs större studier, noggranna säkerhetstester och mindre invasiva metoder för cellleverans innan denna strategi kan prövas i stor skala på människor, lägger studien fram en tydlig plan. Genom att para ihop en biologisk terapi som tillför tillväxtsignaler med en fysisk terapi som omformar aktivitetsmönster kan det bli möjligt att förlänga fönstret för strokeåterhämtning långt bortom vad man tidigare trodde var fastställt.
Citering: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
Nyckelord: kronisk stroke, stamcellsterapi, hjärnstimulering, neurogenes, icke-mänsklig primat