Clear Sky Science · fr
Neurogénèse robuste chez des singes atteints d’un AVC chronique après transplantation de cellules souches mésenchymateuses et stimulation theta-burst intermittente
Un nouvel espoir pour les survivants d’AVC à long terme
Beaucoup de personnes qui survivent à un AVC gardent une faiblesse persistante du bras ou de la jambe, et après les premiers mois leur récupération se stabilise souvent. Cette étude chez le singe examine un traitement inventif en deux volets qui vise à « réveiller » la capacité du cerveau à se réparer, même des années après un AVC. En combinant des cellules souches transplantées et de douces impulsions magnétiques appliquées au crâne, les chercheurs montrent qu’un cerveau apparemment stable et endommagé peut de nouveau produire de nouveaux neurones et reconstruire des connexions qui améliorent le mouvement.
Pourquoi l’AVC chronique est si difficile à traiter
L’AVC interrompt l’apport sanguin à des zones du cerveau, provoquant la mort de neurones et laissant une région cicatricielle qui contrôle le mouvement, la parole ou d’autres fonctions. La rééducation standard est la plus efficace pendant les six premiers mois, période où le cerveau est naturellement le plus plastique. Après cela, les patients entrent dans une phase chronique où les progrès ralentissent drastiquement, laissant beaucoup avec un handicap permanent. Les outils existants, comme la stimulation magnétique cérébrale, peuvent apporter des bénéfices modestes, mais leurs effets tendent à s’estomper. Les cellules souches, issues de tissus comme la moelle osseuse ou le cordon ombilical, ont montré qu’elles pouvaient calmer l’inflammation et soutenir les neurones survivants, mais elles s’intègrent rarement à long terme ou ne restaurent pas totalement la fonction. Ce travail évalue si ces deux approches pourraient être plus efficaces ensemble que chacune séparément.
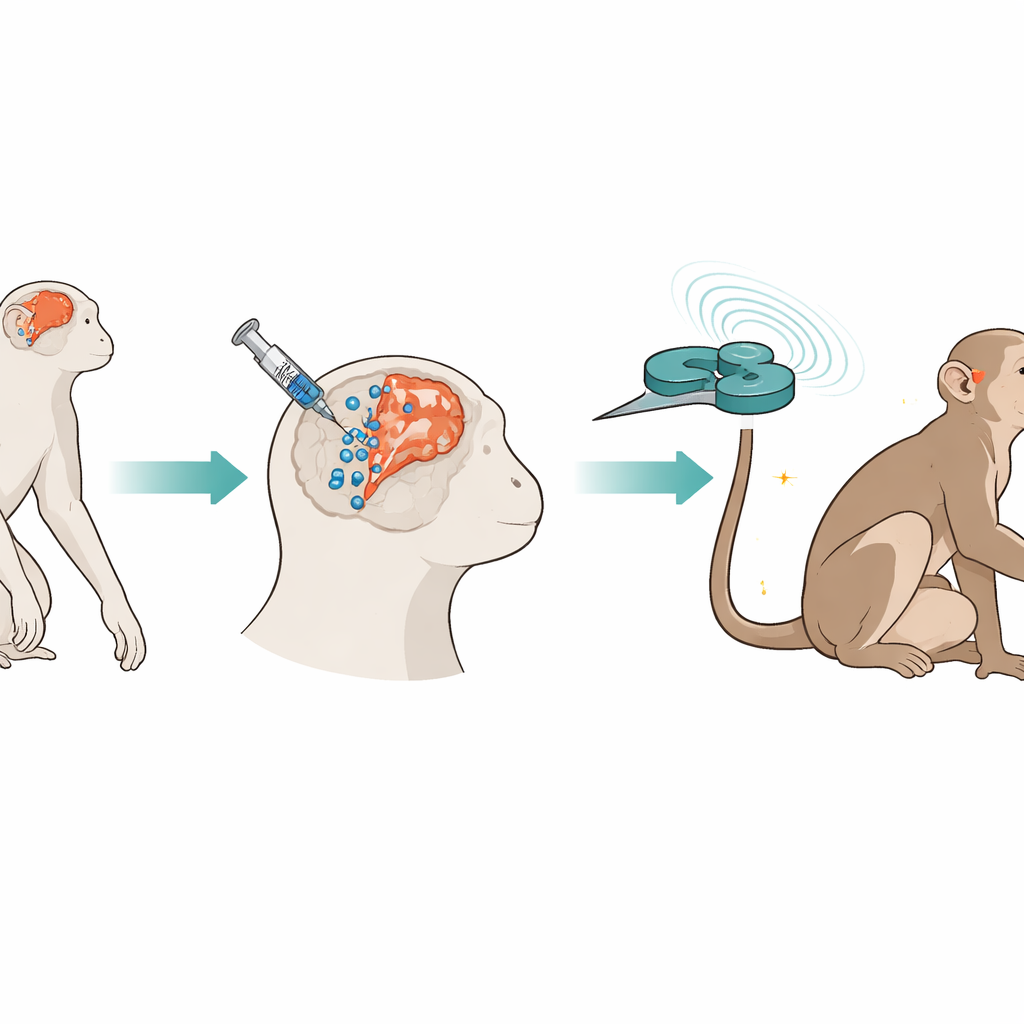
Élaborer une stratégie de réparation en deux étapes
Les chercheurs ont utilisé des macaques cynomolgus, dont le cerveau et la réponse à l’AVC ressemblent à ceux de l’homme. Deux ans après avoir délibérément obstrué une artère cérébrale pour créer un AVC durable, ils ont injecté stéréotaxiquement des cellules souches mésenchymateuses dérivées du cordon ombilical humain en plusieurs sites autour de la zone endommagée et le long d’une zone voisine riche en cellules souches. Les cellules étaient marquées par de minuscules particules de fer et des marqueurs fluorescents afin d’être suivies au fil du temps par IRM et au microscope. Une semaine plus tard, l’équipe a commencé à appliquer une stimulation theta-burst intermittente, un schéma rapide d’impulsions magnétiques délivrées via une bobine en huit positionnée au-dessus du cortex moteur lésé. Cette stimulation a été administrée cinq jours par semaine pendant 17 semaines tandis que les mouvements des animaux, l’activité cérébrale et la chimie sanguine étaient surveillés.
Mouvements renforcés et signaux cérébraux améliorés
Avant le traitement, les bras affectés des singes avaient atteint un plateau de performance dans des tâches telles que gravir de petites marches pour récupérer de la nourriture ou tirer des friandises d’une boîte difficile. Après la thérapie combinée, leurs scores se sont améliorés : les taux de réussite ont augmenté, les temps d’exécution ont diminué et les membres autrefois affaiblis ont été utilisés plus fréquemment. Des tests électriques ont montré qu’il fallait moins de stimulation pour déclencher des réponses musculaires du côté du cerveau lésé, et les signaux circulaient plus rapidement le long des voies motrices, suggérant une réparation des connexions. Les examens cérébraux reflétaient ces changements. L’IRM fonctionnelle a révélé que le cortex moteur endommagé devenait plus actif et mieux synchronisé avec les régions voisines, tandis que la force de communication entre les zones liées au mouvement augmentait. L’imagerie de diffusion suggérait que les « câbles » de substance blanche transportant les signaux devenaient plus ordonnés, et la spectroscopie par résonance magnétique montrait des variations de métabolites cérébraux compatibles avec des neurones en meilleure santé, une meilleure réparation membranaire et une utilisation énergétique améliorée.
Réveiller les propres cellules souches du cerveau
À la fin de l’étude, les cellules souches transplantées étaient encore présentes près du site de l’AVC, confirmant une survie exceptionnellement longue. Des analyses protéiques détaillées du sang et du tissu cérébral ont montré que le traitement augmentait les molécules liées à la croissance neuronale, à la formation de synapses et à la réduction de l’inflammation, mais activait aussi de façon marquée des voies associées à la neurogenèse — la naissance de nouveaux neurones — et à la chimiotaxie, le déplacement guidé des cellules. Dans l’hémisphère lésé, l’équipe a trouvé de nombreuses cellules portant des marqueurs de cellules souches neurales, qui étaient largement absentes du côté non lésé, ainsi que des neurones au stade précoce commençant à acquérir des caractéristiques nerveuses. Un acteur clé semblait être la chimiokine CXCL12, une molécule de signalisation produite par les cellules souches transplantées. Ses récepteurs étaient présents sur les propres cellules souches du cerveau, et des expériences en laboratoire ont montré que la stimulation magnétique incitait les cellules souches à sécréter davantage de CXCL12 et d’autres facteurs d’orientation. Cela suggère une réaction en chaîne : les impulsions magnétiques poussent les cellules transplantées à libérer de plus puissants « phares chimiques », attirant les cellules souches résidentes depuis des niches proches vers la zone lésée, où elles commencent à se transformer en nouveaux neurones.
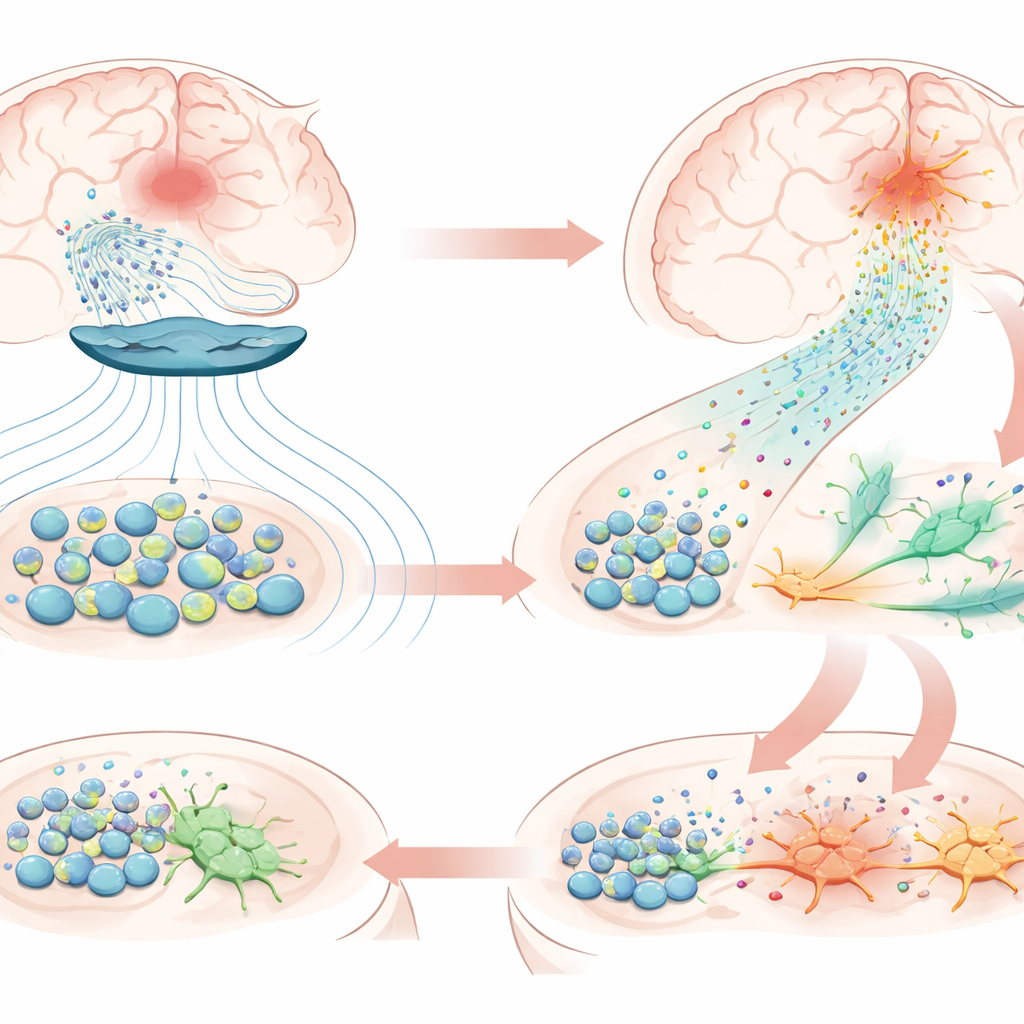
Ce que cela pourrait signifier pour les patients futurs
Pour les personnes vivant avec des séquelles d’AVC de longue date, ce travail offre un message prudemment optimiste : même un cerveau chroniquement blessé pourrait ne pas être irréparable. Chez le singe, la combinaison de greffes de cellules souches et de stimulation magnétique structurée a fait plus que peaufiner des circuits existants — elle a semblé relancer la propre « usine » du cerveau pour fabriquer de nouveaux neurones et les guider dans la reconstruction des zones endommagées, avec des améliorations mesurables du mouvement. Bien qu’il faille des études plus vastes, des tests de sécurité rigoureux et des méthodes d’administration cellulaire moins invasives avant que cette stratégie puisse être largement testée chez l’humain, l’étude trace une feuille de route claire. En mariant une thérapie biologique qui fournit des signaux de croissance à une thérapie physique qui remodèle les schémas d’activité, il pourrait être possible d’étendre la fenêtre de récupération après un AVC bien au-delà de ce que l’on pensait auparavant immuable.
Citation: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
Mots-clés: AVC chronique, thérapie par cellules souches, stimulation cérébrale, neurogénèse, primate non humain