Clear Sky Science · ar
تكوين أعصاب جديد قوي في قرود المصابين بجلطة مزمنة بعد زرع الخلايا الجذعية الميزنكيمية مع تحفيز ثيتا-بيرست متقطع
أمل جديد لنجا من الجلطات على المدى الطويل
يعاني العديد من الأشخاص الذين نجوا من سكتة دماغية من ضعف دائم في ذراع أو ساق، وبعد الأشهر الأولى غالباً ما يتوقف تحسّنهم. تستكشف هذه الدراسة على القرود علاجاً مبتكراً مؤلفاً من جزأين يهدف إلى «إيقاظ» قدرة الدماغ على الإصلاح الذاتي، حتى بعد سنوات من السكتة. من خلال جمع الخلايا الجذعية المزروعة مع نبضات مغناطيسية لطيفة عبر الجمجمة، يظهر الباحثون أن دماغاً متضرراً يوصف بأنه مستقر يمكن أن ينمو مرة أخرى خلايا عصبية جديدة ويعيد بناء اتصالات تحسّن الحركة.
لماذا من الصعب علاج السكتة المزمنة
تؤدي السكتة إلى انقطاع تدفّق الدم عن أجزاء من الدماغ، ما يقتل الخلايا العصبية ويترك وراءه منطقة متندبة تتحكم في الحركة أو النطق أو وظائف أخرى. تعمل إعادة التأهيل التقليدية بشكل أفضل خلال الأشهر الستة الأولى، عندما يكون الدماغ أكثر مرونة طبيعياً. بعد ذلك يدخل المرضى في مرحلة مزمنة تتباطأ فيها التحسينات بشكل كبير، مما يترك كثيرين بعجز دائم. الأدوات الحالية مثل التحفيز المغناطيسي الدماغي قد تقدم فوائد متواضعة، لكن آثارها تميل إلى التلاشي. أظهرت الخلايا الجذعية المستخرجة من أنسجة مثل نخاع العظم أو الحبل السري وعداً في تهدئة الالتهاب ودعم الخلايا العصبية الناجية، لكنها نادراً ما تستقر على المدى الطويل أو تستعيد الوظيفة بالكامل. تختبر هذه الدراسة ما إذا كانت هاتان الطريقتان أقوى معاً مما تكون كل منهما منفردة.
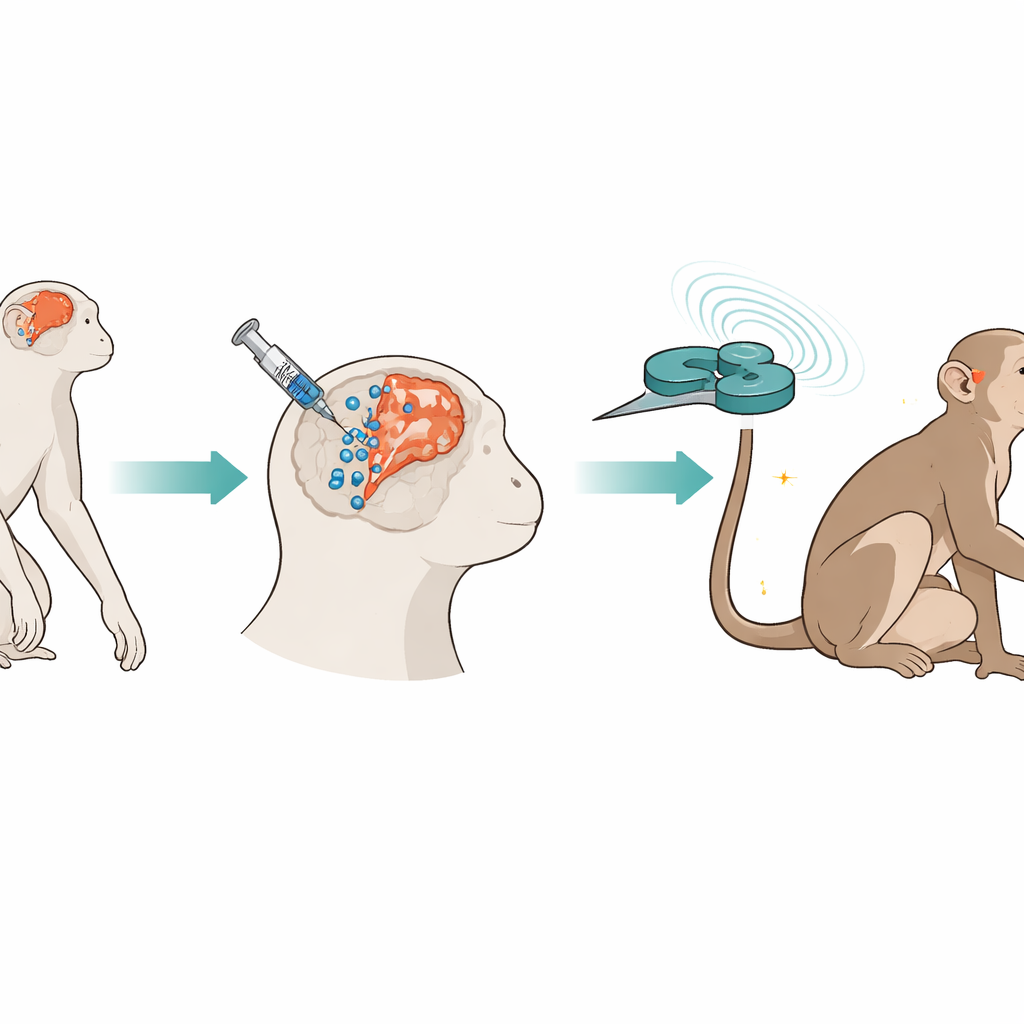
بناء استراتيجية إصلاح من خطوتين
استخدم الباحثون قرود السيناكُولوس، التي تشبه أدمغتها واستجاباتها للسكتة أدمغة البشر. بعد عامين من إغلاق عمدي لشريان دماغي لإحداث سكتة طويلة الأمد، حقنوا بطريقة ستيريوتاكتية خلايا جذعية ميزنكيمية بشرية مستمدة من الحبل السري في مواقع متعددة حول المنطقة المتضررة وطول منطقة غنية بالخلايا الجذعية المجاورة. وُسِّمت الخلايا بجزيئات حديدية صغيرة وعلامات فلورية حتى يمكن تتبّعها مع مرور الوقت عبر فحوصات الرنين المغناطيسي وتحت المجهر. بعد أسبوع، بدأ الفريق بتطبيق تحفيز ثيتا-بيرست متقطع، وهو نمط سريع من النبضات المغناطيسية الموصَّلة عبر ملف على شكل ثمانية يُمسك فوق قشرة الحركة المصابة. أُعطي هذا التحفيز خمسة أيام في الأسبوع لمدة 17 أسبوعاً بينما جرى رصد حركة الحيوانات ونشاط أدمغتها وكيمياء الدم.
حركات أقوى وإشارات دماغية أكثر صحة
قبل العلاج، وصلت أداء أذرع القرود المتأثرة إلى حالة ركود في مهام مثل تسلّق سلالم صغيرة لاسترداد الطعام أو سحب مكافآت من صندوق معقد. بعد العلاج المركب تحسنت درجاتهم: ارتفعت نسب النجاح، انخفضت أزمنة الإنجاز، وأصبحت الأطراف الضعيفة تُستخدم أكثر. أظهرت الاختبارات الكهربائية أن هناك حاجة لتحفيز أقل لإثارة استجابات العضلات من الجانب المصاب من الدماغ، وسافرت الإشارات أسرع على طول مسارات الحركة، مما يوحي بإصلاح الأسلاك. كررت صور الدماغ هذه التغيرات. كشف التصوير الوظيفي بالرنين المغناطيسي أن قشرة الحركة المتضررة أصبحت أكثر نشاطاً ومتزامنة بشكل أفضل مع المناطق المجاورة، بينما ازدادت قوة التواصل بين المناطق المتعلقة بالحركة. اقترح تصوير الانتشار أن «الكابلات» البيضاء الناقلة للإشارات نمت أكثر تنظيماً، وأظهر مطياف الرنين المغناطيسي تغيّرات في مواد الدماغ متسقة مع خلايا عصبية أكثر صحة، وإصلاح أغشية أفضل، وتحسّن في استخدام الطاقة.
إيقاظ الخلايا الجذعية الخاصة بالدماغ
عند انتهاء الدراسة، كانت الخلايا الجذعية المزروعة لا تزال حاضرة بالقرب من موضع السكتة، مؤكدة بقاء غير معتاد طويل الأمد. أظهرت مسوح مفصلة للبروتينات في الدم ونسيج الدماغ أن العلاج عزز جزيئات مرتبطة بنمو الأعصاب وتكوّن المشابك وتقليل الالتهاب، لكنه أيضاً فعّل بشكل بارز مسارات مرتبطة بالتكوّن العصبي—ولادة خلايا عصبية جديدة—والكيموتاكْسِس، التحرك الموجَّه للخلايا. في نصف الكرة المصاب وجد الفريق خلايا وفيرة تحمل علامات الخلايا الجذعية العصبية، التي كانت غائبة إلى حد كبير في الجانب غير المصاب، إلى جانب خلايا عصبية مبكرة بدأت تكتسب خصائص شبيهة بالعصبونات. بدا أن لاعباً رئيسياً هو الكيموكين CXCL12، وهو جزيء إشارة تنتجه الخلايا الجذعية المزروعة. كانت مستقبلاته حاضرة على خلايا الدماغ الجذعية الذاتية، وأظهرت تجارب المختبر أن التحفيز المغناطيسي دفع الخلايا الجذعية لإفراز المزيد من CXCL12 وعوامل إرشاد أخرى. يوحي هذا برد فعل متسلسل: النبضات المغناطيسية تدفع الخلايا المزروعة لإطلاق «منارات كيميائية» أقوى، تجذب الخلايا الجذعية المقيمة من الملاذات القريبة إلى المنطقة المتضررة، حيث تبدأ بالتحول إلى خلايا عصبية جديدة.
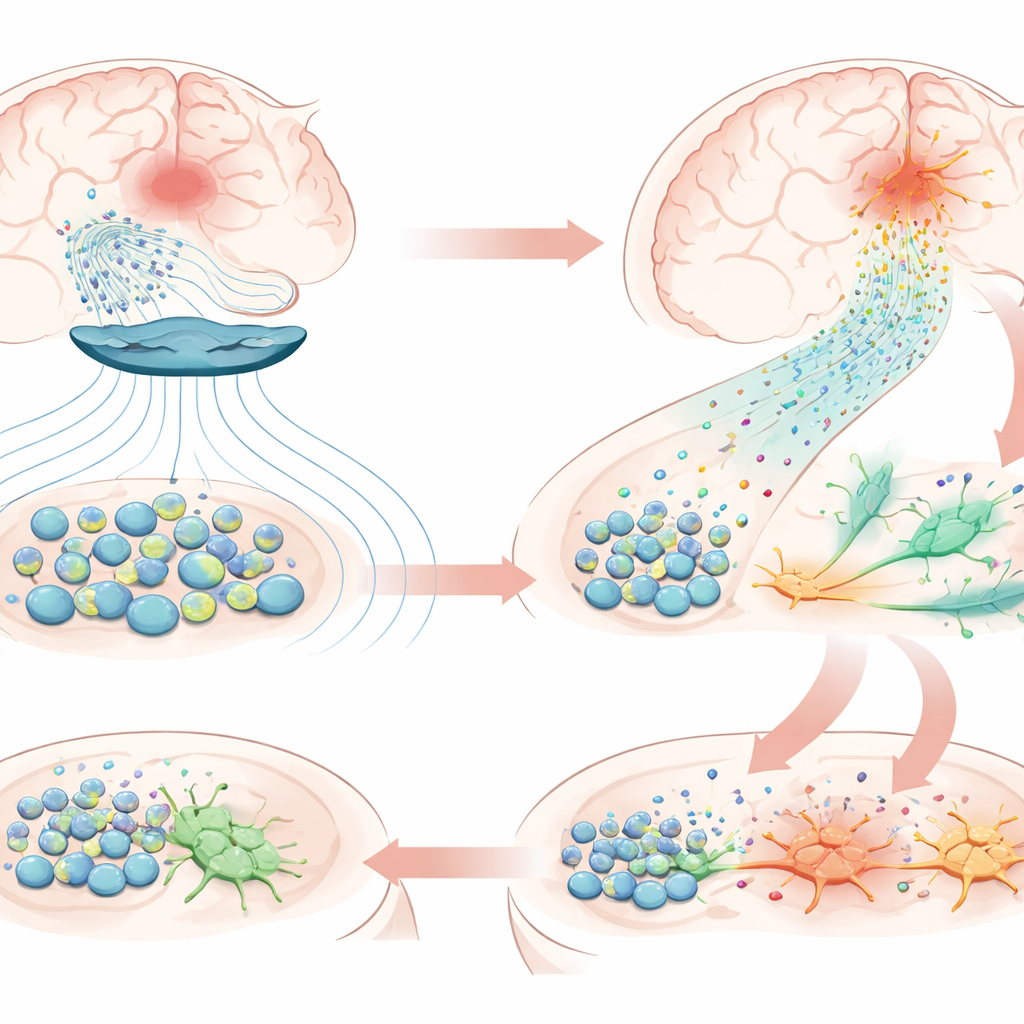
ماذا قد يعني هذا للمرضى في المستقبل
بالنسبة للأشخاص الذين يعيشون مع إعاقات سكتة دماغية مزمنة، تقدم هذه الدراسة رسالة متفائلة بحذر: قد لا يكون الدماغ المصاب المزمن خارج نطاق الإصلاح. في القرود، لم يقتصر الجمع بين طُعوم الخلايا الجذعية والتحفيز المغناطيسي المنمَّط على ضبط الدوائر القائمة فحسب—بل بدا أنه أطلق مصنع الدماغ الخاص للخلايا العصبية الجديدة ووجّهها لإعادة بناء المناطق المتضررة، مع تحسّنات قابلة للقياس في الحركة. وبينما ستحتاج الفكرة إلى دراسات أوسع، واختبارات سلامة دقيقة، وطرق توصيل خلايا أقل توغلاً قبل أن تُجرَّب على نطاق واسع لدى البشر، تضع الدراسة مخططاً واضحاً. من خلال إقران علاج حيوي يوفّر إشارات نمو مع علاج فيزيائي يعيد تشكيل أنماط النشاط، قد يكون من الممكن تمديد نافذة تعافٍ من السكتة إلى ما بعد ما كان يعتبر ثابتاً في السابق.
الاستشهاد: Ma, YH., Chen, GB., Wu, MF. et al. Robust neurogenesis in chronic stroke monkeys following mesenchymal stem cell transplantation plus intermittent theta-burst stimulation. Sig Transduct Target Ther 11, 153 (2026). https://doi.org/10.1038/s41392-026-02694-5
الكلمات المفتاحية: السكتة المزمنة, علاج بالخلايا الجذعية, تحفيز الدماغ, تكوّن عصبي, كائنات قردية غير بشرية