Clear Sky Science · zh
HERC1 致癌基因通过 IL-6/STAT3 信号通路增强来源于 CD44+ 的头颈鳞状细胞癌类器官的干性和致瘤潜能
为什么顽固的头颈癌值得关注
头颈癌常用手术、放疗和化疗治疗,但许多肿瘤会复发、转移或对药物失去反应。一个重要原因是肿瘤内存在一小群强大的细胞,表现出干细胞样特性:它们能自我更新、催生新生长并抵抗治疗。本研究揭示了一个名为 HERC1 的新的分子“开关”,助长了这些危险细胞的生存,并显示肿瘤周围支持细胞发出的信号如何使情况恶化。理解这一开关或能为阻止复发和提高生存率提供更聪明的策略。
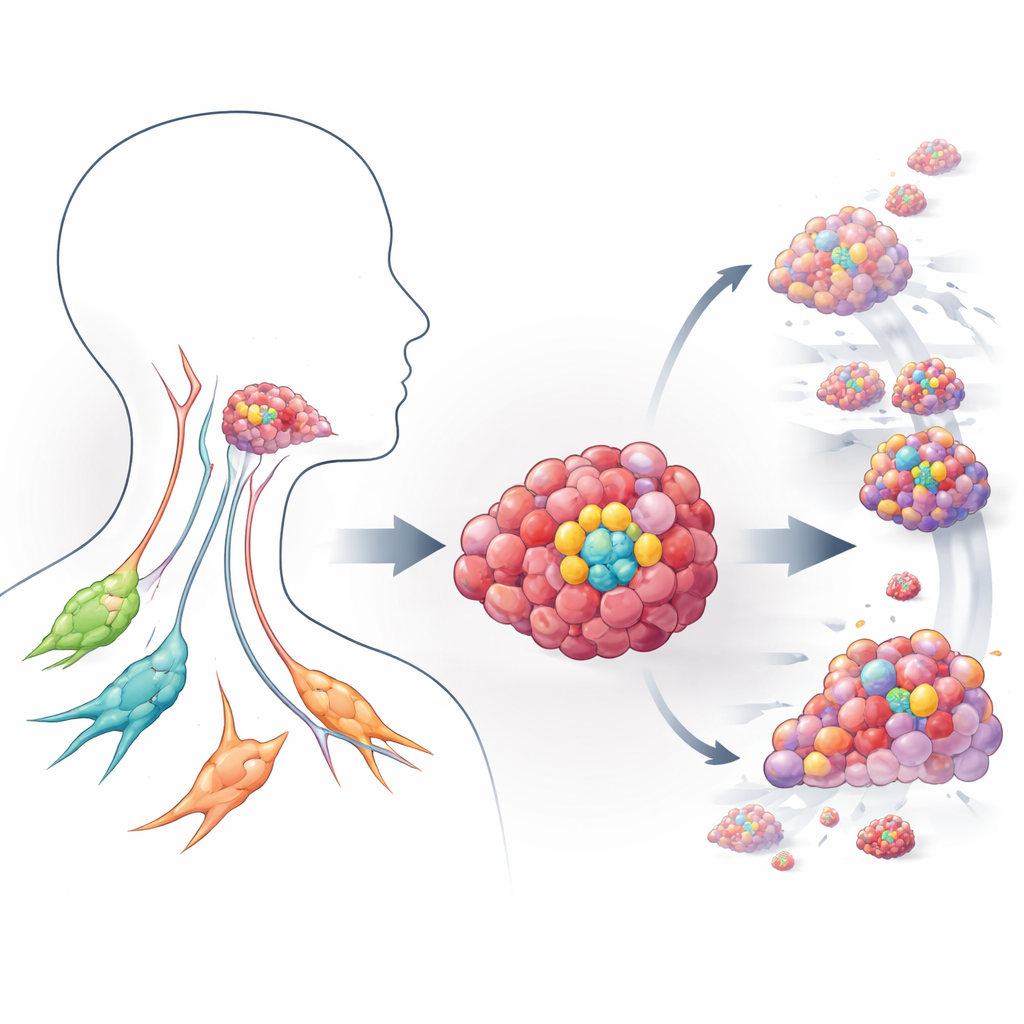
更近一步观察危险的肿瘤起始细胞
研究者把重点放在头颈部鳞状细胞癌上,这是全球最常见且难治的癌症之一。在这些肿瘤中,一部分以表面蛋白 CD44 标记的细胞表现出干细胞样特性:它们既能自我更新,又能产生多种其他肿瘤细胞,推动肿瘤生长、转移和治疗抵抗。研究团队使用来自 CD44 阳性肿瘤细胞的、与患者相关的三维培养体系(即类器官),在体外构建头颈癌的小型模型。这些类器官比平面细胞层更能模拟真实肿瘤,使科学家得以观察干样癌细胞如何与周围环境相互作用并对药物作出反应。
引入 HERC1——癌症干细胞的隐秘帮手
HERC1 是一种大型蛋白,参与将其他蛋白标记用于细胞内降解,曾与脑发育和基因组稳定性相关,但其在癌症中的作用尚不清楚。通过挖掘大型癌症基因组数据库,团队发现高表达 HERC1 与 CD44 共存的肿瘤在晚期头颈癌中更常见,并与较差的患者生存率相关。在体外培养的 CD44 阳性球体和类器官中,使用基因工具抑制 HERC1 明显降低了新球体和类器官的形成能力,并下调了诸如 Sox2 等关键干性标志物及其他自我更新因子。即便原本缺乏 CD44 的细胞在人工提升 HERC1 水平后也变得更具干性并形成更多球体,提示 HERC1 有助于产生并维持这一具有侵袭性的细胞群体。
肿瘤周围环境如何助长侵袭与扩散
肿瘤不是孤立生长的。它们被支持细胞包围,包括成纤维细胞,这些细胞可被重新编程为肿瘤相关成纤维细胞,从而积极助长肿瘤。研究显示,这些成纤维细胞释放炎性介质 IL-6,激活 CD44 阳性癌细胞内的信号蛋白 STAT3。继而提高 HERC1 活性并触发下游 ERK 通路——ERK 是已知的细胞生长与迁移驱动因子。IL-6–STAT3–HERC1–ERK 这一链条协同提升癌细胞的干性特征,促使它们发生与侵袭相关的形态学转变,并帮助它们在小鼠模型中迁移并在肺形成新肿瘤灶。当阻断 HERC1 时,动物体内的肿瘤边缘更加平滑、侵袭性下降,远处器官的转移灶明显减少。
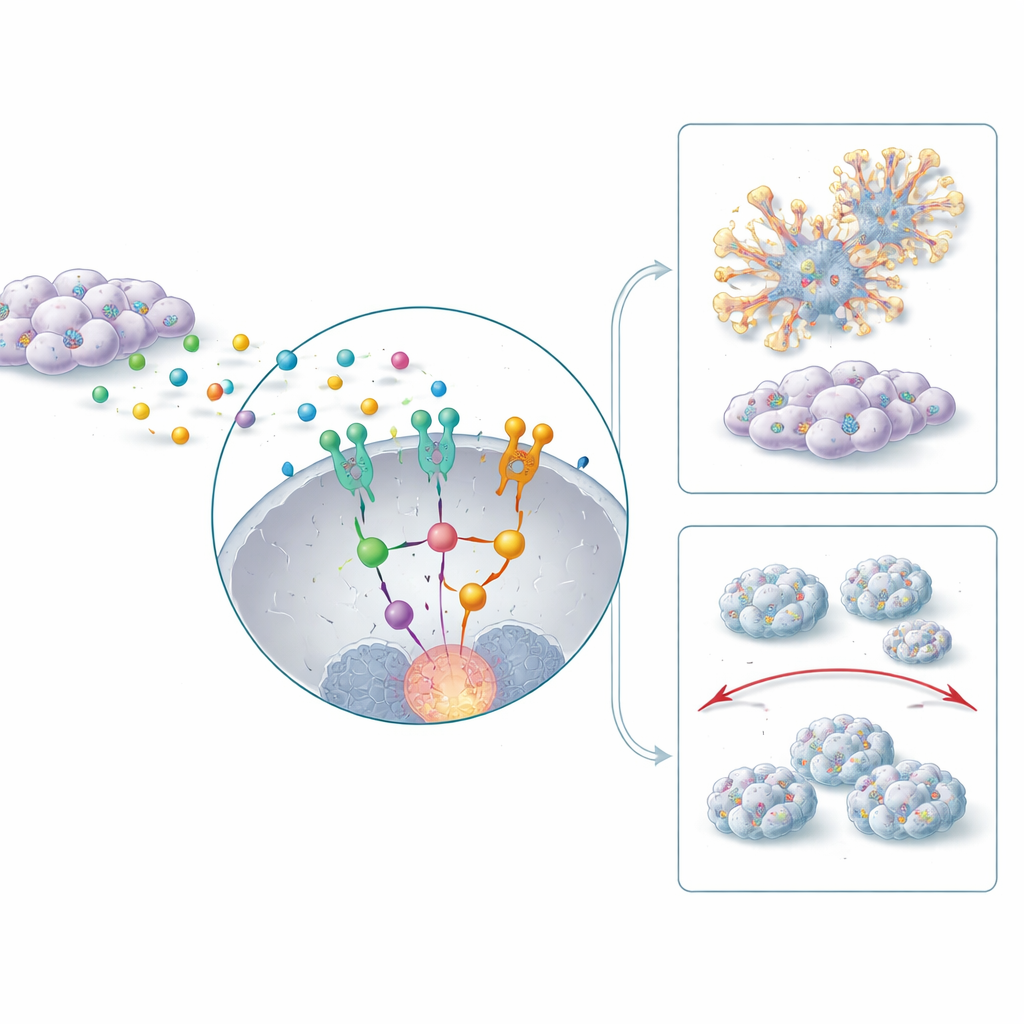
为什么有些肿瘤耐受化疗
顺铂和 5-氟尿嘧啶等常用药物是头颈癌治疗的基石,但 CD44 阳性类器官对这些药物表现出异常的抗杀伤性。研究者发现高 HERC1 水平与细胞内一种抗凋亡程序相关,涉及如 Bcl-2 等帮助细胞在应激下存活的分子。当敲低 HERC1 时,类器官对化疗的敏感性大大增加,表现为细胞凋亡酶活性增强并失去结构完整性。抑制 IL-6 或 STAT3(位于 HERC1 之上游)进一步增强了化疗的杀伤效果。在小鼠体内,将 HERC1 抑制与 5-氟尿嘧啶联合使用使肿瘤体积缩小超过四分之三,远超任何单一方法的效果。
这对未来治疗意味着什么
通过将来自肿瘤周围环境的炎性信号与癌症干样细胞内的分子开关连接起来,这项工作将 HERC1 确立为头颈癌肿瘤生长、侵袭和药物耐受的核心角色。简言之,肿瘤周围的成纤维细胞分泌 IL-6,激活 STAT3,进而提高 HERC1 并触发 CD44 阳性细胞的生长与生存通路。这些细胞因此更善于扩散且更难被消灭。研究结果提示,针对 HERC1 本身或 IL-6/STAT3/HERC1 轴的药物,可能削弱这些顽固细胞,提高常规化疗的效果,并最终减少侵袭性头颈癌患者的复发与转移。
引用: Jeong, E., Kim, H.L., Park, S. et al. HERC1 oncogene enhances stemness and tumorigenic potential in CD44+-derived organoids of head and neck squamous cell carcinoma through IL-6/STAT3 signaling. Oncogene 45, 1840–1855 (2026). https://doi.org/10.1038/s41388-026-03725-9
关键词: 头颈癌, 癌症干细胞, 肿瘤微环境, 化疗耐药, IL-6 STAT3 信号