Clear Sky Science · fr
L’oncogène HERC1 renforce les caractéristiques de cellules souches et le potentiel tumorigène dans des organoïdes dérivés de CD44+ du carcinome épidermoïde tête‑et‑cou via la signalisation IL‑6/STAT3
Pourquoi les cancers tête‑et‑cou tenaces sont importants
Les cancers de la tête et du cou sont souvent traités par chirurgie, radiothérapie et chimiothérapie, et pourtant de nombreuses tumeurs récidivent, se disséminent ou deviennent résistantes aux traitements. Une cause majeure est un petit mais puissant sous‑groupe de cellules au sein de la tumeur qui se comportent comme des cellules souches : elles s’auto‑renouvellent, engendrent de nouvelles masses tumorales et résistent aux thérapies. Cette étude met au jour un nouveau « interrupteur » moléculaire, HERC1, qui aide ces cellules dangereuses à prospérer, et montre comment des signaux émis par des cellules de soutien voisines aggravent la situation. Comprendre cet interrupteur pourrait ouvrir la voie à des stratégies plus efficaces pour prévenir les récidives et améliorer la survie.
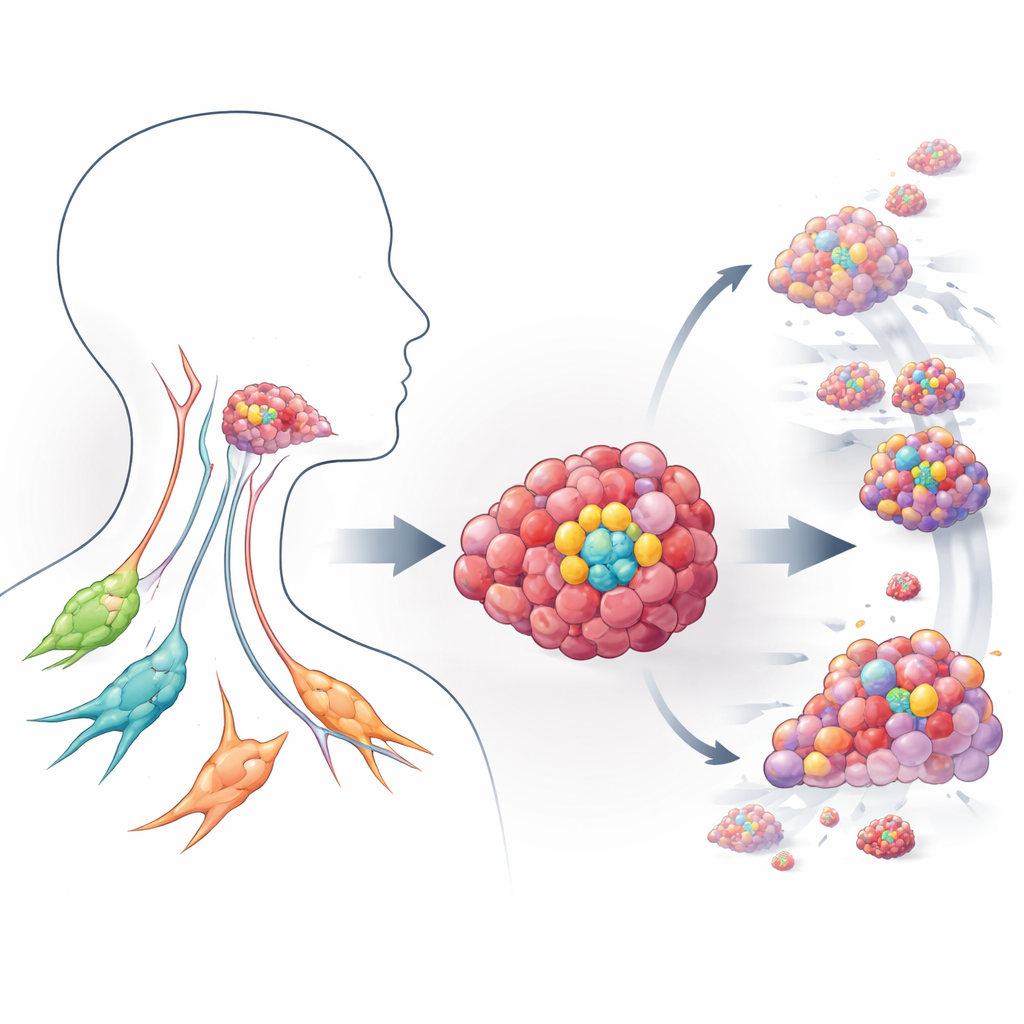
Zoom sur les cellules initiatrices tumorales dangereuses
Les chercheurs se sont concentrés sur le carcinome épidermoïde de la tête et du cou, l’un des cancers les plus courants et les plus difficiles à traiter dans le monde. Au sein de ces tumeurs, un sous‑ensemble de cellules marqué par une protéine de surface appelée CD44 se comporte comme des cellules souches : elles peuvent s’auto‑renouveler et donner naissance à de nombreuses autres cellules tumorales, stimulant la croissance, la dissémination et la résistance aux traitements. En utilisant des cultures tridimensionnelles issues de patients, appelées organoïdes, générées à partir de cellules tumorales CD44 positives, l’équipe a construit des versions miniaturisées de ces cancers en laboratoire. Ces organoïdes reproduisent les tumeurs réelles bien mieux que des couches cellulaires plates, permettant aux scientifiques d’observer comment les cellules cancéreuses de type souche interagissent avec leur environnement et répondent aux médicaments.
Présentation de HERC1, un complice caché des cellules souches cancéreuses
HERC1 est une grande protéine qui aide à marquer d’autres protéines pour leur destruction à l’intérieur des cellules et a été liée au développement cérébral et à la stabilité du génome, mais son rôle dans le cancer restait mal connu. En explorant de vastes bases de données génomiques tumorales, l’équipe a constaté que les tumeurs présentant des niveaux élevés à la fois de HERC1 et de CD44 étaient plus fréquentes dans les cancers tête‑et‑cou avancés et associées à une survie défavorable. Dans des sphéroïdes et organoïdes CD44 positifs cultivés en laboratoire, l’inactivation de HERC1 par des outils génétiques réduisait fortement leur capacité à former de nouveaux sphéroïdes et organoïdes, et diminuait des marqueurs clés de « stemness » tels que Sox2 et d’autres facteurs d’auto‑renouvellement. Même des cellules initialement dépourvues de CD44 devenaient plus de type souche et formaient davantage de sphéroïdes lorsque HERC1 était artificiellement surexprimé, suggérant que HERC1 aide à créer et à maintenir cette population cellulaire agressive.
Comment le voisinage tumoral alimente l’invasion et la dissémination
Les tumeurs ne croissent pas en isolation. Elles sont entourées de cellules de soutien, notamment des fibroblastes, qui peuvent être reprogrammés en fibroblastes associés au cancer et aider activement la tumeur. L’étude montre que ces fibroblastes libèrent le médiateur inflammatoire IL‑6, qui active une protéine de signalisation appelée STAT3 à l’intérieur des cellules cancéreuses CD44 positives. Cela augmente à son tour l’activité de HERC1 et déclenche une voie en aval impliquant ERK, un moteur bien connu de la croissance et de la mobilité cellulaires. Ensemble, cette chaîne IL‑6–STAT3–HERC1–ERK renforce les traits de type souche des cellules tumorales, favorise un processus de changement de forme associé à l’invasion, et aide ces cellules à migrer et à former de nouvelles tumeurs pulmonaires dans des modèles murins. Lorsque HERC1 était bloqué, les tumeurs animales avaient des bords plus lisses et moins invasifs et produisaient beaucoup moins de foyers métastatiques dans les organes distants.
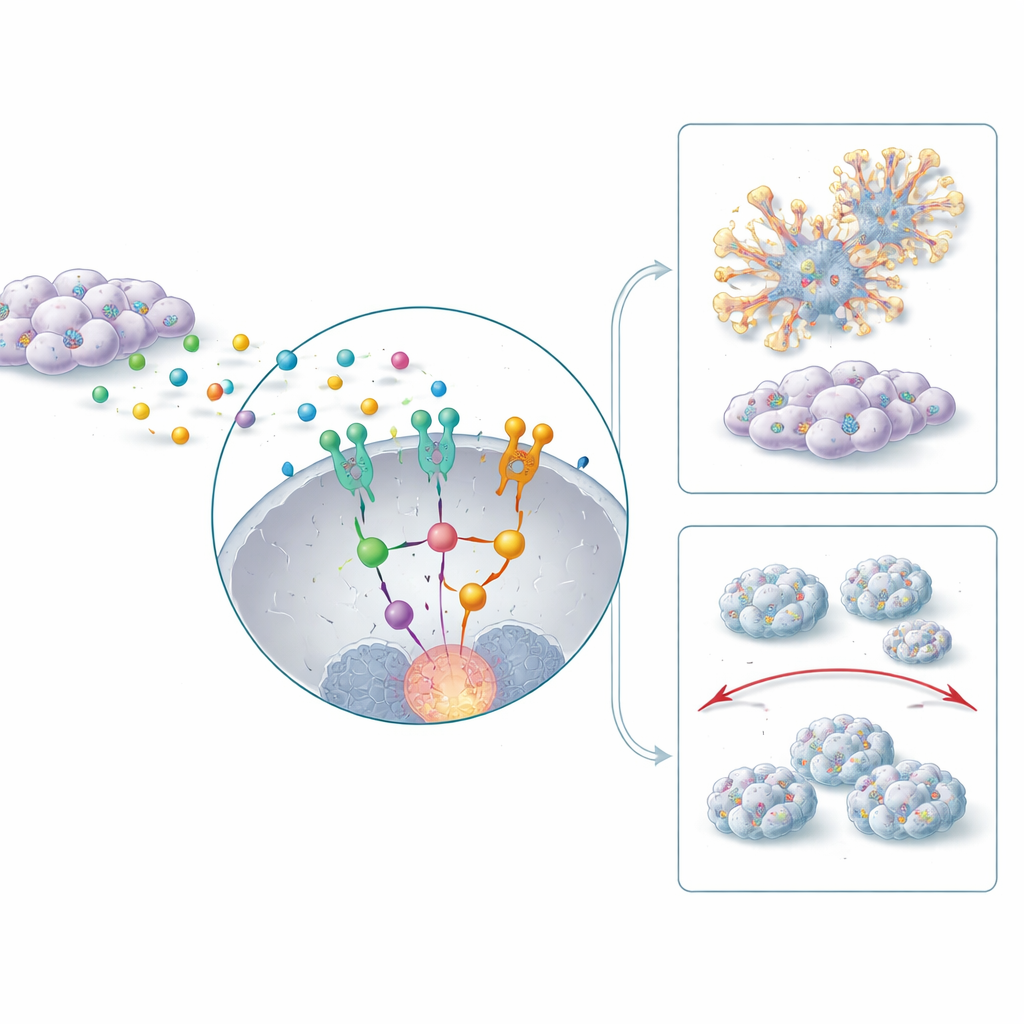
Pourquoi certaines tumeurs résistent à la chimiothérapie
Des médicaments standards tels que le cisplatine et le 5‑fluorouracile sont des piliers du traitement des cancers de la tête et du cou, mais les organoïdes CD44 positifs se sont révélés particulièrement difficiles à éradiquer avec ces agents. Les chercheurs ont découvert que des niveaux élevés de HERC1 sont liés à un programme anti‑apoptotique à l’intérieur des cellules, impliquant des molécules comme Bcl‑2 qui aident les cellules à survivre au stress. Lorsque HERC1 était réduit, les organoïdes devenaient beaucoup plus sensibles à la chimiothérapie, montrant une activation accrue des enzymes de mort cellulaire et une perte de leur intégrité structurelle. Bloquer IL‑6 ou STAT3, en amont de HERC1, renforçait encore l’effet cytotoxique de la chimiothérapie. Chez la souris, l’association d’une inhibition de HERC1 avec du 5‑fluorouracile a réduit les tumeurs de plus des trois quarts, bien plus que chaque traitement administré seul.
Ce que cela signifie pour les traitements futurs
En reliant les signaux inflammatoires du microenvironnement tumoral à un interrupteur moléculaire à l’intérieur des cellules cancéreuses de type souche, ce travail identifie HERC1 comme un acteur central de la croissance tumorale, de l’invasion et de la résistance aux médicaments dans le cancer de la tête et du cou. En termes simples, les fibroblastes entourant la tumeur émettent des signaux IL‑6 qui activent STAT3, ce qui augmente ensuite HERC1 et déclenche des voies de croissance et de survie dans les cellules CD44 positives. Ces cellules deviennent ainsi plus aptes à se disséminer et plus difficiles à éliminer. Les résultats suggèrent que des médicaments ciblant HERC1 lui‑même, ou la chaîne IL‑6/STAT3/HERC1, pourraient affaiblir ces cellules tenaces, rendre les chimiothérapies standards plus efficaces et, en fin de compte, réduire les récidives et les métastases chez les patients atteints de formes agressives de cancer tête‑et‑cou.
Citation: Jeong, E., Kim, H.L., Park, S. et al. HERC1 oncogene enhances stemness and tumorigenic potential in CD44+-derived organoids of head and neck squamous cell carcinoma through IL-6/STAT3 signaling. Oncogene 45, 1840–1855 (2026). https://doi.org/10.1038/s41388-026-03725-9
Mots-clés: cancer de la tête et du cou, cellules souches cancéreuses, microenvironnement tumoral, résistance aux chimiothérapies, signalisation IL‑6 STAT3