Clear Sky Science · de
Das Onkogen HERC1 verstärkt Stammzell-Eigenschaften und Tumorbildungs-Potenzial in aus CD44+ stammenden Organoiden des Plattenepithelkarzinoms von Kopf und Hals über IL-6/STAT3-Signalgebung
Warum hartnäckige Kopf‑und‑Hals‑Tumoren wichtig sind
Kopf‑und‑Hals‑Krebs wird häufig mit Operation, Strahlentherapie und Chemotherapie behandelt, doch viele Tumoren kehren zurück, streuen oder sprechen nicht mehr auf Medikamente an. Ein wesentlicher Grund ist eine kleine, aber mächtige Zellpopulation im Tumor, die sich wie Stammzellen verhält: sie erneuert sich selbst, setzt neues Wachstum in Gang und ist gegenüber Therapien widerstandsfähig. Diese Studie deckt einen neuen molekularen „Schalter“ namens HERC1 auf, der diesen gefährlichen Zellen hilft zu überleben, und zeigt, wie Signale benachbarter Stütz‑ und Bindegewebszellen im Tumor das Problem verschärfen. Das Verständnis dieses Schalters könnte auf intelligentere Wege hinweisen, Rückfälle zu verhindern und das Überleben zu verbessern.
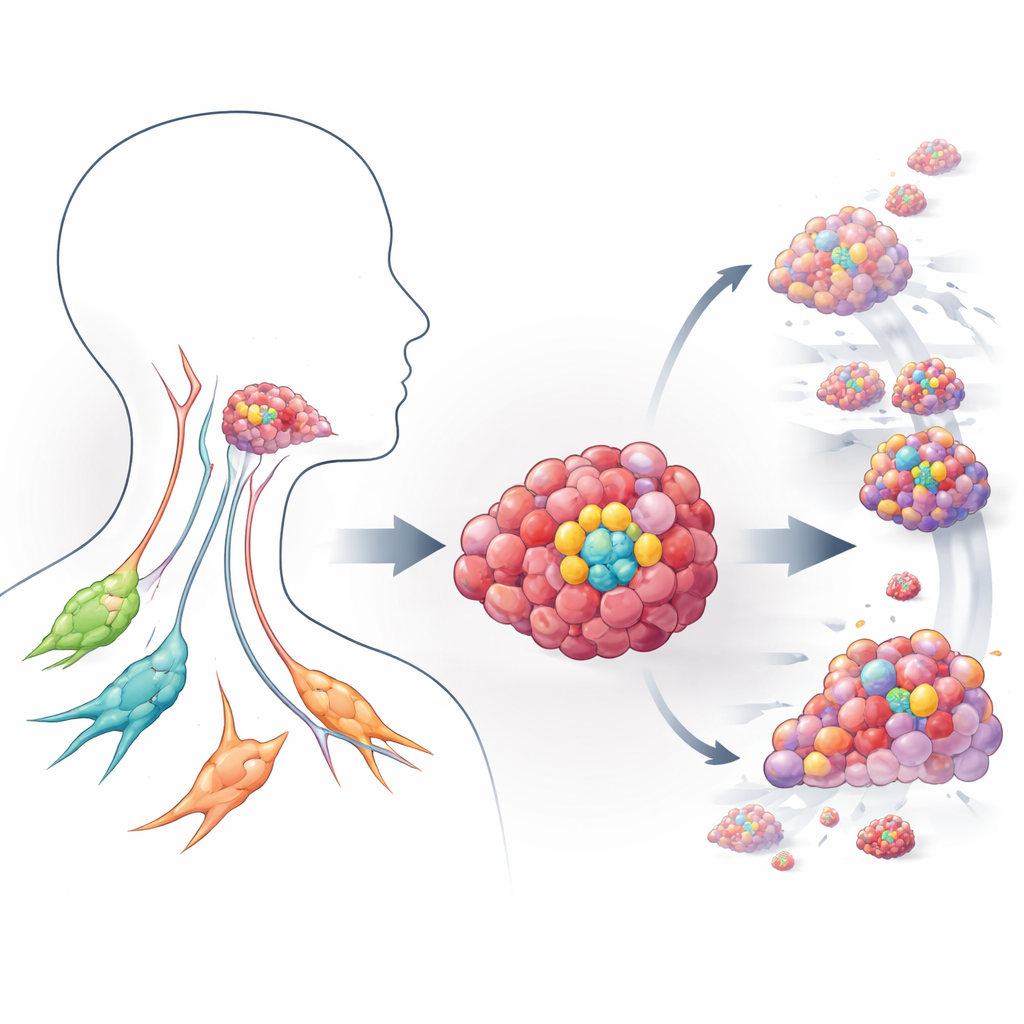
Ein genauerer Blick auf gefährliche Tumor‑Starterzellen
Die Forschenden konzentrierten sich auf das Plattenepithelkarzinom des Kopfes und Halses, eine der weltweit häufigsten und schwer behandelbaren Krebsarten. Innerhalb dieser Tumoren verhält sich eine Untergruppe von Zellen, die durch das Oberflächenprotein CD44 markiert sind, wie Stammzellen: Sie können sich selbst erneuern und viele andere Tumorzellen hervorbringen, was Wachstum, Ausbreitung und Therapie‑Resistenz antreibt. Mithilfe patientenrelevanter dreidimensionaler Kulturen, so genannter Organoide, die aus CD44‑positiven Tumorzellen gezüchtet wurden, bauten die Forschenden Miniaturversionen von Kopf‑und‑Hals‑Tumoren im Labor. Diese Organoide ahmen echte Tumoren wesentlich besser nach als zweidimensionale Zellschichten und erlauben es, zu beobachten, wie stammzellähnliche Krebszellen mit ihrer Umgebung interagieren und auf Medikamente reagieren.
Vorstellung von HERC1, einem verborgenen Helfer der Krebsstammzellen
HERC1 ist ein großes Protein, das hilft, andere Proteine innerhalb der Zelle für den Abbau zu markieren, und wurde mit Gehirnentwicklung und Genomstabilität in Verbindung gebracht; seine Rolle im Krebs war jedoch wenig bekannt. Durch die Analyse großer Krebsgenom‑Datenbanken fanden die Forschenden heraus, dass Tumoren mit hohen HERC1‑ und CD44‑Werten häufiger bei fortgeschrittenen Kopf‑und‑Hals‑Krebsfällen vorkommen und mit schlechterem Überleben der Patienten assoziiert sind. In im Labor gezüchteten CD44‑positiven Sphäroiden und Organoiden führte das Herunterregulieren von HERC1 mit genetischen Werkzeugen zu einer starken Verringerung ihrer Fähigkeit, neue Sphäroide und Organoide zu bilden, und senkte Schlüsselmarker der Stammzelligkeit wie Sox2 und andere Selbsterneuerungsfaktoren. Selbst Zellen, die ursprünglich kein CD44 exprimierten, wurden stammzellähnlicher und bildeten mehr Sphäroide, wenn HERC1 künstlich erhöht wurde, was darauf hindeutet, dass HERC1 hilft, diese aggressive Zellpopulation zu erzeugen und zu erhalten.
Wie die Tumorumgebung Invasion und Ausbreitung antreibt
Tumoren wachsen nicht isoliert. Sie sind von Stütz‑ und Bindegewebszellen umgeben, darunter Fibroblasten, die in cancer‑associated fibroblasts (tumorassoziierte Fibroblasten) umprogrammiert werden können und den Tumor aktiv unterstützen. Die Studie zeigt, dass diese Fibroblasten den Entzündungsbotenstoff IL‑6 freisetzen, der das Signalmolekül STAT3 in CD44‑positiven Krebszellen aktiviert. Das wiederum erhöht die HERC1‑Aktivität und löst eine nachgeschaltete Kaskade aus, an der ERK beteiligt ist — ein bekannter Treiber von Zellwachstum und Bewegung. Zusammen stärken diese IL‑6–STAT3–HERC1–ERK‑Signale die stammzellähnlichen Eigenschaften der Krebszellen, fördern einen Formwechsel‑Prozess, der mit Invasion verbunden ist, und unterstützen Migration sowie die Etablierung neuer Tumoren in der Lunge bei Mausmodellen. Bei Blockade von HERC1 zeigten Tumoren in Tieren glattere, weniger invasive Ränder und bildeten deutlich weniger metastatische Herde in entfernten Organen.
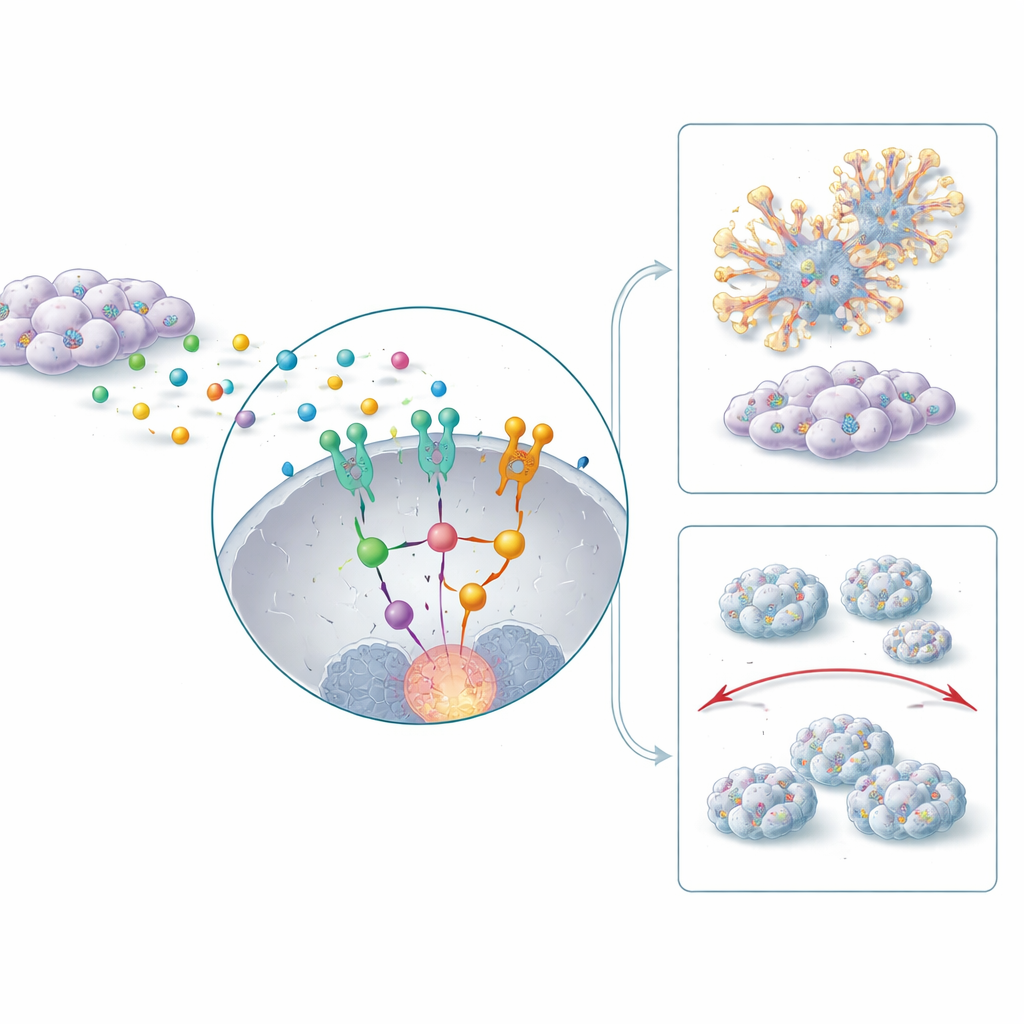
Warum einige Tumoren Chemotherapie widerstehen
Standardmedikamente wie Cisplatin und 5‑Fluorouracil sind Pfeiler der Behandlung von Kopf‑und‑Hals‑Krebs, doch CD44‑positive Organoide erwiesen sich als ungewöhnlich resistent gegenüber diesen Wirkstoffen. Die Forschenden entdeckten, dass hohe HERC1‑Spiegel mit einem Anti‑Apoptose‑Programm in den Zellen verbunden sind, das Moleküle wie Bcl‑2 einschließt und Zellen hilft, Stress zu überleben. Beim Herunterregulieren von HERC1 wurden Organoide deutlich empfindlicher gegenüber Chemotherapie, zeigten eine verstärkte Aktivierung von Todesenzymen und verloren ihre strukturelle Integrität. Die Blockade von IL‑6 oder STAT3, die stromaufwärts von HERC1 liegen, verstärkte die zytotoxische Wirkung der Chemotherapie zusätzlich. In Mäusen schrumpften Tumoren bei Kombination von HERC1‑Hemmung mit 5‑Fluorouracil um mehr als drei Viertel — deutlich mehr als bei einer der beiden Maßnahmen allein.
Was das für künftige Therapien bedeutet
Indem diese Arbeit entzündliche Signale aus der Tumorumgebung mit einem molekularen Schalter in stammzellähnlichen Krebszellen verbindet, identifiziert sie HERC1 als zentralen Akteur für Tumorwachstum, Invasion und Wirkstoffresistenz beim Kopf‑und‑Hals‑Krebs. Kurz gesagt: Fibroblasten rund um den Tumor senden IL‑6, das STAT3 einschaltet, was HERC1 hochfährt und Wachstums‑ und Überlebenswege in CD44‑positiven Zellen aktiviert. Diese Zellen werden besser im Ausbreiten und schwerer zu töten. Die Ergebnisse deuten darauf hin, dass Wirkstoffe, die direkt auf HERC1 oder auf die Kette IL‑6/STAT3/HERC1 abzielen, diese hartnäckigen Zellen schwächen, Standardchemotherapien wirksamer machen und schließlich Rückfall und Metastasierung bei Patientinnen und Patienten mit aggressiven Kopf‑und‑Hals‑Tumoren reduzieren könnten.
Zitation: Jeong, E., Kim, H.L., Park, S. et al. HERC1 oncogene enhances stemness and tumorigenic potential in CD44+-derived organoids of head and neck squamous cell carcinoma through IL-6/STAT3 signaling. Oncogene 45, 1840–1855 (2026). https://doi.org/10.1038/s41388-026-03725-9
Schlüsselwörter: Kopf‑und‑Hals‑Krebs, Krebsstammzellen, Tumormikroumgebung, Chemoresistenz, IL‑6 STAT3 Signalgebung