Clear Sky Science · pl
Onkogen HERC1 wzmacnia właściwości komórek macierzystych i potencjał nowotworotwórczy w organoidach pochodzących z CD44+ raka płaskonabłonkowego głowy i szyi poprzez sygnalizację IL-6/STAT3
Dlaczego uporczywe nowotwory głowy i szyi mają znaczenie
Nowotwory głowy i szyi są często leczone chirurgicznie, radioterapią i chemioterapią, jednak wiele guzów nawraca, metastazuje lub przestaje reagować na leki. Istotną przyczyną jest niewielka, lecz potężna populacja komórek w guzie, które zachowują się jak komórki macierzyste: potrafią samoodnawiać się, inicjować nowe ogniska wzrostu i opierać się terapii. W badaniu odkryto nowy molekularny „włącznik” o nazwie HERC1, który pomaga tym niebezpiecznym komórkom przetrwać, oraz wykazano, jak sygnały od pobliskich komórek wspierających w mikrośrodowisku guza pogarszają sytuację. Zrozumienie tego przełącznika może wskazać lepsze sposoby zapobiegania nawrotom i poprawy przeżywalności.
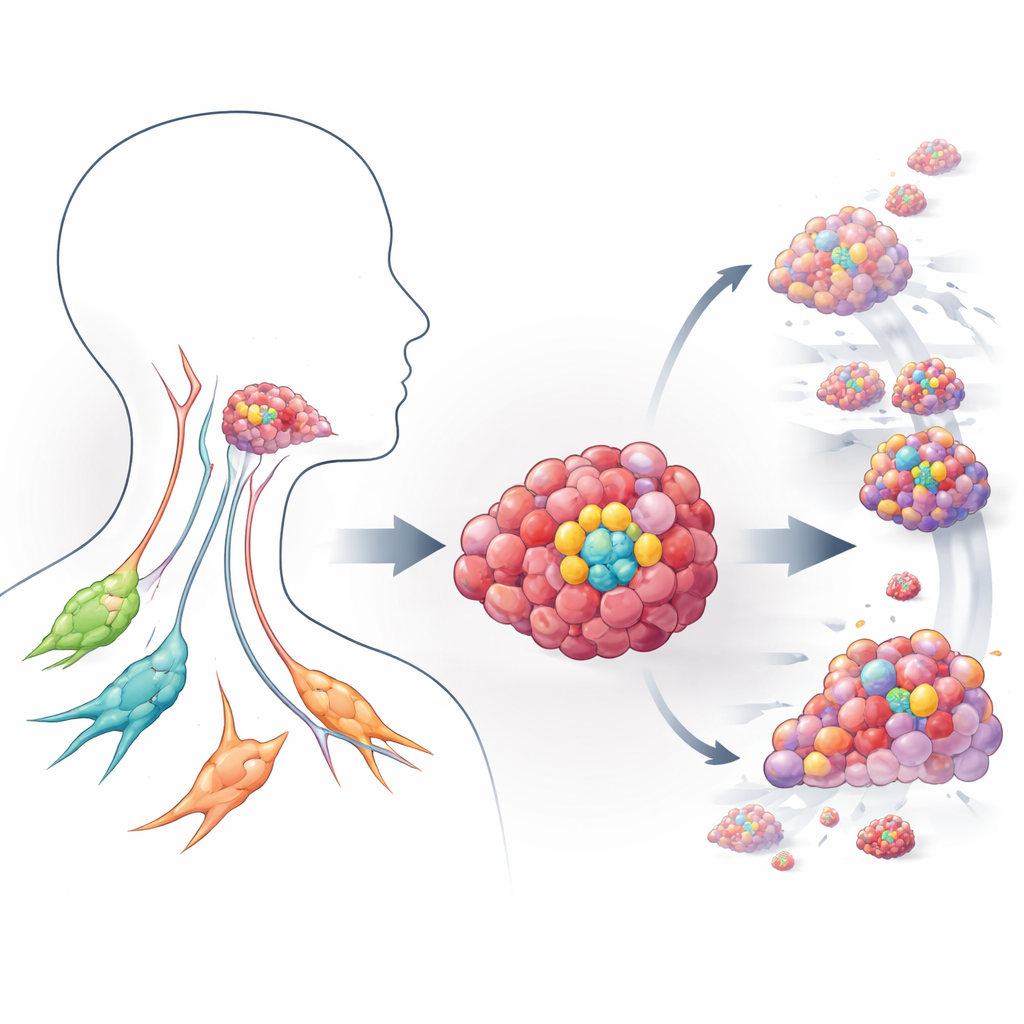
Bliższe spojrzenie na niebezpieczne komórki inicjujące guz
Naukowcy skupili się na raku płaskonabłonkowym głowy i szyi, jednym z najczęstszych i najtrudniejszych do leczenia nowotworów na świecie. W tych guzach istnieje podzbiór komórek oznaczonych białkiem powierzchniowym CD44, które zachowują się jak komórki macierzyste: potrafią zarówno samoodnawiać się, jak i dawać początek wielu innym komórkom nowotworowym, napędzając wzrost, rozsiew i oporność na terapię. Wykorzystując trójwymiarowe hodowle o istotnym znaczeniu klinicznym, zwane organoidami, hodowane z komórek guza pozytywnych dla CD44, zespół stworzył miniaturowe wersje guzów głowy i szyi w warunkach laboratoryjnych. Te organoidy odtwarzają prawdziwe nowotwory znacznie lepiej niż płaskie monowarstwy komórkowe, pozwalając naukowcom obserwować, jak komórki o cechach macierzystych wchodzą w interakcje z otoczeniem i reagują na leki.
Przedstawiamy HERC1, ukrytego wspomagacza komórek nowotworowych macierzystych
HERC1 to duże białko uczestniczące w oznaczaniu innych białek do degradacji w komórce i było powiązane z rozwojem mózgu oraz stabilnością genomu, lecz jego rola w nowotworach była słabo poznana. Analiza dużych baz genomowych nowotworów wykazała, że guzy z wysokim poziomem zarówno HERC1, jak i CD44 występowały częściej w zaawansowanych przypadkach raka głowy i szyi i wiązały się z gorszym przeżyciem pacjentów. W hodowlach sferoidów i organoidów pochodzących z komórek CD44-dodatnich, wyłączenie HERC1 za pomocą narzędzi genetycznych znacznie zmniejszało ich zdolność do tworzenia nowych sferoidów i organoidów oraz obniżało kluczowe markery „stemness”, takie jak Sox2 i inne czynniki samoodnowy. Nawet komórki początkowo pozbawione CD44 stawały się bardziej przypominające komórki macierzyste i tworzyły więcej sferoidów po sztucznym zwiększeniu ekspresji HERC1, co sugeruje, że HERC1 pomaga tworzyć i utrzymywać tę agresywną populację komórek.
Jak sąsiedztwo guza napędza inwazję i rozsiew
Guzy nie rosną w izolacji. Otaczają je komórki wspierające, w tym fibroblasty, które mogą zostać przeprogramowane w fibroblasty związane z nowotworem i aktywnie mu pomagać. Badanie pokazuje, że te fibroblasty wydzielają zapalny przekaźnik IL-6, który aktywuje białko sygnałowe STAT3 wewnątrz komórek CD44-dodatnich. To z kolei zwiększa aktywność HERC1 i uruchamia szlak pośredniczący obejmujący ERK, dobrze znany promotor wzrostu i motoryki komórkowej. Łańcuch IL-6–STAT3–HERC1–ERK wzmacnia cechy przypominające komórki macierzyste, sprzyja przejściu komórek w stan związany z inwazją oraz pomaga im migrować i zasiedlać nowe guzy w płucach u modeli mysich. Po zablokowaniu HERC1 guzy u zwierząt miały gładsze, mniej naciekające brzegi i dały znacznie mniej ognisk przerzutowych w odległych narządach.
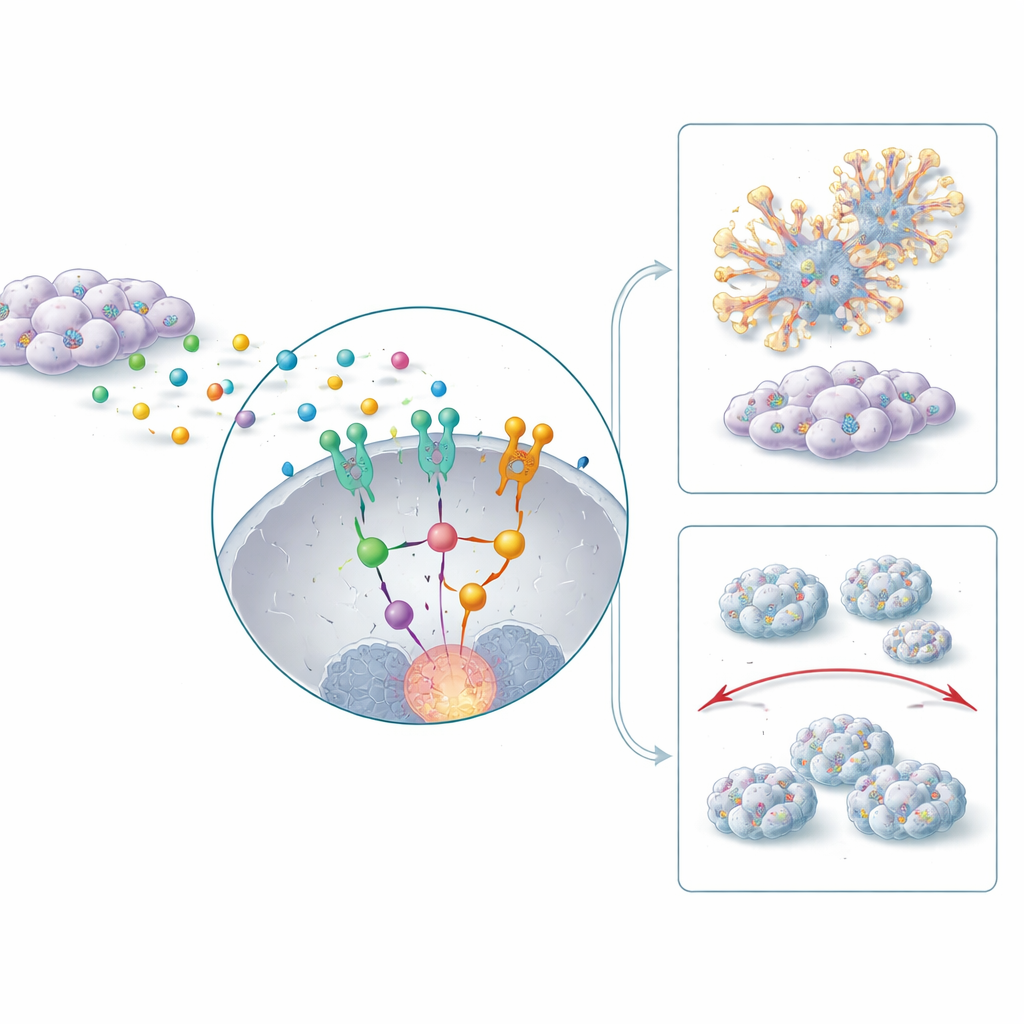
Dlaczego niektóre guzy opierają się chemioterapii
Standardowe leki, takie jak cisplatyna i 5-fluorouracyl, są podstawą leczenia raka głowy i szyi, lecz organoidy CD44-dodatnie okazały się wyjątkowo oporne na te środki. Naukowcy odkryli, że wysoki poziom HERC1 wiąże się z programem anty-apoptotycznym w komórkach, obejmującym cząsteczki takie jak Bcl-2, które pomagają komórkom przetrwać stres. Po zahamowaniu HERC1 organoidy stały się znacznie bardziej wrażliwe na chemioterapię, wykazując zwiększoną aktywację enzymów odpowiedzialnych za śmierć komórkową i utratę integralności strukturalnej. Blokowanie IL-6 lub STAT3, które działają powyżej HERC1, dodatkowo zwiększało efekt zabijający chemioterapii. U myszy połączenie hamowania HERC1 z 5-fluorouracylem zmniejszyło guzy o ponad trzy czwarte, znacznie bardziej niż każde z tych podejść osobno.
Co to oznacza dla przyszłych terapii
Łącząc zapalne sygnały z mikrośrodowiska guza z molekularnym przełącznikiem wewnątrz komórek o cechach macierzystych, ta praca wskazuje HERC1 jako centralny czynnik wzrostu guza, inwazji i oporności na leki w raku głowy i szyi. Mówiąc prościej: fibroblasty wokół guza wysyłają sygnał IL-6, który uruchamia STAT3, co następnie zwiększa HERC1 i aktywuje szlaki wzrostu i przetrwania w komórkach CD44-dodatnich. Te komórki stają się lepsze w rozsiewie i trudniejsze do zabicia. Wyniki sugerują, że leki celujące w sam HERC1 lub w łańcuch IL-6/STAT3/HERC1 mogą osłabić te oporne komórki, zwiększyć skuteczność standardowej chemioterapii i ostatecznie zmniejszyć ryzyko nawrotu i przerzutów u pacjentów z agresywnymi nowotworami głowy i szyi.
Cytowanie: Jeong, E., Kim, H.L., Park, S. et al. HERC1 oncogene enhances stemness and tumorigenic potential in CD44+-derived organoids of head and neck squamous cell carcinoma through IL-6/STAT3 signaling. Oncogene 45, 1840–1855 (2026). https://doi.org/10.1038/s41388-026-03725-9
Słowa kluczowe: rak głowy i szyi, komórki nowotworowe macierzyste, mikrośrodowisko guza, oporność na chemioterapię, sygnalizacja IL-6 STAT3