Clear Sky Science · zh
NIR-II 触发的尖端局部增强等离子体催化:用于骨科植入物缺氧生物膜清除的策略
为什么顽固的植入物感染很重要
当患者接受金属螺钉、钢板或关节置换时,肉眼看不见的细菌群落可能在表面悄然形成黏性堡垒,称为生物膜。这些生物膜对抗生素和热量具有抵抗力,常常迫使患者承受反复手术和长期住院。该研究描述了一种用于钛骨植入物的新型智能涂层,利用能深层穿透的近红外 II 区(NIR‑II)光既拆除这些细菌据点,又促进周围骨组织生长,旨在让植入物更安全、更耐用。
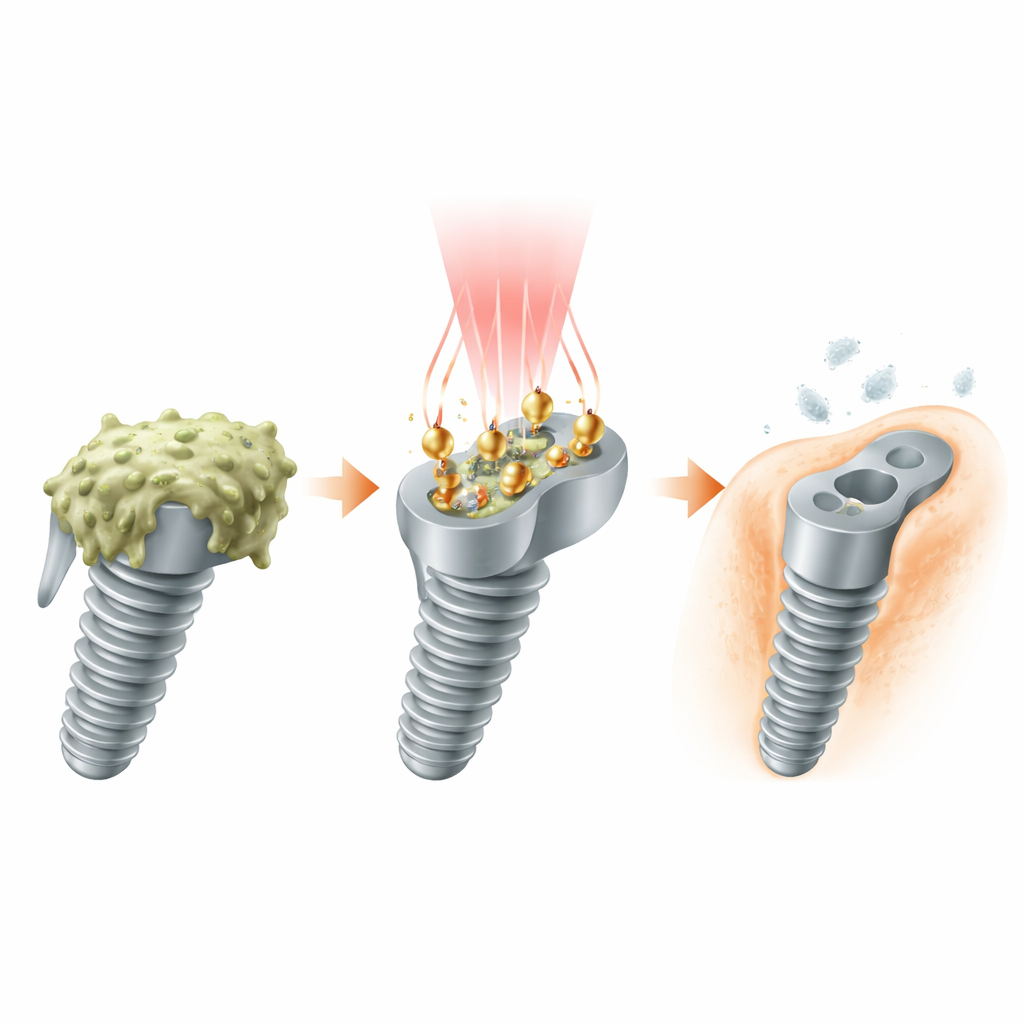
由光驱动的清理小队
研究人员设计了由金和铂构成的微小“工人”颗粒,安置在植入物表面。每个颗粒呈金双端金字塔形,尖端点缀着铂纳米点。这一设计不仅是外观考虑:它将颗粒调谐到对一段特殊波段——NIR‑II 光敏感,这种光比可见光更能有效穿透体组织。当 NIR‑II 激光照射到涂层植入物时,金–铂结构吸收光能并将其转化为热能和高能电子,使表面成为一个光激活的清洁场,直击细菌藏匿之处。
从光到显微“剪刀”
在合适条件下,受激颗粒会表现得像人工酶。配合少量过氧化氢,它们会产生高度活性的羟基自由基——寿命短暂的化学“剪刀”,攻击维系生物膜的分子。铂尖端的金结构有助于分离并引导光生电荷,防止正负电荷互相抵消,从而使反应更高效。结果是,植入物表面在温和升温的同时持续生成自由基,割裂细菌的保护网并削弱其细胞膜,即便在低氧环境下——许多其他光疗法难以奏效的情形——也能发挥作用。
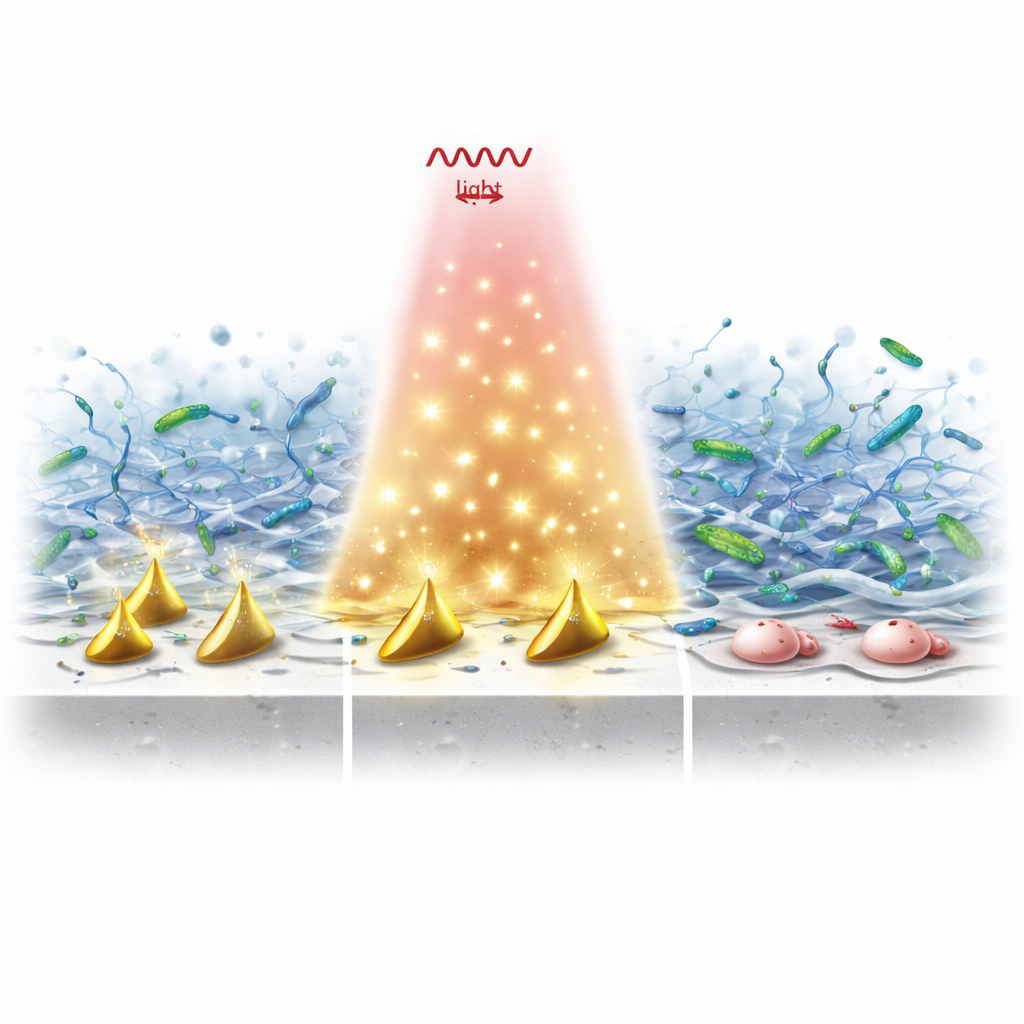
破除黏液护盾并杀灭细菌
在体外实验中,涂有这些颗粒并经 NIR‑II 照射的植入物相比裸钛显示出细菌存活率显著下降。热效应与自由基的双重作用不仅杀死游离微生物:它还通过切割胞外 DNA、在细菌壁上打孔、使重要蛋白外泄并压垮其内源性抗氧化防御,破坏成熟生物膜。即便氧气稀缺—这是长期感染周围常见的情况—该系统仍能持续产生足够的活性物种,破坏生物膜支架及其内部受保护的细菌。
不仅杀菌,还助力骨再生
因为植入物必须与骨牢固结合才能成功,团队在纳米颗粒层上加入了一段短肽,称为 RGDC。该肽模拟体内天然的粘附信号,为成骨细胞提供附着点。在细胞培养中,相较于裸钛,更多的成骨前体细胞在修饰表面上附着、铺展并增殖。随着时间推移,这些细胞启动了与构建骨基质和矿化相关的基因表达。在带有感染性骨缺损的大鼠模型中,涂层植入物不仅抑制了感染和炎症,还显示出更多新骨贴合金属生长,表明与骨骼的整合更好。
迈向更智能、更安全的骨科植入物
总体而言,该研究展示了一种策略,使外科植入的金属可以兼具可控治疗装置的功能:体外短时照射不可见光即可激活涂层,通过化学与热学手段瓦解生物膜,同时对周围组织保持温和。与此同时,表面化学有助于成骨细胞定殖并修复受损区域。对于患者而言,这类对光响应的、抗菌且有利于骨愈合的涂层日后可能减少重复手术和长期抗生素治疗的需要,让我们更接近能够自我防护并协助机体愈合的植入物。
引用: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
关键词: 骨科植入物, 细菌生物膜, 近红外光, 等离子纳米酶, 骨再生