Clear Sky Science · fr
Catalyse plasmonique déclenchée par le NIR‑II avec renforcement localisé aux pointes : une stratégie pour l’éradication des biofilms hypoxiques sur implants orthopédiques
Pourquoi les infections tenaces d’implants sont importantes
Lorsque des personnes reçoivent des vis, des plaques métalliques ou des prothèses articulaires, des colonies invisibles de bactéries peuvent progressivement former des forteresses visqueuses, appelées biofilms, à la surface. Ces biofilms résistent aux antibiotiques et à la chaleur, forçant souvent les patients à subir des interventions répétées et de longs séjours hospitaliers. Cette étude décrit un nouveau type de revêtement intelligent pour implants osseux en titane qui utilise la lumière proche infrarouge de grande pénétration (NIR‑II) pour à la fois démanteler ces bastions bactériens et favoriser la croissance osseuse environnante, dans le but de rendre les implants plus sûrs et plus durables.
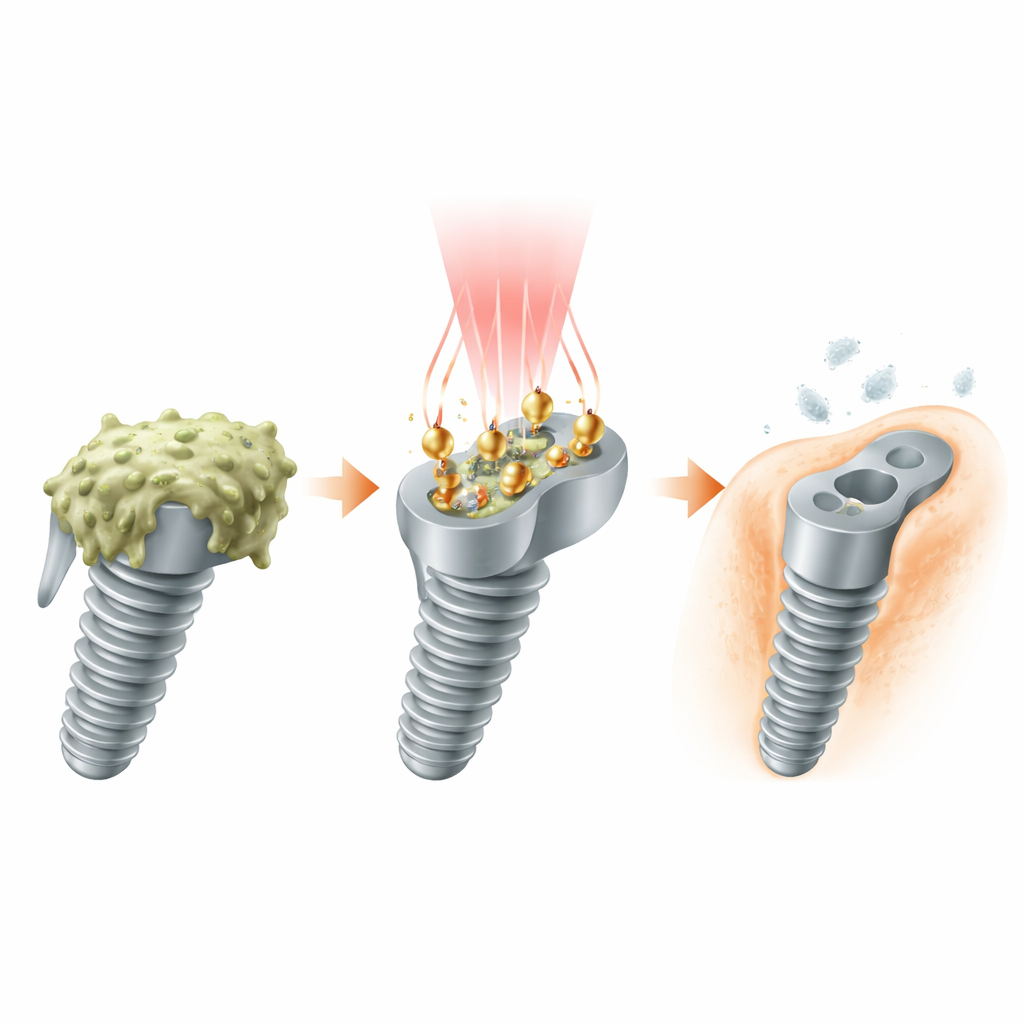
Une équipe de nettoyage alimentée par la lumière
Les chercheurs ont conçu de minuscules particules « ouvrières » en or et en platine qui reposent à la surface de l’implant. Chaque particule a la forme d’une double pyramide d’or avec une dispersion de points de platine à ses extrémités. Ce design n’est pas purement esthétique : il accorde les particules pour qu’elles réagissent à une fenêtre lumineuse particulière, le NIR‑II, qui traverse les tissus corporels plus efficacement que la lumière visible. Lorsqu’un laser NIR‑II éclaire l’implant revêtu, les structures or‑platine absorbent la lumière et la convertissent à la fois en chaleur et en électrons énergétiques, transformant la surface en un champ de nettoyage activé par la lumière qui cible les bactéries là où elles se cachent.
De la lumière à des « ciseaux » microscopiques
Dans de bonnes conditions, les particules énergisées agissent comme des enzymes artificielles. En présence d’une faible quantité de peroxyde d’hydrogène, elles génèrent des radicaux hydroxyles hautement réactifs — des « ciseaux » chimiques de courte durée qui attaquent les molécules maintenant les biofilms. La forme dorée à pointes de platine aide à séparer et à guider les charges chaudes créées par la lumière, évitant qu’elles ne s’annihilent mutuellement et rendant la réaction beaucoup plus efficace. En conséquence, la surface de l’implant chauffe modérément tout en produisant en continu des radicaux qui déchirent la matrice protectrice des biofilms et fragilisent les membranes bactériennes, même dans des environnements pauvres en oxygène où bien d’autres traitements à base de lumière peinent à fonctionner.
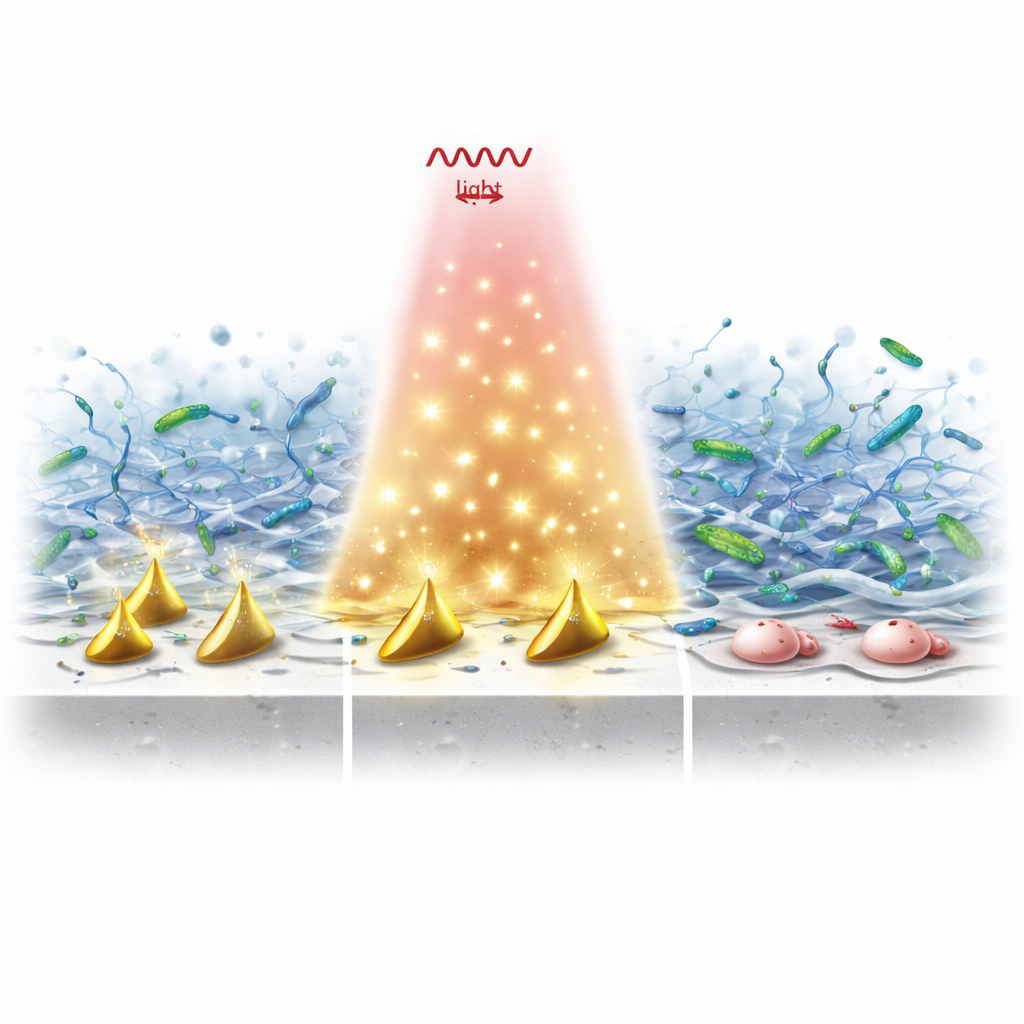
Perforer le bouclier visqueux et tuer les bactéries
En essais de laboratoire, les implants recouverts de ces particules puis exposés à la lumière NIR‑II ont montré une chute spectaculaire de la survie bactérienne comparé au titane nu. L’action double de la chaleur et des radicaux a fait plus que tuer les microbes en suspension : elle a perturbé les biofilms matures en coupant leur ADN extracellulaire, en perforant les parois bactériennes, en provoquant des fuites de protéines vitales et en submergeant leurs défenses antioxydantes internes. Même lorsque l’oxygène était rare — condition typique des infections anciennes — le système continuait de produire suffisamment d’espèces réactives pour détruire à la fois l’échafaudage du biofilm et les bactéries qu’il protégeait.
Aider l’os à repousser, pas seulement tuer les germes
Parce qu’un implant doit s’intégrer fermement à l’os pour réussir, l’équipe a ajouté un court peptide, appelé RGDC, à la couche de nanoparticules. Ce peptide mime des signaux d’adhésion naturels dans le corps, offrant aux cellules ostéogéniques un point d’accroche. En culture cellulaire, davantage de précurseurs osseux se sont attachés, étalés et multipliés sur les surfaces modifiées que sur le titane nu. Avec le temps, ces cellules ont activé des gènes associés à la synthèse de la matrice osseuse et au dépôt de minéraux. Chez des rats porteurs de défauts osseux infectés, les implants revêtus ont non seulement supprimé l’infection et l’inflammation, mais ont aussi montré davantage de nouveau tissu osseux se formant étroitement autour du métal, indiquant une meilleure intégration au squelette.
Vers des implants osseux plus intelligents et plus sûrs
Dans l’ensemble, l’étude démontre une stratégie dans laquelle l’implant métallique du chirurgien peut faire office d’appareil thérapeutique contrôlable : une brève exposition à une lumière invisible depuis l’extérieur du corps active le revêtement pour démanteler chimiquement et thermiquement les biofilms tout en restant suffisamment doux pour les tissus environnants. Parallèlement, la chimie de surface encourage les cellules osseuses à coloniser et à reconstruire les zones lésées. Pour les patients, de tels revêtements réactifs à la lumière, antibactériens et favorables à l’os pourraient un jour réduire le besoin d’interventions répétées et de longues cures d’antibiotiques, nous rapprochant d’implants capables de se défendre tout en aidant le corps à guérir.
Citation: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
Mots-clés: implants orthopédiques, biofilms bactériens, lumière proche infrarouge, nanozymes plasmoniques, régénération osseuse