Clear Sky Science · pl
Kataliza plazmoniczna wywołana w NIR‑II z lokalnym wzmocnieniem na końcach: strategia zwalczania biofilmów w warunkach hipoksji na implantach ortopedycznych
Dlaczego uporczywe zakażenia implantów mają znaczenie
Gdy pacjentom wszczepia się metalowe śruby, płytki czy endoprotezy, niewidoczne kolonie bakterii mogą po cichu tworzyć śliskie forty — tzw. biofilmy — na powierzchni. Biofilmy opierają się antybiotykom i spalaniu, często zmuszając pacjentów do powtarzanych operacji i długiego pobytu w szpitalu. W tym badaniu opisano nowy rodzaj inteligentnej powłoki na implanty tytanowe, która wykorzystuje głęboko przenikające światło bliskiej podczerwieni (NIR‑II), aby jednocześnie rozmontować te bakteryjne fortece i pobudzić wzrost otaczającej kości — celem jest zwiększenie bezpieczeństwa i trwałości implantów.
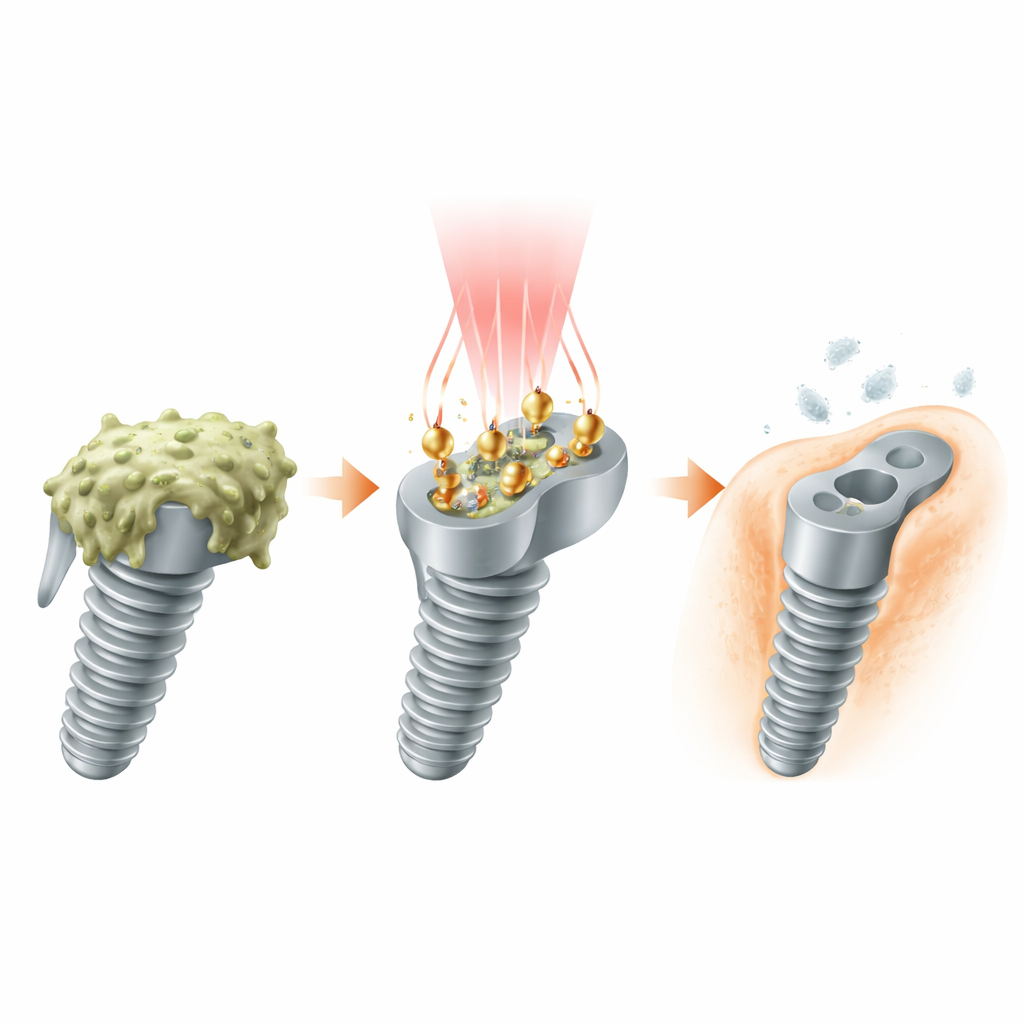
Zespół sprzątający zasilany światłem
Naukowcy zaprojektowali maleńkie „cząstki‑pracowniki” złożone ze złota i platyny, osadzone na powierzchni implantu. Każdy taki element ma kształt złotej, podwójnie zakończonej piramidy z drobnymi kropkami platyny na wierzchołkach. Ten układ nie jest tylko estetyczny: dostraja cząstki do specjalnego zakresu światła NIR‑II, które przechodzi przez tkanki lepiej niż światło widzialne. Gdy laser NIR‑II oświetla powłokę, struktury złoto–platynowe pochłaniają światło i przekształcają je zarówno w ciepło, jak i w energetyczne elektrony, zamieniając powierzchnię w aktywne pole czyszczące, które celuje w miejsca ukrycia bakterii.
Od światła do mikroskopijnych „nożyc”
W odpowiednich warunkach naenergetyzowane cząstki zachowują się jak sztuczne enzymy. W połączeniu z niewielką ilością nadtlenku wodoru generują wysoce reaktywne rodniki hydroksylowe — krótkotrwałe chemiczne „nożyce”, które atakują cząsteczki spajające biofilmy. Platynowe zakończenia złotego kształtu pomagają rozdzielać i kierować gorącymi ładunkami powstałymi pod wpływem światła, zapobiegając ich wzajemnemu anulowaniu i znacząco zwiększając wydajność reakcji. W rezultacie powierzchnia implantu nagrzewa się umiarkowanie, podczas gdy jednocześnie nieprzerwanie powstają rodniki, które rozrywają ochronną sieć bakterii i osłabiają ich błony, również w środowiskach ubogich w tlen, gdzie wiele innych terapii świetlnych zawodzi.
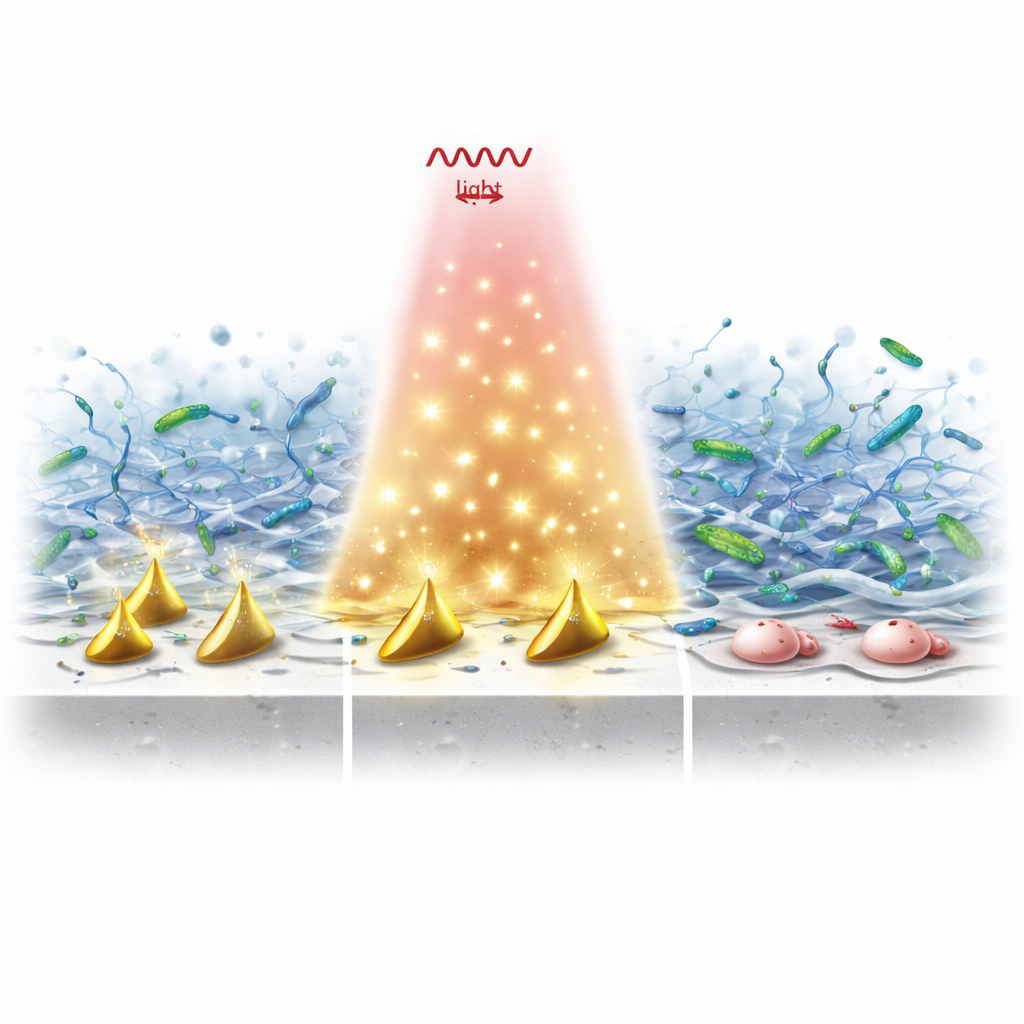
Przełamywanie tarczy ze śluzu i zabijanie bakterii
W testach laboratoryjnych implanty pokryte tymi cząstkami i następnie naświetlane NIR‑II wykazały dramatyczny spadek przeżywalności bakterii w porównaniu z gołym tytanem. Podwójne działanie ciepła i rodników zrobiło więcej niż zabić wolno pływające mikroby: zaburzyło dojrzałe biofilmy przez przecinanie ich zewnątrzkomórkowego DNA, dziurawienie ścian bakterii, wyciek niezbędnych białek i przeciążenie ich wewnętrznych mechanizmów antyoksydacyjnych. Nawet przy niedoborze tlenu — typowym wokół długotrwałych zakażeń — system nadal wytwarzał wystarczającą ilość reaktywnych cząstek, by zniszczyć zarówno rusztowanie biofilmu, jak i bakterie w nim chronione.
Wspomaganie odbudowy kości, nie tylko zabijanie zarazków
Ponieważ implant musi dobrze zrastać się z kością, zespół dodał do warstwy nanocząstek krótki peptyd o nazwie RGDC. Peptyd ten naśladuje naturalne sygnały adhezyjne w organizmie, dając komórkom tworzącym kość przyczepne miejsca. W hodowlach komórkowych więcej prekursorów osteoblastów przylegało, rozpostarło się i mnożyło na zmodyfikowanych powierzchniach niż na gołym tytanie. Z czasem komórki te włączały geny związane z budową macierzy kostnej i odkładaniem minerałów. U szczurów z zakażonymi ubytkami kostnymi powlekane implanty nie tylko hamowały infekcję i stan zapalny, lecz również wykazywały większe tworzenie nowej kości przylegającej ściśle do metalu, co wskazuje na lepszą integrację z układem szkieletowym.
W kierunku inteligentniejszych, bezpieczniejszych implantów kostnych
Podsumowując, badanie demonstruje strategię, w której metalowy implant chirurga może pełnić podwójną rolę jako kontrolowane urządzenie terapeutyczne: krótka dawka niewidzialnego światła z zewnątrz aktywuje powłokę do chemicznego i termicznego rozkładania biofilmów, pozostając jednocześnie wystarczająco łagodna dla okolicznych tkanek. Równocześnie chemia powierzchni sprzyja kolonizacji przez komórki kostne i odbudowie uszkodzonych obszarów. Dla pacjentów takie światłoczułe, zwalczające bakterie i przyjazne kości powłoki mogłyby pewnego dnia zmniejszyć potrzebę powtórnych operacji i długich kursów antybiotyków, przybliżając nas do implantów, które same się bronią, jednocześnie wspomagając gojenie organizmu.
Cytowanie: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
Słowa kluczowe: implanty ortopedyczne, biofilmy bakteryjne, światło bliskiej podczerwieni, plazmoniczne nanozymy, regeneracja kości