Clear Sky Science · ar
التحفيز البلازمويني المستحث بـ NIR-II مع تعزيز موضعي عند الطرف: استراتيجية للقضاء على الأغشية الحيوية ناقصة الأكسجين على زرعات العظام
لماذا تهم عدوى الزرعات المستعصية
عندما يتلقى الناس مساميرًا أو صفائح أو بدائل مفصلية معدنية، يمكن لمستعمرات بكتيرية غير مرئية أن تبني بهدوء حصونًا مخاطية تُسمى الأغشية الحيوية على السطح. تهمل هذه الأغشية المضادات الحيوية والحرارة، وغالبًا ما تضطر المرضى لتحمّل عمليات جراحية متكررة وإقامات طويلة في المستشفى. تصف هذه الدراسة طلاءً ذكيًا جديدًا لزرعات التيتانيوم العظمية يستخدم ضوءًا قريبًا من تحت الأحمر ذو اختراق عميق لتفكيك معاقل البكتيريا هذه وتشجيع نمو العظم المحيط، بهدف جعل الزرعات أكثر أمانًا وطول عمر.
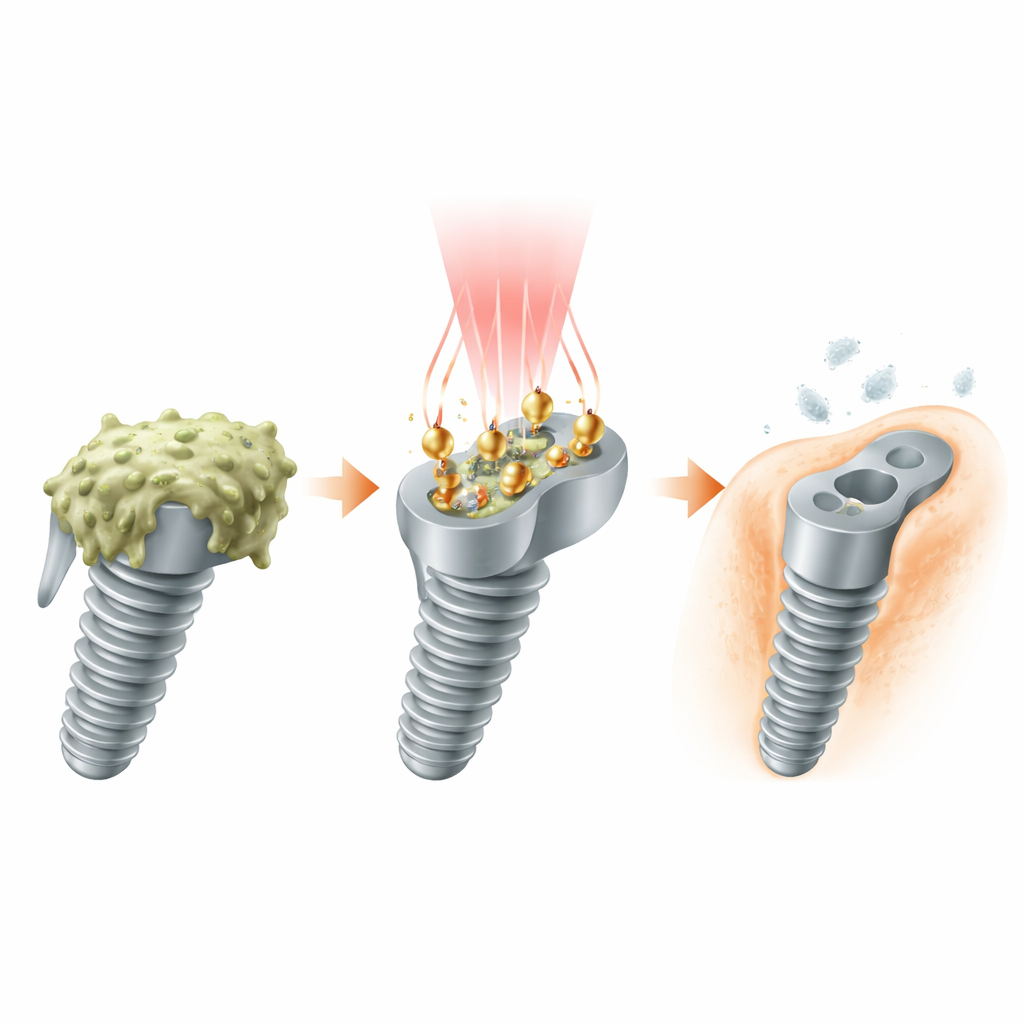
فرقة تنظيف تعمل بالضوء
صمم الباحثون جسيمات «عاملة» دقيقة من الذهب والبلاتين تستقر على سطح الزرع. كل جسيم على شكل هرمين مزدوجين من الذهب مع نقاط بلاتينية متناثرة عند أطرافه. هذا التصميم ليس تجميليًا فحسب: إنه يضبط استجابة الجسيمات لنافذة ضوئية خاصة تسمى NIR‑II، والتي يمكنها المرور عبر أنسجة الجسم بكفاءة أكبر من الضوء المرئي. عندما يسقط ليزر NIR‑II على الزرع المطلي، تمتص التركيبات الذهبية‑البلاتينية الضوء وتحوّله إلى حرارة وإلكترونات عالية الطاقة، محوّلة السطح إلى مجال تنظيف مُفعل بالضوء يستهدف البكتيريا حيث تختبئ.
من الضوء إلى «مقصات» مجهرية
في الظروف المناسبة، تتصرف الجسيمات المشحونة كإنزيمات صناعية. وبالتعاون مع كمية صغيرة من بيروكسيد الهيدروجين، تولد جذور هيدروكسيل نشطة للغاية—«مقصات» كيميائية قصيرة العمر تهاجم الجزيئات التي تربط الأغشية الحيوية معًا. يساعد الطرف البلاتيني لشكل الذهب في فصل وتوجيه الشحنات الساخنة الناتجة عن الضوء، مانعًا إلغاؤها بعضها البعض وجاعلًا التفاعل أكثر كفاءة بكثير. نتيجة لذلك، يسخن سطح الزرع بشكل معتدل بينما يستمر في إنتاج الجذور التي تقطع شبكة حماية البكتيريا وتضعف أغشيتها، حتى في بيئات منخفضة الأكسجين حيث تتعثر العديد من العلاجات الضوئية الأخرى.
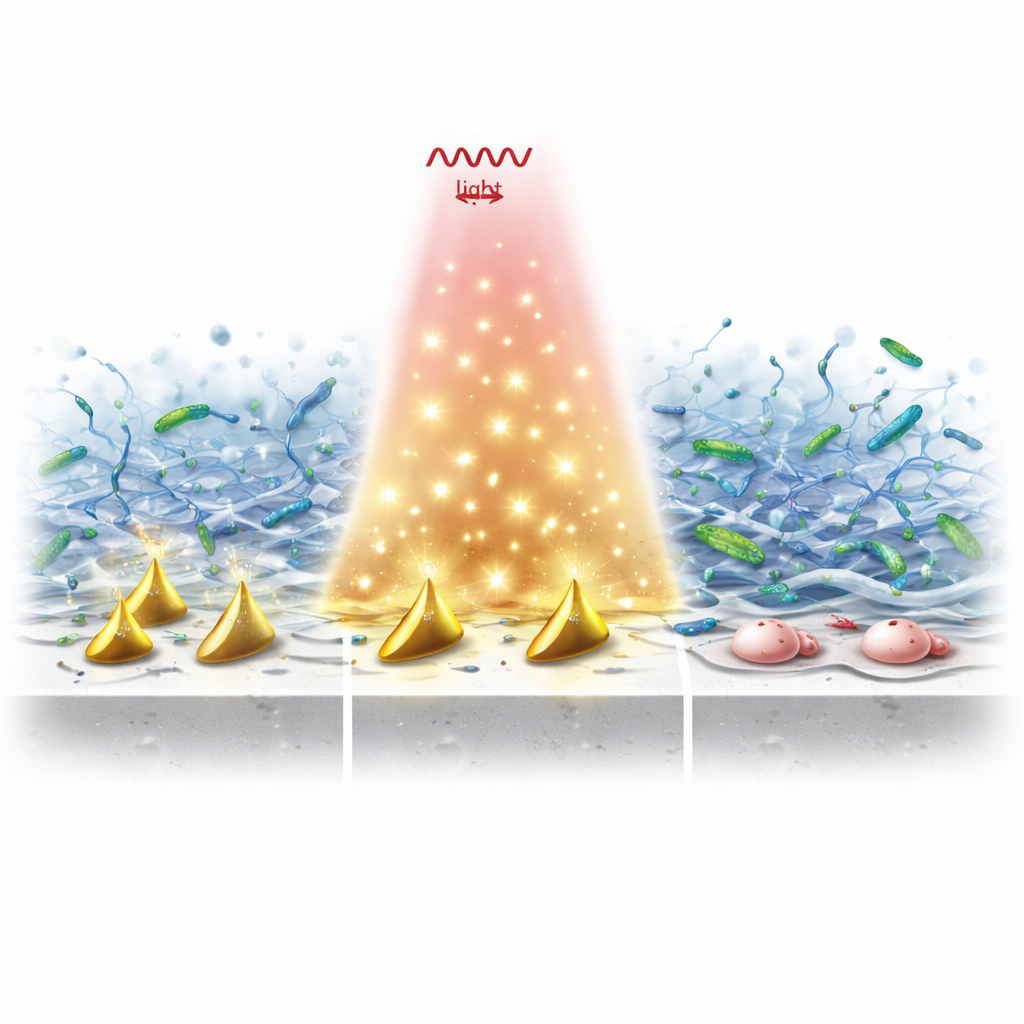
تفكيك درع المخاط وقتل البكتيريا
في تجارب مخبرية، أظهرت الزرعات المطلية بهذه الجسيمات والتي تعرضت لاحقًا لضوء NIR‑II انخفاضًا حادًا في بقاء البكتيريا مقارنة بالتيتانيوم العاري. لم يقتصر العمل المزدوج للدفء والجذور على قتل الكائنات الدقيقة الطافية فقط: بل فتك بالأغشية الحيوية الناضجة عبر قطع الحمض النووي خارج الخلية، وثقب جدران البكتيريا، وتسريب البروتينات الحيوية، وإرهاق دفاعاتها المضادة للأكسدة الداخلية. حتى عندما كان الأكسجين نادرًا—وهو ظرف شائع حول العدوى المزمنة—استمر النظام في إنتاج ما يكفي من الأنواع التفاعلية لتدمير كل من سقالة الأغشية الحيوية والبكتيريا المحمية داخلها.
مساعدة العظم على النمو من جديد، وليس مجرد قتل الجراثيم
لأن الزرع يجب أن يتصلب مع العظم لينجح، أضاف الفريق ببتيدًا قصيرًا يُدعى RGDC إلى طبقة الجسيمات النانوية. يحاكي هذا الببتيد إشارات الالتصاق الطبيعية في الجسم، مانحًا خلايا تكوّن العظم نقطة تمسك. في زراعة الخلايا، التزمت المزيد من خلايا السلف العظمية، وانتشرت وتكاثرت على الأسطح المعدلة أكثر مما حصل على التيتانيوم العاري. ومع مرور الوقت، شغّلت هذه الخلايا جينات مرتبطة ببناء مصفوفة العظم وترسيب المعادن. في فئران ذات عيوب عظمية مصابة، لم تكبح الزرعات المطلية العدوى والالتهاب فقط، بل أظهرت أيضًا تكوّن عظم جديد أكثر تماسًا حول المعدن، مما يشير إلى تكامل أفضل مع الهيكل العظمي.
نحو زرعات عظمية أذكى وأكثر أمانًا
بشكل عام، تُظهر الدراسة استراتيجية يمكن من خلالها أن يعمل زرع الجراح المعدني كجهاز علاج قابل للتحكم: جرعة قصيرة من ضوء غير مرئي من خارج الجسم تُفعّل الطلاء لتفكيك الأغشية الحيوية كيميائيًا وحراريًا مع البقاء لطيفًا بما يكفي على الأنسجة المحيطة. وفي الوقت نفسه، تشجع كيمياء السطح خلايا العظم على الاستيطان وإعادة بناء المناطق التالفة. بالنسبة للمرضى، قد تقلل مثل هذه الطلاءات المستجيبة للضوء والمكافحة للبكتيريا والصديقة للعظم يومًا ما من الحاجة إلى عمليات جراحية متكررة ودورات طويلة من المضادات الحيوية، وتقربنا من زرعات تدافع عن نفسها بينما تساعد الجسم على الشفاء.
الاستشهاد: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
الكلمات المفتاحية: زرعات عظمية, الأغشية الحيوية البكتيرية, الضوء القريب من تحت الأحمر, نانوإنزيمات بلازمونية, تجدد العظم