Clear Sky Science · de
NIR-II-aktivierte plasmonische Katalyse mit spitzenlokalisierter Verstärkung: Eine Strategie zur Eradikation hypoxischer Biofilme an orthopädischen Implantaten
Warum hartnäckige Implantatinfektionen wichtig sind
Wenn Menschen Metall-Schrauben, -Platten oder Gelenkersatz erhalten, können sich unsichtbare Bakterienkolonien stillschweigend schleimige Festungen auf der Oberfläche bilden, sogenannte Biofilme. Diese Biofilme sind gegenüber Antibiotika und Hitze oft resistent, was Patienten wiederholte Operationen und lange Krankenhausaufenthalte aufzwingt. Die vorliegende Studie beschreibt eine neue Art intelligenter Beschichtung für Titan-Knochenimplantate, die tief eindringendes Nahinfrarotlicht (NIR‑II) nutzt, um sowohl diese bakteriellen Stützpunkte zu demontieren als auch das umgebende Knochenwachstum zu fördern — mit dem Ziel, Implantate sicherer und langlebiger zu machen.
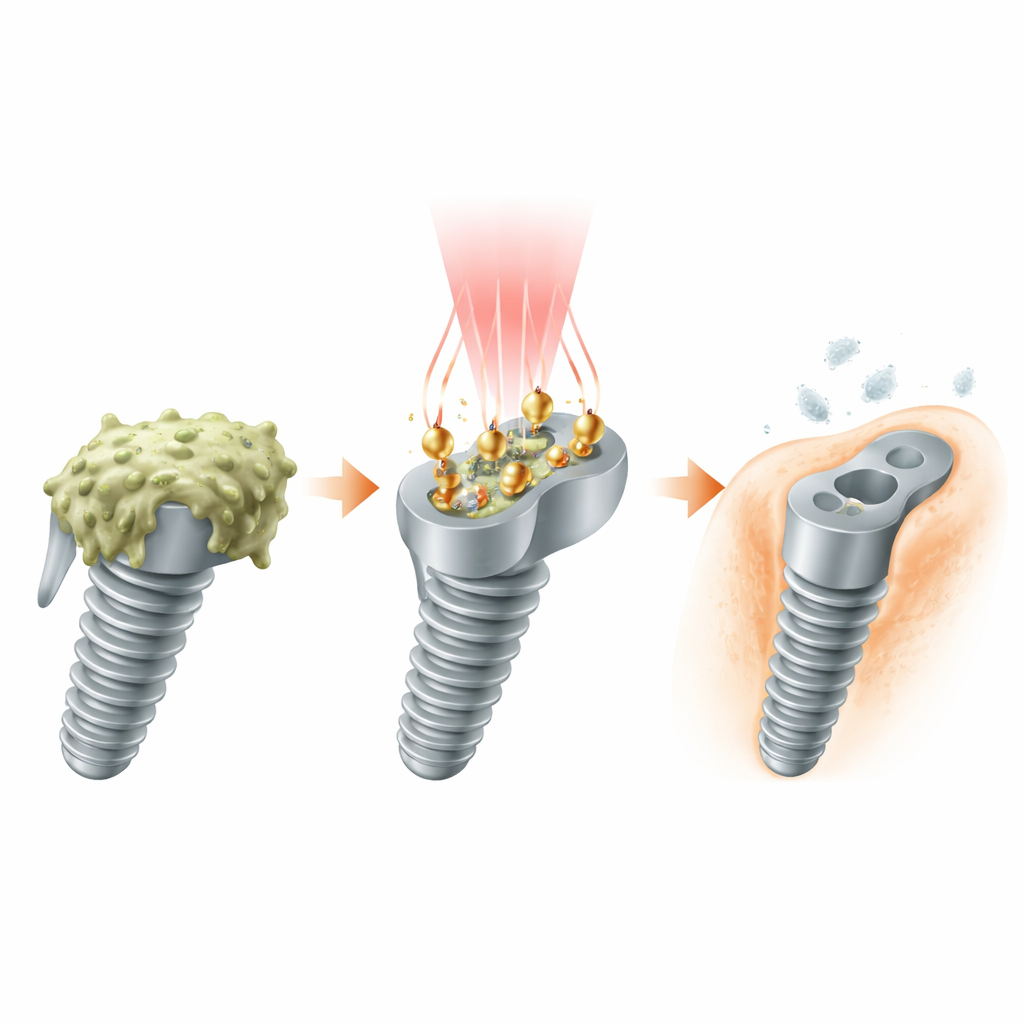
Eine lichtbetriebene Aufräumtruppe
Die Forschenden entwickelten winzige „Arbeiter“-Partikel aus Gold und Platin, die auf der Implantatoberfläche sitzen. Jeder Arbeiter hat die Form einer goldenen doppeltspitzigen Pyramide mit vereinzelten Platinnanodots an den Spitzen. Dieses Design ist nicht nur ästhetisch: Es bringt die Partikel dazu, auf ein spezielles Lichtspektrum, das NIR‑II-Fenster, zu reagieren, das Gewebe effizienter durchdringt als sichtbares Licht. Wenn ein NIR‑II-Laser auf das beschichtete Implantat scheint, absorbieren die Gold–Platin-Strukturen das Licht und wandeln es in Wärme und energiereiche Elektronen um, wodurch die Oberfläche zu einem lichtaktivierten Reinigungsfeld wird, das Bakterien an ihren Verstecken angreift.
Von Licht zu mikroskopischen „Scheren“
Unter den richtigen Bedingungen verhalten sich die angeregten Partikel wie künstliche Enzyme. In Kombination mit einer geringen Menge Wasserstoffperoxid erzeugen sie hochreaktive Hydroxylradikale — kurzlebige chemische „Scheren“, die die Moleküle angreifen, die Biofilme zusammenhalten. Die platinierten Spitzen der goldenen Form helfen, die heißen Ladungen, die durch Licht entstehen, zu separieren und zu lenken, sodass sie sich nicht gegenseitig auslöschen, was die Reaktion deutlich effizienter macht. Infolgedessen erwärmt sich die Implantatoberfläche moderat, während kontinuierlich Radikale produziert werden, die das schützende Netz der Bakterien zerschneiden und ihre Membranen schwächen — selbst in sauerstoffarmen Umgebungen, in denen viele andere lichtbasierte Therapien an ihre Grenzen stoßen.
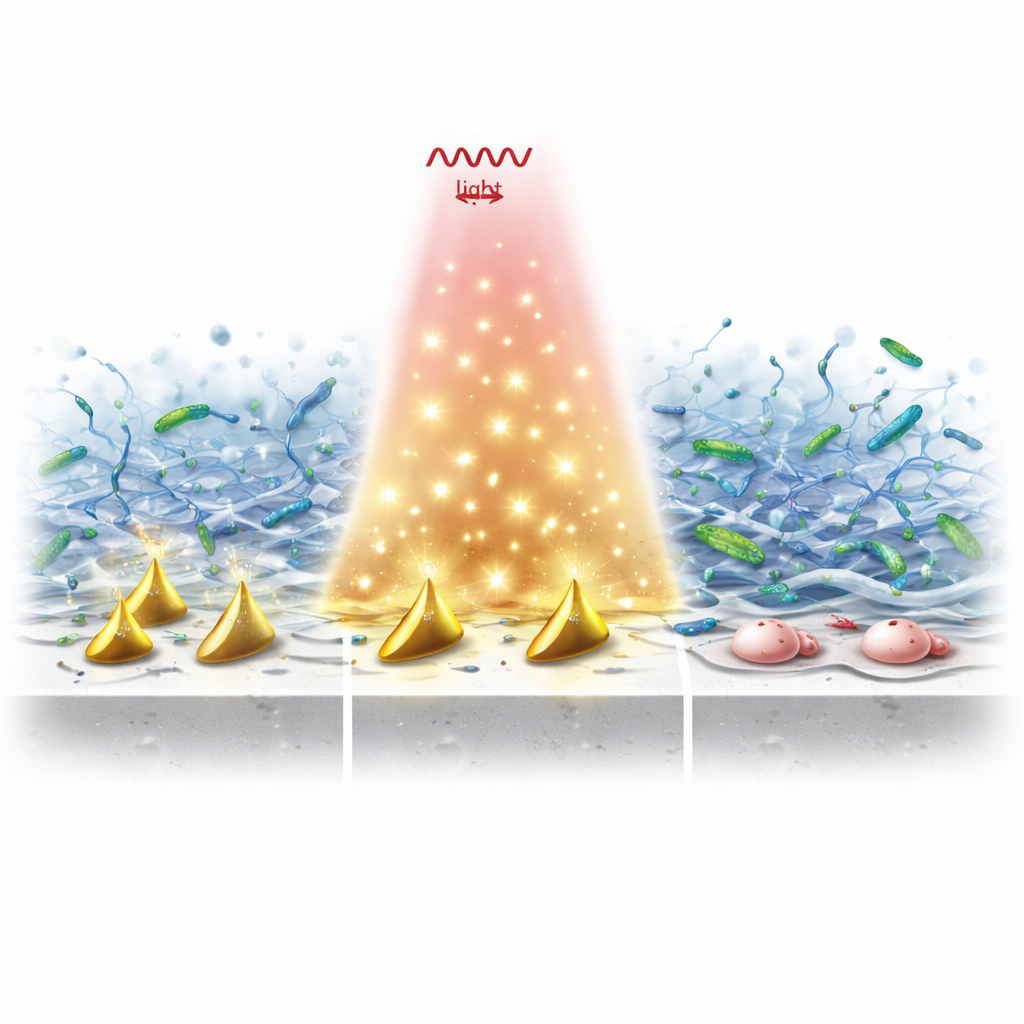
Den Schleimschild durchbrechen und die Bakterien töten
In Laborversuchen zeigten Implantate, die mit diesen Partikeln beschichtet und dann NIR‑II-Licht ausgesetzt wurden, einen dramatischen Rückgang des bakteriellen Überlebens im Vergleich zu blankem Titan. Die doppelte Wirkung von Wärme und Radikalen bewirkte mehr als das Abtöten frei schwimmender Mikrobenn: Sie störte ausgereifte Biofilme, indem sie extrazelluläre DNA zerschnitt, Löcher in bakterielle Zellwände stanzte, lebenswichtige Proteine auslaufen ließ und die inneren antioxidativen Abwehrsysteme der Bakterien überforderte. Selbst bei Sauerstoffmangel — ein typischer Zustand bei langwierigen Infektionen — produzierte das System weiterhin ausreichend reaktive Spezies, um sowohl das Biofilm-Gerüst als auch die darin geschützten Bakterien zu zerstören.
Knochenneubildung fördern, nicht nur Keime abtöten
Weil ein Implantat fest mit dem Knochen verwachsen muss, ergänzte das Team die Nanopartikel‑Schicht mit einem kurzen Peptid namens RGDC. Dieses Peptid imitiert natürliche Haftsignale im Körper und bietet knochenbildenden Zellen Ankerpunkte. In Zellkulturen hafteten sich mehr Knochenvorläuferzellen an, breiteten sich aus und vermehrten sich auf den modifizierten Oberflächen stärker als auf blankem Titan. Im Laufe der Zeit schalteten diese Zellen Gene ein, die mit dem Aufbau der Knochenmatrix und der Mineralisierung verbunden sind. Bei Ratten mit infizierten Knochendefekten unterdrückten die beschichteten Implantate nicht nur Infektion und Entzündung, sondern zeigten auch vermehrte Neubildung von Knochen, der sich eng um das Metall bildete — ein Hinweis auf bessere Integration mit dem Skelett.
Auf dem Weg zu intelligenteren, sichereren Knochenimplantaten
Insgesamt demonstriert die Studie eine Strategie, bei der das Metallimplantat des Chirurgen zugleich als kontrollierbares Behandlungsgerät fungieren kann: Eine kurze Dosis unsichtbaren Lichts von außerhalb des Körpers aktiviert die Beschichtung, um Biofilme chemisch und thermisch zu demontieren, während sie zugleich sanft genug für das umliegende Gewebe bleibt. Gleichzeitig fördert die Oberflächenchemie die Besiedelung durch Knochenzellen und das Wiederaufbauen geschädigter Bereiche. Für Patientinnen und Patienten könnten solche lichtreaktiven, bakterienbekämpfenden und knochenfreundlichen Beschichtungen eines Tages die Notwendigkeit für wiederholte Operationen und lange Antibiotikatherapien reduzieren und uns Implantate näherbringen, die sich selbst verteidigen und gleichzeitig dem Körper beim Heilen helfen.
Zitation: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
Schlüsselwörter: orthopädische Implantate, bakterielle Biofilme, nahes Infrarotlicht, plasmonische Nanozyme, Knochenregeneration