Clear Sky Science · pt
Catálise plasmônica acionada por NIR‑II com reforço localizado nas pontas: uma estratégia para erradicação de biofilmes hipóxicos em implantes ortopédicos
Por que infecções persistentes em implantes importam
Quando pessoas recebem parafusos metálicos, placas ou próteses articulares, colônias invisíveis de bactérias podem formar silenciosamente fortalezas viscosas, chamadas biofilmes, na superfície. Esses biofilmes resistem a antibióticos e ao calor, frequentemente forçando pacientes a passar por cirurgias repetidas e longas internações. Este estudo descreve um novo tipo de revestimento inteligente para implantes ósseos de titânio que usa luz no infravermelho próximo de alta penetração (NIR‑II) para, ao mesmo tempo, desmontar essas fortalezas bacterianas e estimular o crescimento ósseo ao redor, com o objetivo de tornar os implantes mais seguros e duradouros.
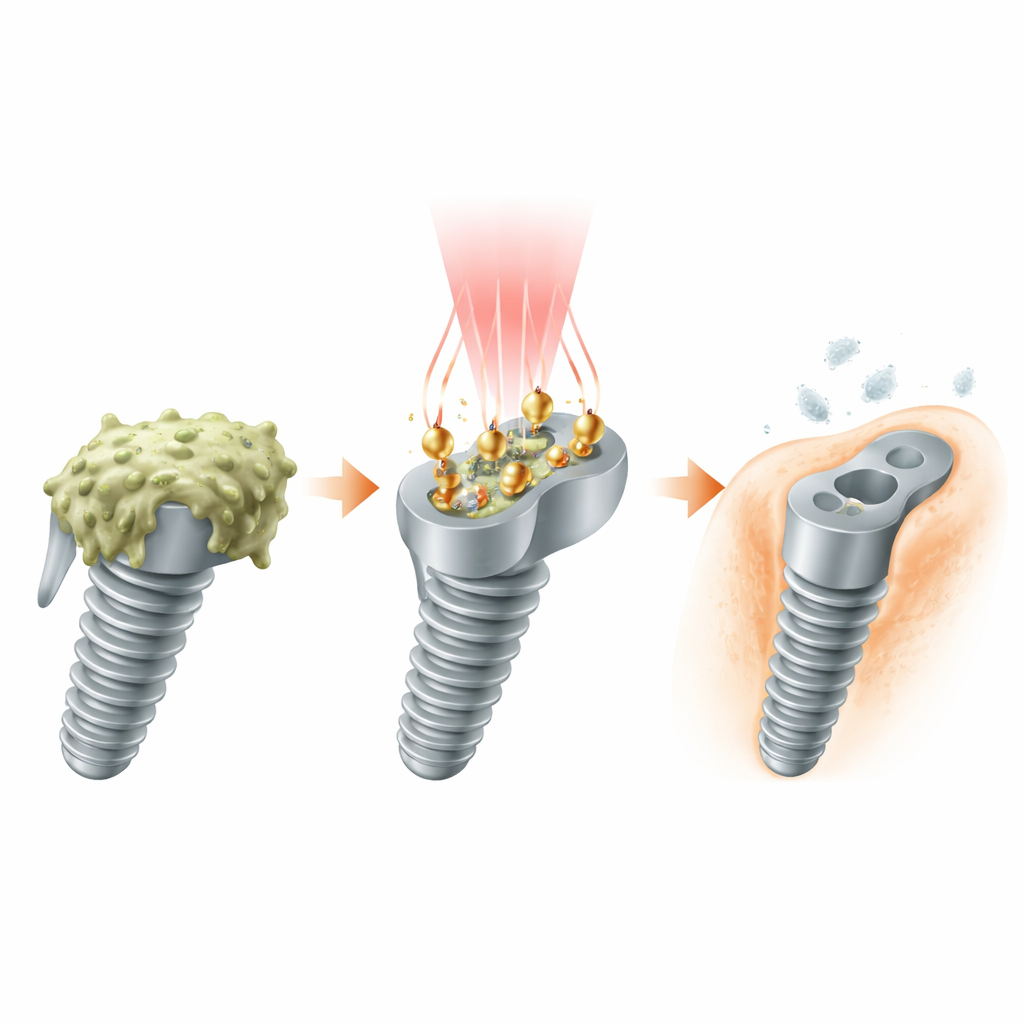
Uma equipe de limpeza acionada por luz
Os pesquisadores projetaram pequenas partículas “trabalhadoras” feitas de ouro e platina que se assentam na superfície do implante. Cada partícula tem a forma de uma pirâmide dupla de ouro com pontos de platina nas pontas. Esse desenho não é apenas estético: ele ajusta as partículas para responder a uma janela especial de luz, chamada NIR‑II, que consegue atravessar tecidos corporais com mais eficiência do que a luz visível. Quando um laser NIR‑II incide sobre o implante revestido, as estruturas ouro–platina absorvem a luz e a convertem tanto em calor quanto em elétrons energéticos, transformando a superfície em um campo de limpeza ativado por luz que atinge as bactérias onde elas se escondem.
Da luz para “tesouras” microscópicas
Nas condições adequadas, as partículas energizadas atuam como enzimas artificiais. Em conjunto com uma pequena quantidade de peróxido de hidrogênio, elas geram radicais hidroxila altamente reativos—“tesouras” químicas de curta duração que atacam as moléculas que mantêm os biofilmes unidos. A ponta de platina na estrutura de ouro ajuda a separar e guiar as cargas quentes criadas pela luz, impedindo que se anulem e tornando a reação muito mais eficiente. Como resultado, a superfície do implante aquece de forma moderada enquanto produz continuamente radicais que cortam a malha protetora das bactérias e enfraquecem suas membranas, mesmo em ambientes pobres em oxigênio onde muitos outros tratamentos baseados em luz têm dificuldade.
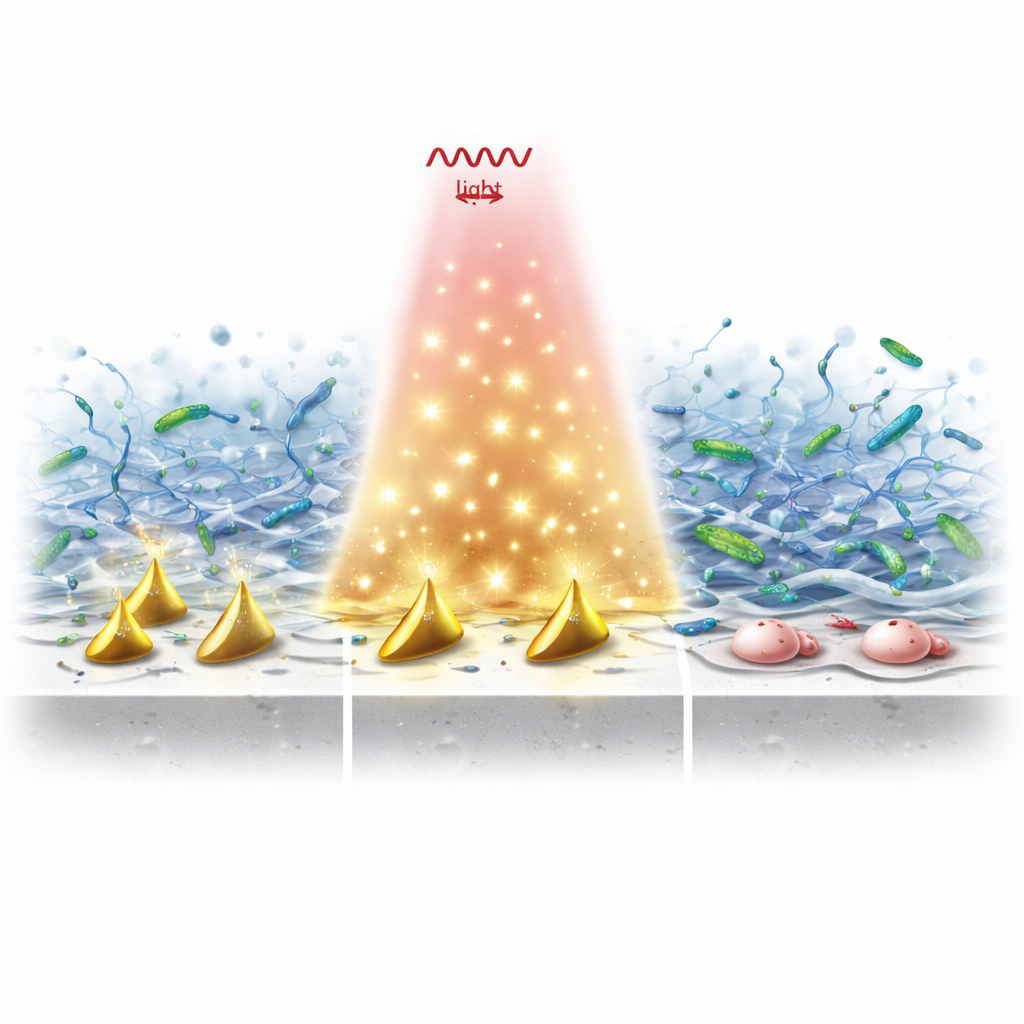
Romper o escudo viscoso e matar as bactérias
Em testes laboratoriais, implantes revestidos com essas partículas e então expostos à luz NIR‑II apresentaram uma queda dramática na sobrevivência bacteriana em comparação com titânio simples. A ação dupla de aquecimento e radicais fez mais do que matar microrganismos em suspensão: ela desorganizou biofilmes maduros ao cortar seu DNA extracelular, perfurar paredes bacterianas, provocar perda de proteínas vitais e sobrecarregar as defesas antioxidantes internas. Mesmo quando o oxigênio era escasso—condição típica em infecções de longa duração—o sistema continuou a gerar espécies reativas suficientes para destruir tanto o esqueleto do biofilme quanto as bactérias protegidas em seu interior.
Promover o crescimento ósseo, não apenas matar germes
Porque um implante precisa se integrar firmemente ao osso para ter sucesso, a equipe adicionou um peptídeo curto, chamado RGDC, à camada nanoparticulada. Esse peptídeo mimetiza sinais naturais de adesão no corpo, oferecendo às células formadoras de osso um ponto de ancoragem. Em cultura celular, mais células precursoras ósseas aderiram, espalharam‑se e multiplicaram‑se nas superfícies modificadas do que no titânio nu. Ao longo do tempo, essas células ativaram genes associados à construção da matriz óssea e ao depósito de minerais. Em ratos com defeitos ósseos infectados, os implantes revestidos não só suprimiram a infecção e a inflamação, como também apresentaram mais osso novo formando‑se firmemente ao redor do metal, indicando melhor integração com o esqueleto.
Rumo a implantes ósseos mais inteligentes e seguros
No conjunto, o estudo demonstra uma estratégia na qual o implante metálico do cirurgião pode duplicar como um dispositivo de tratamento controlável: uma breve dose de luz invisível de fora do corpo ativa o revestimento para desmontar quimicamente e termicamente os biofilmes, mantendo‑se suficientemente gentil para os tecidos circundantes. Ao mesmo tempo, a química de superfície incentiva células ósseas a colonizar e reconstruir áreas danificadas. Para os pacientes, tais revestimentos responsivos à luz, antibacterianos e favoráveis ao osso podem um dia reduzir a necessidade de cirurgias repetidas e longos ciclos de antibióticos, aproximando‑nos de implantes que se defendem enquanto ajudam o corpo a curar.
Citação: Sun, Y., Sheng, F., Liang, Y. et al. NIR-II-triggered plasmonic catalysis with tip-localized enhancement: a strategy for hypoxic biofilm eradication on orthopedic implants. Light Sci Appl 15, 204 (2026). https://doi.org/10.1038/s41377-026-02279-5
Palavras-chave: implantes ortopédicos, biofilmes bacterianos, luz no infravermelho próximo, nanozymes plasmônicos, regeneração óssea