Clear Sky Science · zh
OGT介导MEIS2的O-GlcNAc化并影响腭骨成骨发育
这项研究对面部生长为何重要
唇腭裂是最常见的先天性畸形之一,影响婴儿的口腔和面部。这会使喂养、语言以及日后牙齿健康变得更加困难,而目前临床上只能在出生后进行修复。该研究提出了一个更深层的问题:在胚胎腭骨形成的显微层面上,究竟发生了哪些错误?理解这些隐蔽过程是否有朝一日能帮助预防腭裂的发生?
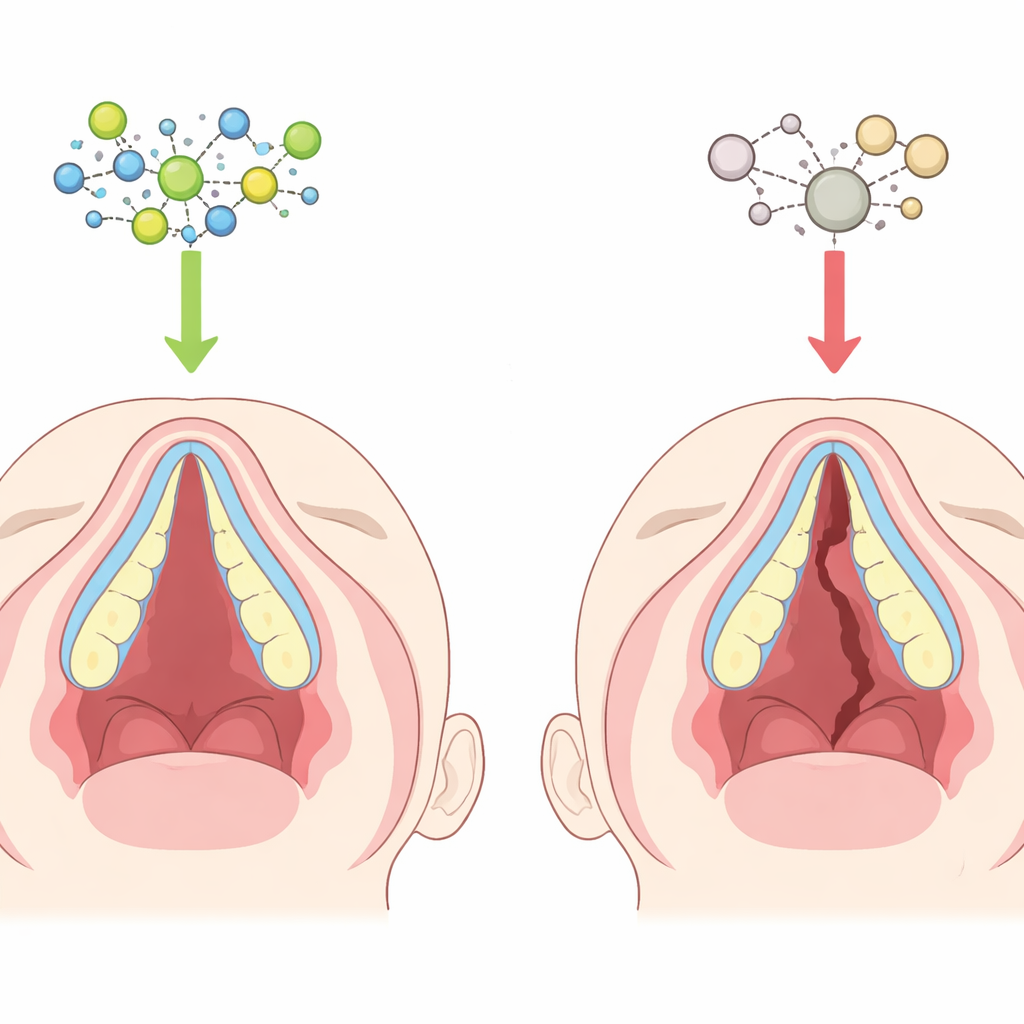
腭是如何正常成形的
在早期发育中,上颌两侧的两片组织向内生长,升起到舌侧并在中线相遇融合,形成口腔的顶部(腭)。在这些组织内,胚胎期的柔软细胞逐渐分化为生成硬腭的成骨细胞。如果这些组织未能正确生长、移动、相遇或矿化,就可能留下缺口,产生腭裂。腭的前部直接由软组织向骨组织转变而成,这一过程必须非常精确地把握时机。时间调控的细微紊乱可能导致腭被皮肤和黏膜覆盖,但却缺乏坚实的骨性支撑。
一个微小糖基标记的重大发育作用
作者关注一种称为O-GlcNAc的化学“标记”,这是一种细胞可附加到多种蛋白上的小糖,用以微调蛋白功能。单一酶O-GlcNAc转移酶(OGT)负责添加此标记,类似一个响应细胞营养与应激状态的分子交换台。在接受全反式维甲酸处理的小鼠胚胎中——这种化合物可可靠地诱发腭裂——研究团队发现发育中腭组织里的O-GlcNAc标记和OGT水平显著降低。这提示当此糖基标记系统被抑制时,腭可能难以形成正常的骨组织。
来自鱼类和人类腭细胞的证据
为检验该糖基标记对腭构建是否真正重要,研究者转向斑马鱼,其颅面发育在关键方面与哺乳动物相似。当在斑马鱼胚胎中阻断OGT或化学抑制O-GlcNAc时,鱼类在腭区出现类裂隙的比例显著上升,中部颅骨的矿化也变弱。补充额外的ogt基因材料可部分挽救这些缺陷,加强了O-GlcNAc与健康腭形成之间的联系。与此同时,团队使用了人胚腭间充质(HEPM)细胞——与形成人体硬腭的细胞相似。降低这些细胞中的OGT并未阻止其分裂,但削弱了它们向成骨细胞分化并沉积矿物质的能力,证实了糖基标记系统与成骨能力的直接关联。
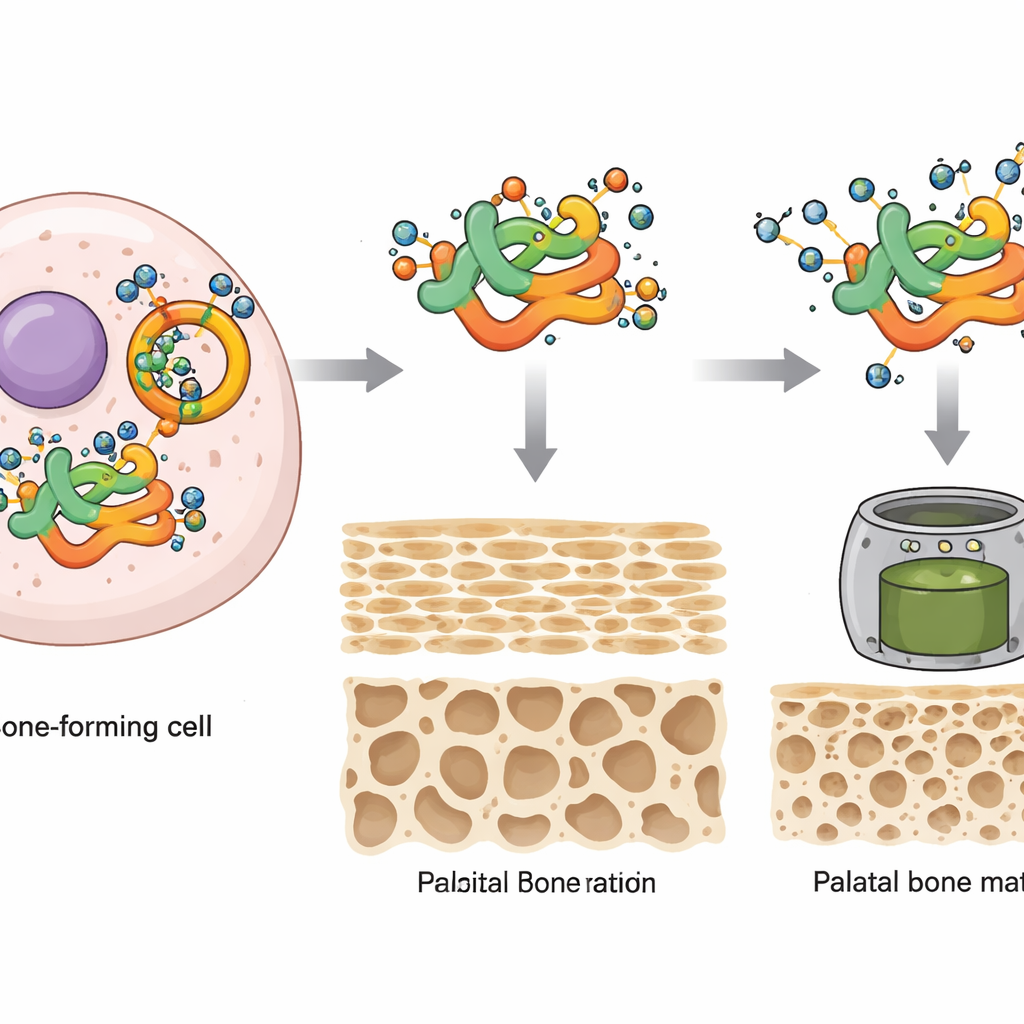
保护关键“建筑师”蛋白不被摧毁
研究进一步聚焦于特定蛋白MEIS2——一种已知对颅面发育至关重要的DNA结合因子,且在儿童中其突变与腭裂相关。作者发现MEIS2与OGT存在物理相互作用,并在特定氨基酸位点(哺乳动物中称为Ser237)携带O-GlcNAc标记。当该位点被改变以致无法被糖基化时,MEIS2失去了大部分糖修饰。缺乏适当的O-GlcNAc标记并未关闭其基因表达,而是导致MEIS2蛋白水平迅速下降,这是因为该蛋白更容易被细胞的泛素–蛋白酶体“碎纸机”标记并降解。因此,O-GlcNAc修饰充当了一层保护盾,稳定MEIS2并防止其过早被降解。
将这些机制与成骨基因连接起来
被稳定下来的MEIS2不仅仅是存在——它会启动其他基因。其一个重要靶基因是SHOX2,另一种在硬腭发育中被强烈牵涉的调控因子。团队显示MEIS2结合SHOX2基因的调控区并增强其活性,而OGT丧失或MEIS2糖基化位点突变则削弱了这种激活。在缺失OGT的HEPM细胞中,重新引入正常的MEIS2可以恢复成骨标志物和矿化沉积,但无法携带糖基的MEIS2变体则不能。在斑马鱼中,额外的meis2 mRNA能够拯救因ogt缺失引起的腭骨缺陷,而缺乏糖基位点的变体再次失败。这些实验共同勾勒出一条明确链条:OGT向MEIS2添加糖基,从而维持MEIS2的稳定性,进而激活SHOX2及其他成骨基因,使腭骨正常形成。
这对未来唇腭裂干预意味着什么
通俗地说,这项工作识别了一套显微层面的质量控制系统,帮助胚胎腭细胞让关键的“建筑师”蛋白在岗时间足够长,以建起坚固的口腔骨性顶盖。当添加糖基的酶OGT被削弱——无论是因遗传变化还是环境应激——MEIS2蛋白就会过早被剥夺并降解,成骨指令无法完全执行,从而增加腭裂的风险。尽管任何临床应用仍遥远,但理解这一OGT–MEIS2–SHOX2链条为思考基因、营养与化学暴露在面部发育中如何交互提供了新框架,并指出了未来可能用于更好诊断、预测甚至预防某些腭裂病例的分子靶点。
引用: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
关键词: 唇腭裂, 颅面发育, 翻译后修饰, O-GlcNAc修饰, MEIS2