Clear Sky Science · ar
إنزيم OGT يُوسّع O-GlcNAcylation لبروتين MEIS2 ويؤثر في تطور عظم الحنك
لماذا يهم هذا البحث للوجوه النامية
يُعد الحنك المشقوق واحدًا من أكثر العيوب الخِلقية شيوعًا التي تؤثر على أفواه ووجوه الأطفال. يمكن أن يعقّد الرضاعة، والكلام، وصحة الأسنان المستقبلية، واليوم يقتصر العلاج على ما بعد ظهور العيب. يطرح هذا البحث سؤالًا أعمق: ما الذي يخطئ على المستوى المجهرِي أثناء تكوّن عظام الحنك في الجنين، وهل قد يساعد فهم تلك العمليات الخفية يومًا ما في منع تشكّل الشقوق من الأساس؟
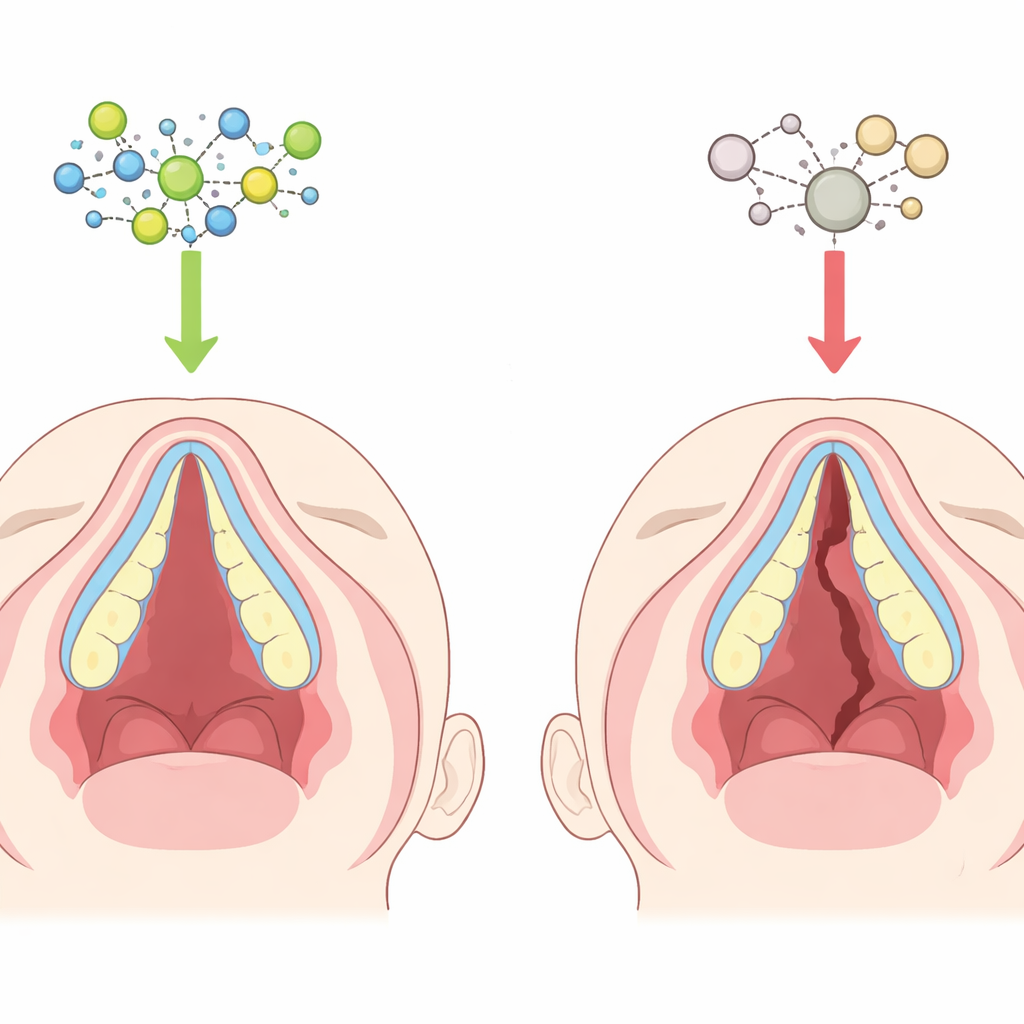
كيف يتشكّل الحنك عادة
خلال التطور المبكّر، ينمو رفّان من النسيج نحو الداخل من جانبي الفك العلوي، يرتفعان بجانب اللسان ثم يلتقيان ويلتحمان في الوسط لتكوين سقف الفم. داخل هذه الرفوف، تتحوّل الخلايا الجنينية الطرية تدريجيًا إلى خلايا عظمية تبني الحنك الصلب. إذا فشلت الرفوف في النمو أو التحرك أو الالتقاء أو التكلّس بشكل صحيح، قد يبقى فراغ ينتج عنه شق. الجزء الأمامي من الحنك يتكوّن مباشرة من تحوّل النسيج الطري إلى عظم، وهي عملية تحتاج توقيتًا وتحكّمًا دقيقين للغاية. يمكن للاضطرابات الدقيقة في هذا التوقيت أن تترك الحنك مغطّى بالجلد والغشاء المخاطي لكن بدون دعم عظمي كافٍ.
وسم سكّري صغير له دور تطوري كبير
يركّز الباحثون على "وسم" كيميائي يُدعى O-GlcNAc، وهو سكر صغير يمكن للخلايا أن ترفقه بالعديد من البروتينات لضبط سلوكها بدقة. إنزيم واحد، ناقل O-GlcNAc (OGT)، يضيف هذا الوسم، ويعمل كنوع من لوحة المفاتيح الجزيئية التي تستجيب لحالة المغذّيات والإجهاد في الخلية. في أجنة الفئران المعرّضة لحمض الريتينويك الشامل (all-trans retinoic acid)، مركّب معروف بتسبّبه الموثوق في الحنك المشقوق، وجد الفريق أن كلًا من وسوم O-GlcNAc ومستويات OGT انخفضت بشكل حاد في الحنك النامي. ويدل ذلك على أنه عندما ينخفض نشاط نظام التوسيم السكري هذا، قد يواجه الحنك صعوبة في تكوين عظم طبيعي.
دروس من الأسماك وخلايا حنك بشرية
لاختبار أهمية هذا الوسم السكري لبناء الحنك، لجأ الباحثون إلى سمك الزِبرا، الذي يعكس تطوّر الوجه والجمجمة عند الثدييات في جوانب رئيسية. عندما أعاقوا OGT أو حموا O-GlcNAc كيميائيًا في أجنة الزِبرا، طورت الأسماك معدلات أعلى بكثير من الفجوات الشبيهة بالشق في منطقة الحنك وتكلّسًا أضعف لعظمة قحفية مركزية. إن توفير مادة جينية إضافية لـ ogt أعاد جزئيًا هذه العيوب، مما عزّز الصلة بين O-GlcNAc وتكوّن حنك صحي. بالتوازي، استخدم الفريق خلايا الميزنكايم الحنكية الجنينية البشرية (HEPM)—خلايا تشبه تلك التي تشكّل الحنك الصلب البشري. خفض OGT في هذه الخلايا لم يوقف انقسامها، لكنه أخمد قدرتها على التمايز إلى خلايا مُكوّنة للعظم ووضع الترسبات المعدنية، مؤكّدًا أن نظام التوسيم السكري مرتبط مباشرة بقدرة بناء العظم.
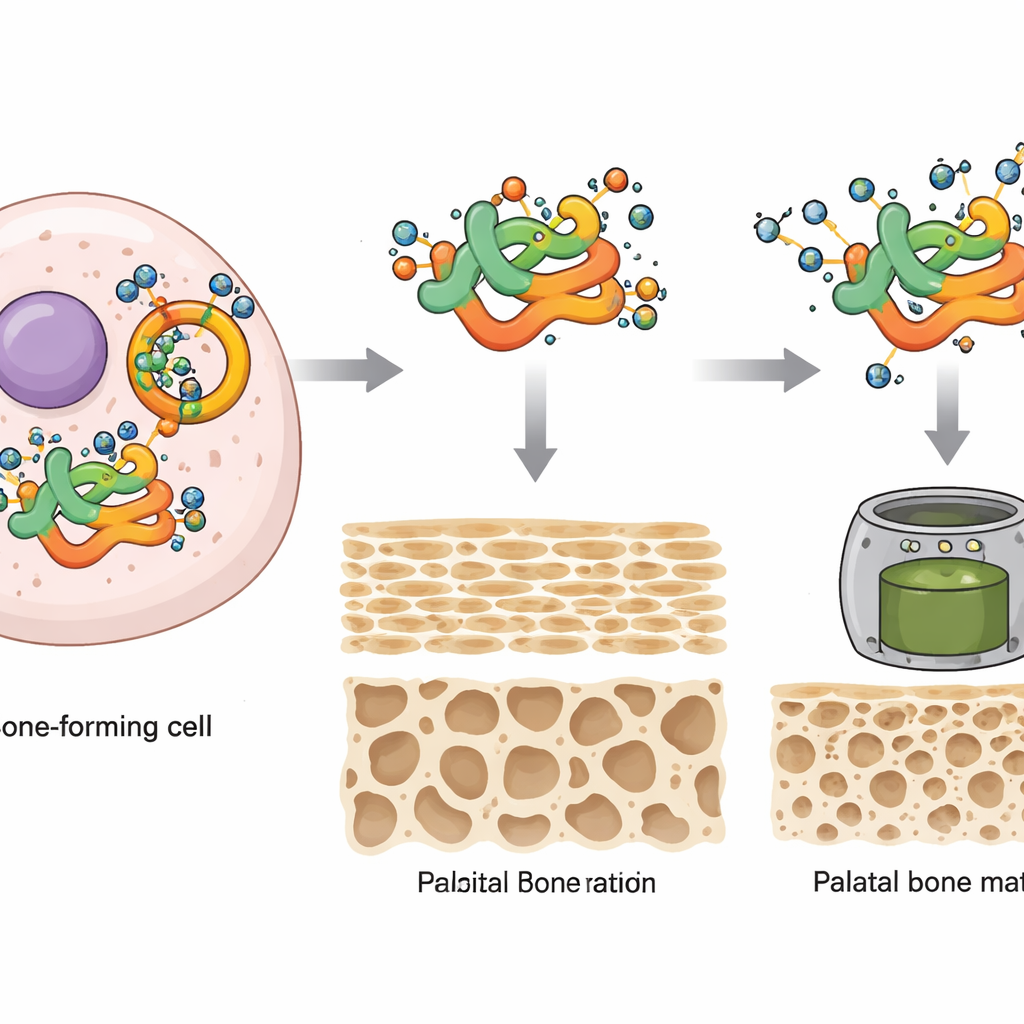
حماية "المهندس" الرئيسي من التحطيم
توجّهت الدراسة بعد ذلك نحو بروتين محدد يُدعى MEIS2، وهو عامل رابط للحمض النووي معروف بالفعل بأهميته لتطوّر الوجه والجمجمة ومرتبط بالحنك المشقوق لدى الأطفال عند طفرته. اكتشف المؤلفون أن MEIS2 يرتبط فعليًا بـ OGT ويحمل وسوم O-GlcNAc في موقع حمض أميني معيّن (يسمّى Ser237 في الثدييات). عندما تغيّر هذا الموقع بحيث لم يعد قابلاً للتوسيم، فقد MEIS2 معظم تعديله السكري. وبدون وسم O-GlcNAc السليم، انخفضت مستويات بروتين MEIS2 بسرعة، ليس لأن الجين أُطفئ، بل لأن البروتين وُوسم أكثر لتدميره عبر نظام اليوبيكويتين–بروتيازوم في الخلية. لذا يعمل وسم O-GlcNAc كدرع يثبّت MEIS2 ويمنع تفكيكه المبكّر.
ربط النقاط بجينات بناء العظم
لا يكتفي MEIS2 المثبّت بوجوده فحسب—بل يُفعّل جيوبًا جينية أخرى. أحد أهدافه المهمة هو SHOX2، منظّم آخر متورط بقوة في تطوّر الحنك الصلب. أظهر الفريق أن MEIS2 يربط منطقة التحكم في جين SHOX2 ويعزّز نشاطه، في حين أن فقدان OGT أو طفرَة موقع وسم MEIS2 تضعف هذا التنشيط. في خلايا HEPM الخالية من OGT، أعاد إدخال MEIS2 الطبيعي علامات التمايز العظمي والترسبات المعدنية، بينما فشل شكل MEIS2 غير القابل لحمل الوسم في ذلك. في سمك الزِبرا، استطاعت كمية إضافية من رسالة meis2 المُرتّلة إنقاذ عيوب عظم الحنك الناجمة عن فقد ogt، في حين فشل الشكل الخالي من الوسم مجددًا. معًا، توضح هذه التجارب سلسلة واضحة: يضيف OGT وسومًا سكريّة إلى MEIS2، مما يحافظ على استقراره، فيفعّل بدوره SHOX2 وجينات عظمية أخرى، ما يسمح بتشكّل عظام الحنك بشكل سليم.
ماذا يعني هذا لرعاية الحنك المشقوق مستقبلًا
بعبارات بسيطة، يحدّد هذا العمل نظام رقابة نوعي مجهرِي يساعد خلايا الحنك الجنينية على إبقاء "المهندس" البروتيني الرئيسي في موقعه لفترة كافية لبناء سقف فم عظمي متين. عندما يضعف إنزيم وسم السكر OGT—بسبب تغييرات جينية أو ضغوط بيئية—يُجرد بروتين MEIS2 ويتحلّل بسرعة، ولا تُنفّذ تعليمات بناء العظم كاملة، ما يزيد خطر حدوث الحنك المشقوق. ورغم أن أي تطبيق سريري ما يزال بعيدًا، فإن فهم سلسلة OGT–MEIS2–SHOX2 يوفر إطارًا جديدًا للتفكير في كيفية تداخل الجينات والتغذية والتعرّضات الكيميائية أثناء تطور الوجه، ويشير إلى أهداف جزيئية قد تُستغل يومًا ما لتحسين التشخيص أو التنبؤ أو حتى الوقاية من بعض حالات الحنك المشقوق.
الاستشهاد: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
الكلمات المفتاحية: الشفّة الأرنبية والحنك المشقوق, تطوّر الوجه والجمجمة, تعديل بعد الترجّم, O-GlcNAcylation, MEIS2