Clear Sky Science · fr
OGT médie l’O-GlcNAcylation de MEIS2 et influence le développement ostéogénique du palais
Pourquoi cette recherche compte pour les visages en croissance
La fente palatine est l’un des défauts de naissance les plus fréquents affectant la bouche et le visage des nouveau‑nés. Elle peut compliquer l’alimentation, la parole et, plus tard, la santé dentaire, et aujourd’hui les médecins ne peuvent la traiter qu’après son apparition. Cette étude pose une question plus fondamentale : que se passe‑t‑il au niveau microscopique pendant la formation des os du palais dans l’embryon, et la compréhension de ces processus cachés pourrait‑t‑elle un jour aider à prévenir l’apparition des fentes ?
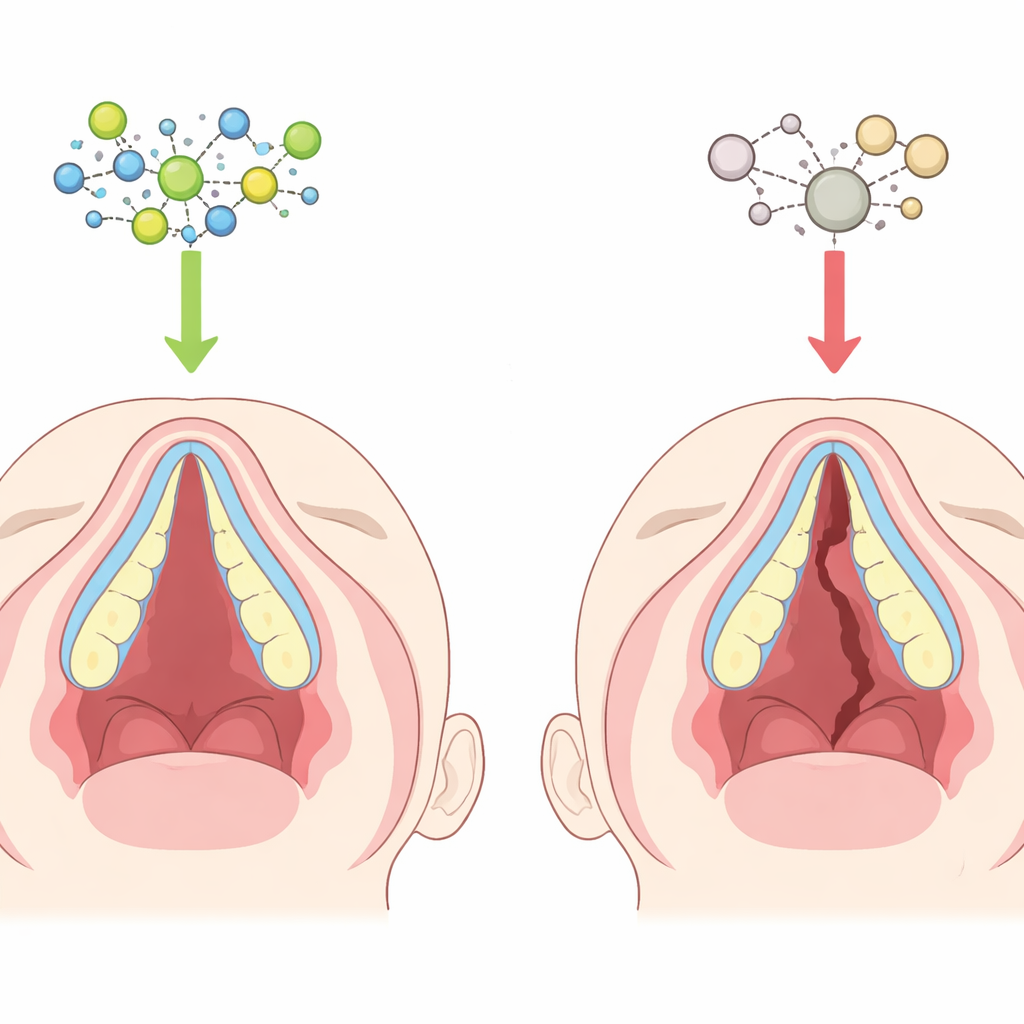
Comment le palais se forme normalement
Au cours du développement précoce, deux bourrelets de tissu croissent vers l’intérieur à partir des côtés de la mâchoire supérieure, se dressent de part et d’autre de la langue, puis se rejoignent et fusionnent au milieu pour créer le toit de la bouche. À l’intérieur de ces bourrelets, des cellules embryonnaires souples se transforment progressivement en cellules osseuses qui forment le palais dur. Si les bourrelets ne croissent pas, ne se déplacent pas, ne se rencontrent pas ou ne se minéralisent pas correctement, un espace peut subsister, produisant une fente. La partie antérieure du palais se forme par la transformation directe de tissu mou en os, un processus qui doit être minutieusement synchronisé et régulé. De subtiles perturbations de ce calendrier peuvent laisser le palais recouvert de peau et de muqueuse mais insuffisamment soutenu par l’os.
Une petite étiquette sucrée au rôle essentiel
Les auteurs s’intéressent à une « étiquette » chimique appelée O‑GlcNAc, un petit sucre que la cellule peut attacher à de nombreuses protéines pour ajuster finement leur comportement. Une seule enzyme, la O‑GlcNAc transférase (OGT), ajoute cette étiquette, agissant comme un tableau de commutation moléculaire qui répond au statut nutritionnel et au stress de la cellule. Chez des embryons de souris exposés à l’acide rétinoïque tout‑trans, un composé qui provoque de façon fiable des fentes palatines, l’équipe a observé une forte réduction à la fois des marques O‑GlcNAc et du niveau d’OGT dans le palais en développement. Cela suggère que lorsque ce système d’étiquetage sucré est diminué, le palais peut éprouver des difficultés à former un os normal.
Enseignements tirés des poissons et des cellules palatines humaines
Pour tester si cette étiquette sucrée est réellement importante pour la formation du palais, les chercheurs se sont tournés vers le poisson zèbre, dont le développement craniofacial reflète étroitement des aspects clés des mammifères. Lorsqu’ils ont bloqué OGT ou inhibé chimiquement l’O‑GlcNAc chez des embryons de zèbre, les poissons ont présenté des taux beaucoup plus élevés d’espaces de type fente dans la région palatine et une minéralisation affaiblie d’un os crânien central. L’apport d’un excès de matériel génétique ogt a partiellement sauvé ces défauts, renforçant le lien entre l’O‑GlcNAc et la formation saine du palais. Parallèlement, l’équipe a utilisé des cellules mésenchymateuses palatines embryonnaires humaines (HEPM) — des cellules similaires à celles qui forment le palais dur humain. La réduction d’OGT dans ces cellules n’a pas arrêté leur division, mais a diminué leur capacité à se différencier en ostéoblastes et à déposer des minéraux, confirmant que le système d’étiquetage sucré est directement lié à la capacité de formation osseuse.
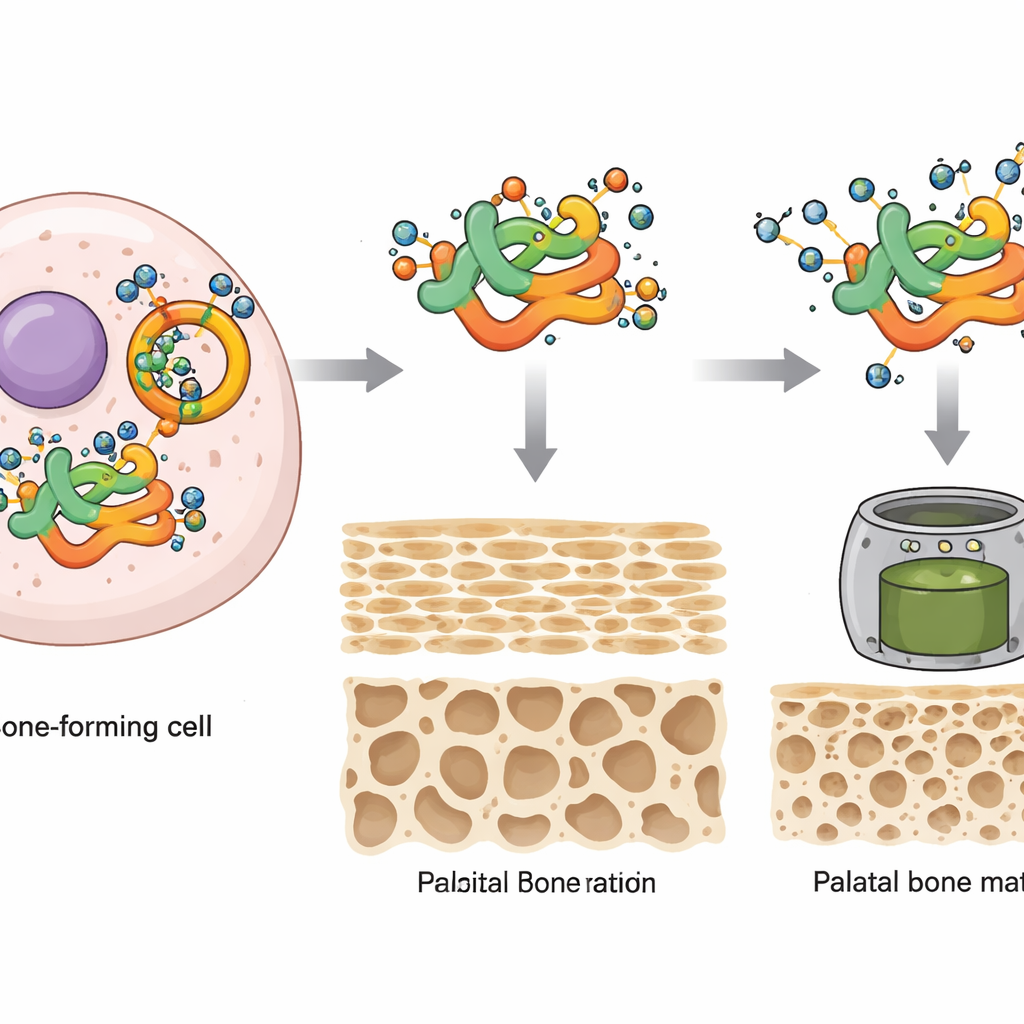
Protéger une protéine « architecte » clé de la destruction
L’étude s’est ensuite concentrée sur une protéine spécifique appelée MEIS2, un facteur liant l’ADN déjà connu pour être crucial au développement craniofacial et associé à la fente palatine chez l’enfant lorsqu’il est muté. Les auteurs ont découvert que MEIS2 s’associe physiquement à OGT et porte des marques O‑GlcNAc à une position acide‑aminée particulière (appelée Ser237 chez les mammifères). Lorsque ce site a été modifié de façon à ne plus pouvoir être étiqueté, MEIS2 a perdu la majeure partie de sa modification sucrée. En l’absence d’un marquage O‑GlcNAc correct, les niveaux de protéine MEIS2 ont chuté rapidement, non pas parce que le gène était éteint, mais parce que la protéine était davantage ciblée pour destruction par le système ubiquitine–protéasome de la cellule. L’étiquetage par O‑GlcNAc agit donc comme un bouclier qui stabilise MEIS2 et l’empêche d’être prématurément dégradée.
Relier cela aux gènes ostéogéniques
MEIS2 stabilisé ne se contente pas d’exister — il active d’autres gènes. L’une de ses cibles importantes est SHOX2, un autre régulateur fortement impliqué dans le développement du palais dur. L’équipe a montré que MEIS2 se lie à la région de contrôle du gène SHOX2 et en augmente l’activité, tandis que la perte d’OGT, ou la mutation du site d’étiquetage de MEIS2, affaiblit cette activation. Dans les cellules HEPM dépourvues d’OGT, la réintroduction de MEIS2 normal a restauré les marqueurs de formation osseuse et les dépôts minéraux, mais une version de MEIS2 incapable de porter l’étiquette sucrée ne l’a pas fait. Chez le poisson zèbre, un excès d’ARNm de meis2 a pu sauver les défauts osseux palatins causés par la perte d’ogt, alors qu’une version déficiente en étiquette a de nouveau échoué. Ensemble, ces expériences décrivent une chaîne claire : OGT ajoute des marques sucrées à MEIS2, ce qui stabilise MEIS2, qui à son tour active SHOX2 et d’autres gènes osseux, permettant la formation correcte de l’os palatin.
Ce que cela signifie pour la prise en charge future des fentes palatines
En termes concrets, ce travail identifie un système microscopique de contrôle de qualité qui aide les cellules embryonnaires du palais à maintenir une protéine « architecte » clé suffisamment longtemps pour construire un toit osseux solide de la bouche. Lorsque l’enzyme d’étiquetage sucré OGT est affaiblie — par des variations génétiques ou des stress environnementaux — la protéine MEIS2 est dépouillée et détruite trop rapidement, les instructions de construction osseuse ne sont pas pleinement exécutées et le risque de fente palatine augmente. Bien que toute application clinique soit encore lointaine, la compréhension de cette chaîne OGT–MEIS2–SHOX2 offre un nouveau cadre pour penser l’interaction entre gènes, nutrition et expositions chimiques pendant le développement facial, et pointe vers des cibles moléculaires qui pourraient un jour servir à mieux diagnostiquer, prédire ou même prévenir certains cas de fente palatine.
Citation: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
Mots-clés: fente palatine, développement craniofacial, modification post‑tradutionnelle, O‑GlcNAcylation, MEIS2