Clear Sky Science · nl
OGT bemiddelt O-GlcNAcylatie van MEIS2 en beïnvloedt osteogene ontwikkeling van het gehemelte
Waarom dit onderzoek belangrijk is voor groeiende gezichten
Een gespleten gehemelte is een van de meest voorkomende aangeboren afwijkingen die de mond en het gezicht van zuigelingen aantasten. Het kan voeding, spraak en later de tandheelkundige gezondheid sterk bemoeilijken, en tegenwoordig kunnen artsen het alleen behandelen nadat het zich heeft voorgedaan. Deze studie stelt een dieperliggende vraag: wat gaat er op microscopisch niveau mis terwijl de gehemeltebeenderen zich in de embryo vormen, en kan het begrijpen van die verborgen processen op termijn helpen om schisis te voorkomen?
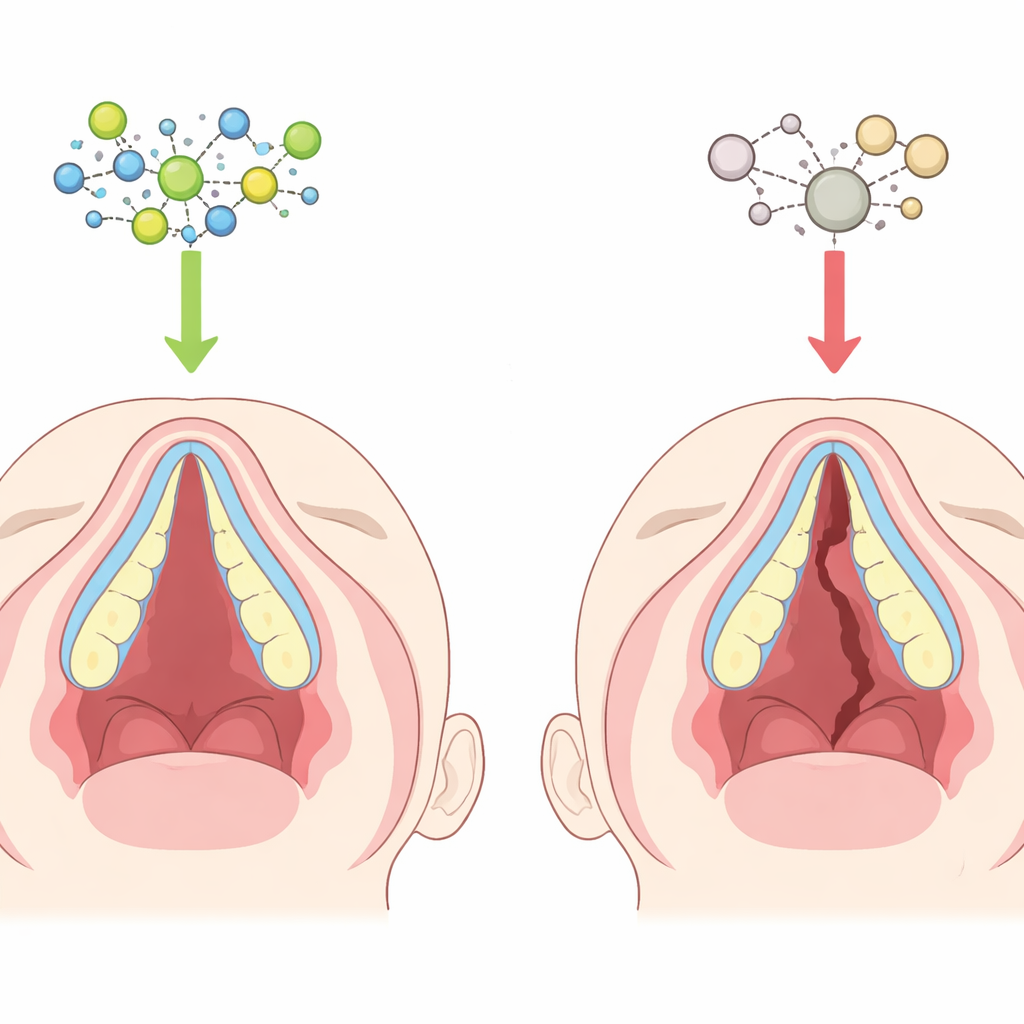
Hoe het gehemelte normaal gevormd wordt
In de vroege ontwikkeling groeien twee weefselschotten naar binnen vanaf de zijkanten van de bovenkaak, rijzen op naast de tong en ontmoeten en versmelten vervolgens in het midden om het gehemelte te vormen. In deze schotten veranderen zachte embryonale cellen geleidelijk in botvormende cellen die het harde gehemelte opbouwen. Als de schotten niet goed groeien, bewegen, samenkomen of verharden, kan er een opening overblijven die een schisis veroorzaakt. Het voorste deel van het gehemelte ontstaat direct doordat zacht weefsel in bot verandert, een proces dat zeer precies in tijd en regulatie moet zijn afgestemd. Subtiele verstoringen in deze timing kunnen ertoe leiden dat het gehemelte bedekt blijft met huid en slijmvlies maar onvoldoende door bot wordt ondersteund.
Een klein suikertje met een grote ontwikkelingsrol
De auteurs richten zich op een chemisch „etiket” dat O-GlcNAc wordt genoemd, een klein suikerrestje dat cellen aan veel verschillende eiwitten kunnen koppelen om hun gedrag fijn af te stemmen. Één enzym, O-GlcNAc-transferase (OGT), voegt dit etiket toe en fungeert als een soort moleculair schakelpaneel dat reageert op de voedings- en stressstatus van de cel. In muizenembryo’s die werden blootgesteld aan all-trans retinoïnezuur, een verbinding die betrouwbaar een schisis veroorzaakt, vonden de onderzoekers dat zowel O-GlcNAc-labels als OGT-niveaus scherp verminderd waren in het zich ontwikkelende gehemelte. Dit suggereerde dat wanneer dit suikerlabelsysteem wordt teruggedraaid, het gehemelte moeite kan hebben om normaal bot te vormen.
Lessen uit vissen en menselijke gehemeltecellen
Om te testen of dit suikeretiket echt belangrijk is voor de bouw van het gehemelte, gebruikten de onderzoekers zebravissen, waarvan de craniomaxillaire ontwikkeling belangrijke overeenkomsten met zoogdieren vertoont. Wanneer ze OGT blokkeerden of O-GlcNAc chemisch remden in zebravisembryo’s, ontwikkelden de vissen veel vaker scheurachtige openingen in het gehemeltegebied en minder sterke mineralisatie van een centraal schedelbeen. Het toedienen van extra ogt-genmateriaal herstelde deze defecten gedeeltelijk, wat de link tussen O-GlcNAc en gezonde gehemeltevorming versterkt. Parallel daaraan gebruikte het team menselijke embryonale palatale mesenchymcellen (HEPM)—cellen vergelijkbaar met die het menselijke harde gehemelte vormen. Het verminderen van OGT in deze cellen stopte hun deling niet, maar verminderde wel hun vermogen om te differentiëren naar botvormende cellen en om mineraaldeposities aan te leggen, wat bevestigt dat het suikerlabelsysteem direct gerelateerd is aan botopbouwcapaciteit.
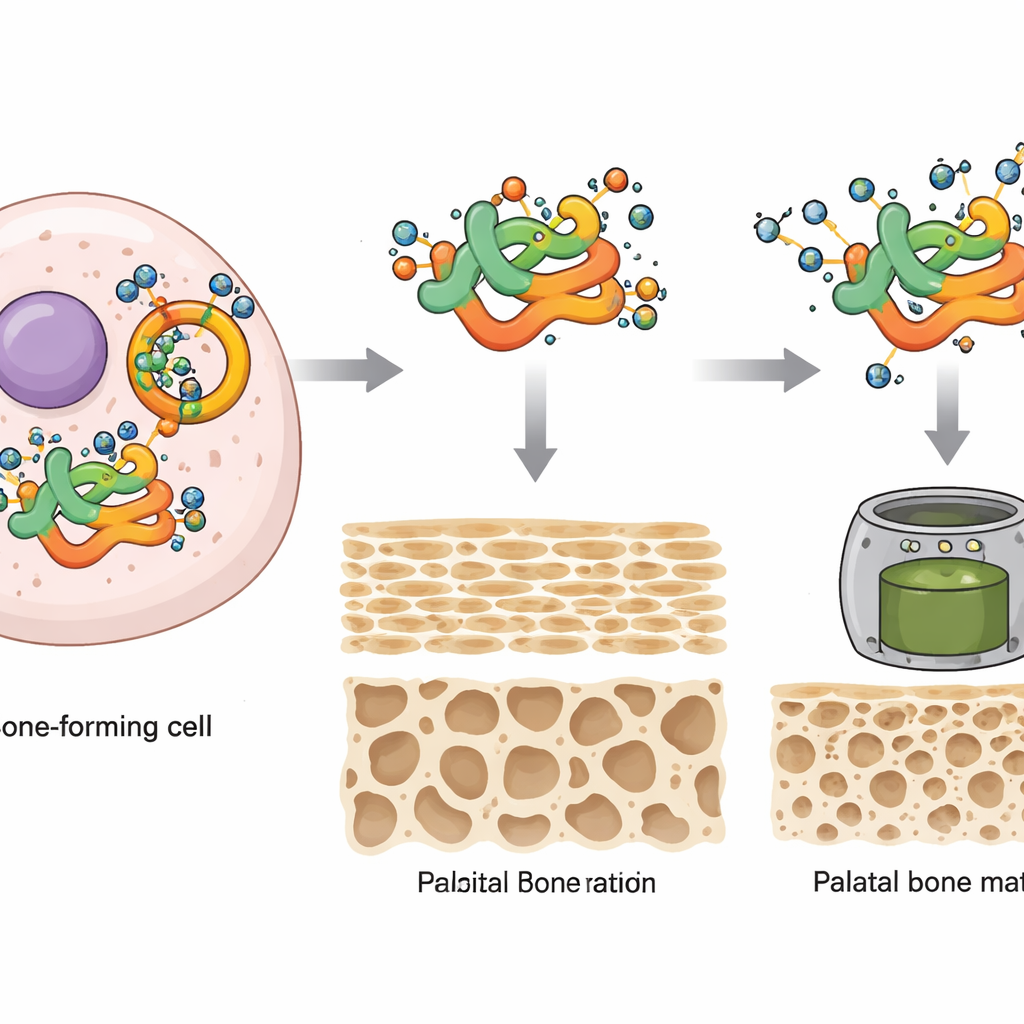
Een sleutel‑"architect"eiwit beschermen tegen afbraak
Vervolgens zoomde de studie in op een specifiek eiwit genaamd MEIS2, een DNA-bindende factor die al bekendstaat als cruciaal voor craniomaxillaire ontwikkeling en geassocieerd wordt met schisis bij kinderen wanneer het gemuteerd is. De auteurs ontdekten dat MEIS2 fysiek samenwerkt met OGT en O-GlcNAc-labels draagt op een specifieke aminozuurpositie (Ser237 bij zoogdieren). Wanneer deze site zo werd veranderd dat hij niet meer gelabeld kon worden, verloor MEIS2 het grootste deel van zijn suiker-modificatie. Zonder juiste O-GlcNAc-modificatie daalden de MEIS2-eiwitniveaus snel, niet omdat het gen minder actief was, maar omdat het eiwit sterker gemarkeerd werd voor afbraak door het ubqiuïtine–proteasoom ‘versnipperaar’-systeem van de cel. O-GlcNAc-tagging fungeert dus als een schild dat MEIS2 stabiliseert en voorkomt dat het voortijdig wordt afgebroken.
De schakels naar botopbouwgenen
Gestabiliseerd MEIS2 doet meer dan alleen aanwezig zijn — het schakelt andere genen aan. Een belangrijk doelgen is SHOX2, een andere regulator die sterk betrokken is bij de ontwikkeling van het harde gehemelte. Het team toonde aan dat MEIS2 bindt aan het controlegebied van het SHOX2-gen en de activiteit ervan verhoogt, terwijl verlies van OGT, of een mutatie in de MEIS2-suikerlabelsitel, deze activatie verzwakt. In HEPM-cellen zonder OGT herstelde het opnieuw inbrengen van normaal MEIS2 markers voor botvorming en mineraaldeposities, maar een MEIS2‑variant die het suikeretiket niet kon dragen deed dat niet. In zebravissen kon extra meis2-mRNA gehemeltebotdefecten door ogt‑verlies verhelpen, terwijl een label‑deficiënte versie opnieuw faalde. Samen schetsen deze experimenten een duidelijke keten: OGT voegt suikerlabels toe aan MEIS2, waardoor MEIS2 stabiel blijft, wat op zijn beurt SHOX2 en andere botgenen activeert, waardoor gehemeltebot zich correct kan vormen.
Wat dit betekent voor toekomstige zorg bij gespleten gehemelte
In alledaagse bewoordingen identificeert dit werk een microscopisch kwaliteitssysteem dat embryonale gehemeltecellen helpt om een sleutel‑"architect"eiwit lang genoeg aan het werk te houden om een solide benig dak van de mond te bouwen. Wanneer het suikerlabelende enzym OGT verzwakt is — door genetische veranderingen of omgevingsstress — wordt het MEIS2‑eiwit te snel gestript en afgebroken, worden botopbouwinstructies niet volledig uitgevoerd en neemt het risico op schisis toe. Hoewel klinische toepassingen nog ver weg zijn, biedt begrip van de OGT–MEIS2–SHOX2-keten een nieuw kader om te begrijpen hoe genen, voeding en chemische blootstellingen samenkomen tijdens de gezichtontwikkeling, en wijst het op moleculaire doelen die op termijn mogelijk kunnen helpen bij betere diagnose, voorspelling of zelfs preventie van sommige gevallen van schisis.
Bronvermelding: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
Trefwoorden: schisis (gespleten gehemelte), craniomaxillaire ontwikkeling, post-translationele modificatie, O-GlcNAcylatie, MEIS2