Clear Sky Science · de
OGT vermittelt die O‑GlcNAcylierung von MEIS2 und beeinflusst die osteogene Entwicklung des Gaumens
Warum diese Forschung für wachsende Gesichter wichtig ist
Lippen‑ und Gaumenspalten gehören zu den häufigsten angeborenen Fehlbildungen im Mund‑ und Gesichtsbereich. Sie können das Stillen und Füttern, die Sprachentwicklung und später die zahnmedizinische Gesundheit deutlich erschweren, und heute lassen sich solche Spalten erst nach ihrem Auftreten behandeln. Diese Studie stellt eine grundlegendere Frage: Was läuft auf mikroskopischer Ebene schief, während im Embryo die Gaumenknochen entstehen, und könnte das Verständnis dieser verborgenen Prozesse eines Tages helfen, Spalten bereits vorbeugend zu verhindern?
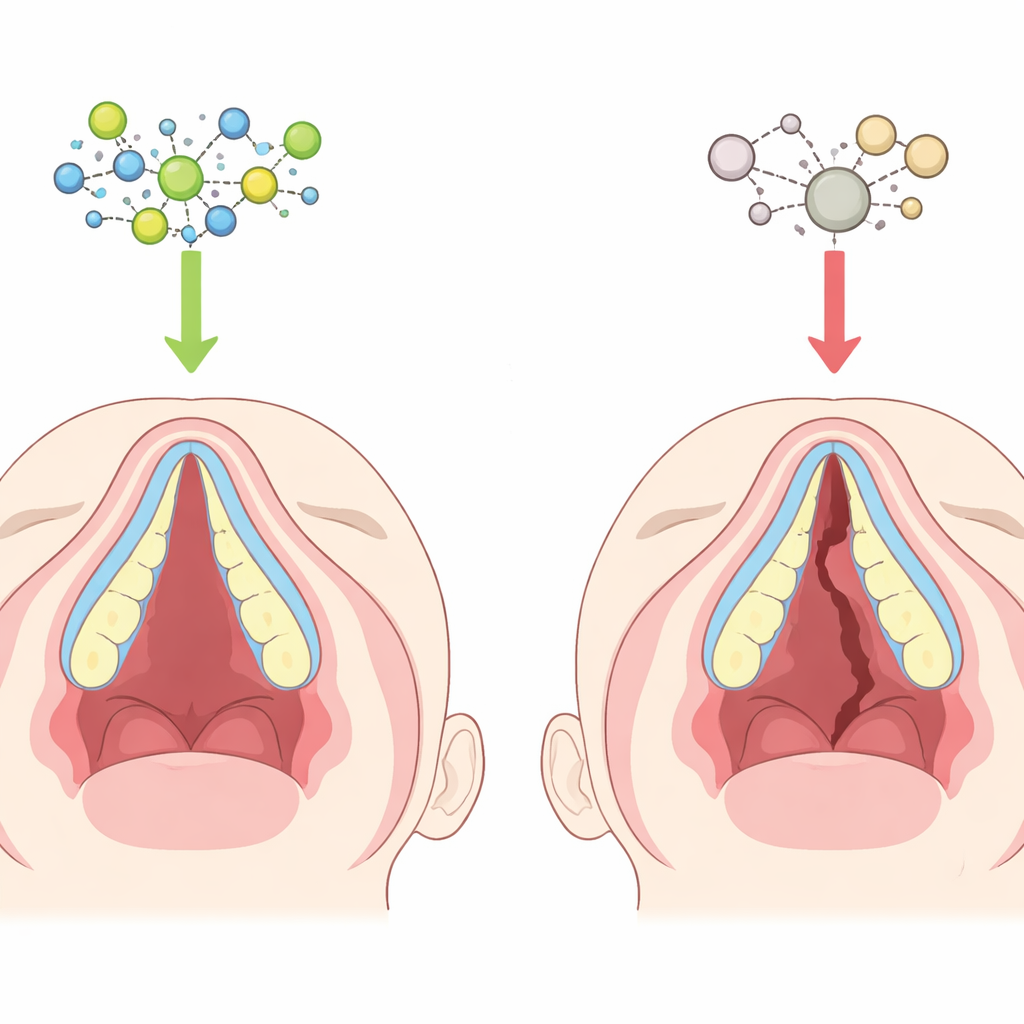
Wie sich der Gaumen normalerweise formt
In der frühen Entwicklung wachsen zwei Gewebswülste vom seitlichen Oberkiefer nach innen, erheben sich neben der Zunge und treffen sich in der Mitte, um das Gaumendach zu bilden. In diesen Wülsten differenzieren sich weiche embryonale Zellen allmählich zu knochenbildenden Zellen, die den harten Gaumen aufbauen. Versagen das Wachstum, die Bewegung, das Zusammentreffen oder die Verknöcherung der Wülste, kann eine Lücke bestehen bleiben und eine Spalte entstehen. Der vordere Teil des Gaumens entsteht direkt durch die Umwandlung von Weichgewebe in Knochen – ein Prozess, der zeitlich sehr genau gesteuert werden muss. Schon subtile Störungen in diesem Timing können dazu führen, dass der Gaumen zwar von Haut und Schleimhaut bedeckt ist, aber nur unzureichend durch Knochen gestützt wird.
Ein winziger Zuckeranhang mit großer Entwicklungsrolle
Die Autorinnen und Autoren konzentrieren sich auf eine chemische „Marke“ namens O‑GlcNAc, ein kleiner Zucker, den Zellen an viele verschiedene Proteine anhängen können, um deren Verhalten fein zu justieren. Ein einziges Enzym, die O‑GlcNAc‑Transferase (OGT), fügt diese Marke an und fungiert damit als eine Art molekulares Schalbrett, das auf den Nährstoff‑ und Stressstatus der Zelle reagiert. In Mausembryonen, die all‑trans Retinsäure ausgesetzt waren – einer Verbindung, die zuverlässig Gaumenspalten hervorruft –, fanden die Forschenden deutlich reduzierte O‑GlcNAc‑Markierungen und niedrigere OGT‑Spiegel im sich entwickelnden Gaumen. Das deutet darauf hin, dass bei Abschwächung dieses Zuckeranhang‑Systems die Ausbildung normalen Gaumenknochens gestört sein kann.
Erkenntnisse aus Fisch und menschlichen Gaumenzellen
Um zu prüfen, ob diese Zuckermarkierung tatsächlich wichtig für den Gaumenaufbau ist, nutzten die Forschenden Zebrafische, deren kraniofaziale Entwicklung entscheidende Parallelen zu Säugetieren aufweist. Wurden OGT blockiert oder O‑GlcNAc chemisch gehemmt, entwickelten die Embryonen deutlich höhere Raten von spaltenähnlichen Lücken im Gaumenbereich und eine schwächere Mineralisierung eines zentralen Schädelknochens. Die Zuführung zusätzlicher ogt‑Genkopien konnte diese Defekte teilweise beheben und verstärkte damit die Verbindung zwischen O‑GlcNAc und gesunder Gaumenbildung. Parallel dazu verwendete das Team humane embryonale palatinale mesenchymale (HEPM) Zellen – Zellen, die denen ähneln, die den menschlichen harten Gaumen bilden. Die Reduktion von OGT in diesen Zellen verhinderte nicht deren Teilung, schwächte aber ihre Fähigkeit, zu knochenbildenden Zellen zu differenzieren und Mineralablagerungen zu bilden, was bestätigt, dass das Zuckeranhang‑System direkt mit der Knochenbildungsfähigkeit verknüpft ist.
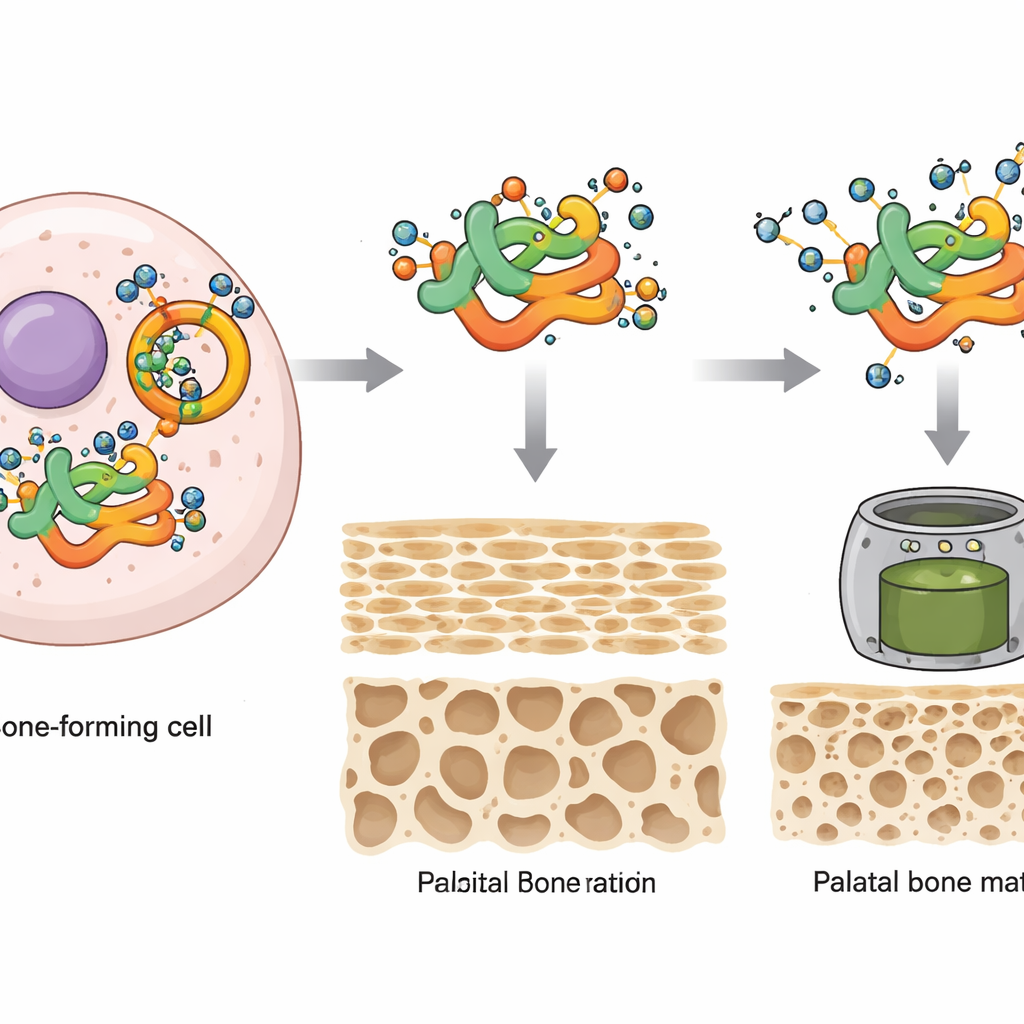
Ein wichtigen „Architekten“protein vor dem Abbau schützen
Die Studie fokussierte sich anschließend auf ein bestimmtes Protein namens MEIS2, einen DNA‑bindenden Faktor, der bereits als kritisch für die kraniofaziale Entwicklung bekannt ist und bei mutierten Formen mit Gaumenspalten bei Kindern in Verbindung gebracht wird. Die Forschenden entdeckten, dass MEIS2 physisch mit OGT assoziiert und O‑GlcNAc‑Marken an einer bestimmten Aminosäureposition trägt (bei Säugetieren Ser237). Wenn diese Stelle so verändert wurde, dass sie nicht mehr markiert werden konnte, verlor MEIS2 den Großteil seiner Zuckermodifikation. Ohne die richtige O‑GlcNAc‑Markierung sanken die MEIS2‑Proteinspiegel rasch – nicht weil das Gen ausgeschaltet wurde, sondern weil das Protein stärker für den Abbau durch das zelluläre Ubiquitin–Proteasom‑System markiert wurde. Die O‑GlcNAc‑Markierung wirkt somit wie ein Schild, das MEIS2 stabilisiert und verhindert, dass es vorzeitig abgebaut wird.
Die Verbindung zu knochenbildenden Genen
Stabilisiertes MEIS2 bewirkt mehr als nur Stabilität – es schaltet andere Gene ein. Eines seiner wichtigen Ziele ist SHOX2, ein weiterer Regulator, der stark an der Entwicklung des harten Gaumens beteiligt ist. Das Team zeigte, dass MEIS2 an die Kontrollregion des SHOX2‑Gens bindet und dessen Aktivität steigert, während der Verlust von OGT oder die Mutation der MEIS2‑Zuckerstelle diese Aktivierung abschwächt. In HEPM‑Zellen ohne OGT stellte die Wiedereinführung von normalem MEIS2 knochenbildende Marker und Mineralablagerungen wieder her, während eine MEIS2‑Variante, die den Zucker nicht tragen konnte, dies nicht vermochte. In Zebrafischen konnte zusätzliches meis2‑mRNA die durch ogt‑Verlust verursachten Gaumenknochendefekte retten, eine zuckerlose Variante hingegen erneut nicht. Zusammengenommen skizzieren diese Experimente eine klare Kette: OGT fügt MEIS2 Zuckeranhängsel hinzu, dies stabilisiert MEIS2, MEIS2 aktiviert SHOX2 und andere Knochen‑Gene, und ermöglicht so die korrekte Ausbildung des Gaumenknochens.
Was das für die zukünftige Versorgung von Gaumenspalten bedeutet
Anschaulich identifiziert diese Arbeit ein mikroskopisches Qualitätskontrollsystem, das embryonalen Gaumenzellen hilft, einen wichtigen „Architekten“ lange genug im Dienst zu halten, damit ein stabiles knöchernes Gaumendach entsteht. Wird das Zuckeranhang‑Enzym OGT durch genetische Veränderungen oder Umweltstress geschwächt, wird das MEIS2‑Protein zu schnell abgebaut, knochenbildende Instruktionen werden nicht vollständig umgesetzt und das Risiko einer Gaumenspalte steigt. Klinische Anwendungen liegen zwar noch in weiter Ferne, doch liefert das Verständnis der OGT–MEIS2–SHOX2‑Achse einen neuen Rahmen dafür, wie Gene, Ernährung und chemische Expositionen während der Gesichtsentwicklung zusammenwirken, und weist auf molekulare Ziele hin, die eines Tages zur besseren Diagnose, Prognose oder sogar Prävention einiger Fälle von Gaumenspalten genutzt werden könnten.
Zitation: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
Schlüsselwörter: Lippen‑Gaumen‑Spalte, kraniofaziale Entwicklung, posttranslationale Modifikation, O‑GlcNAcylierung, MEIS2