Clear Sky Science · es
OGT media la O-GlcNAcilación de MEIS2 y afecta el desarrollo osteogénico del paladar
Por qué esta investigación importa para las caras en crecimiento
El paladar hendido es uno de los defectos congénitos más comunes que afectan la boca y la cara de los recién nacidos. Puede dificultar la alimentación, el habla y la salud dental futura, y hoy los médicos solo pueden tratarlo una vez que ya aparece. Este estudio plantea una pregunta más profunda: ¿qué falla a nivel microscópico mientras se forman los huesos del paladar en el embrión, y podría entender esos procesos ocultos ayudar algún día a prevenir la aparición de hendiduras?
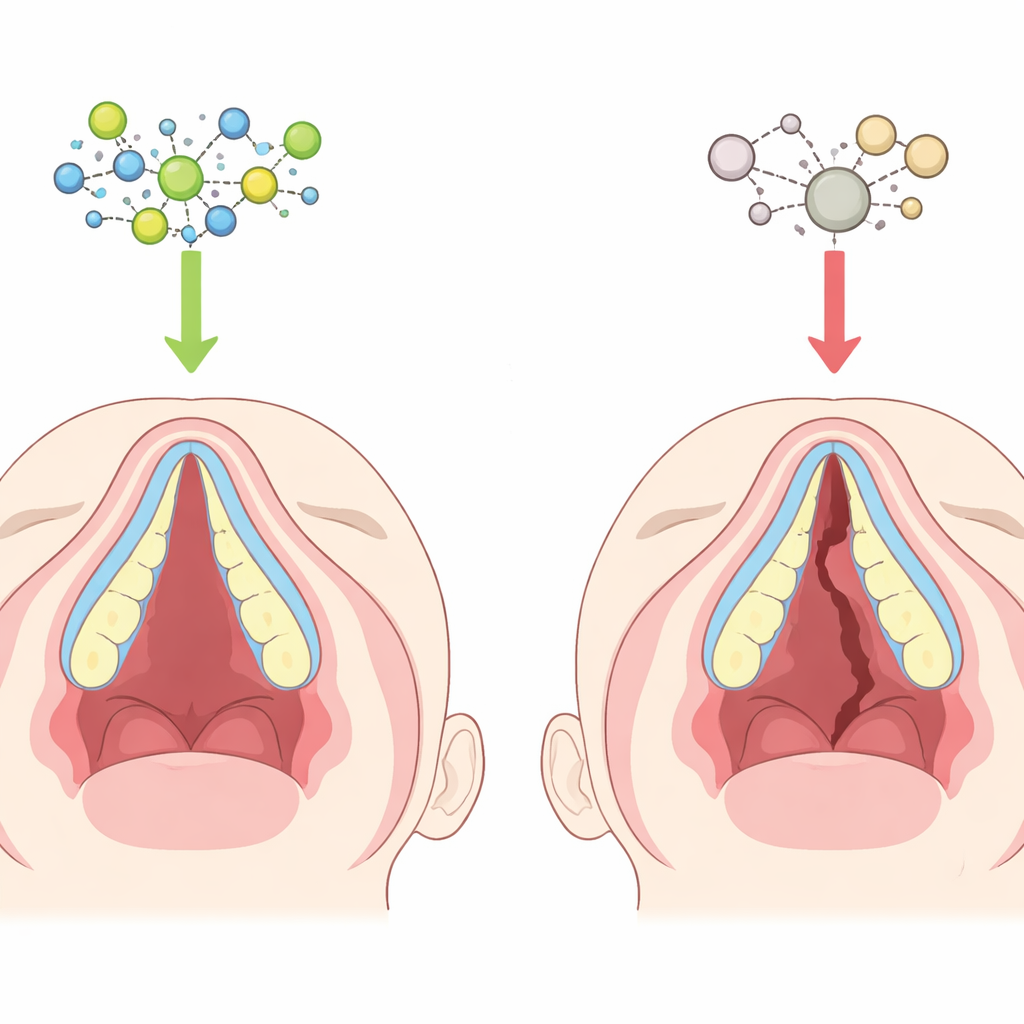
Cómo toma forma normalmente el paladar
En las primeras etapas del desarrollo, dos láminas de tejido crecen hacia el interior desde los lados del maxilar superior, se elevan junto a la lengua y luego se encuentran y fusionan en el centro para crear el techo de la boca. Dentro de estas láminas, células embrionarias blandas se transforman gradualmente en células óseas que construyen el paladar duro. Si las láminas no crecen, no se desplazan, no se encuentran o no se osifican correctamente, puede quedar una abertura que produce una hendidura. La parte anterior del paladar se forma directamente por la conversión de tejido blando en hueso, un proceso que debe estar sincronizado y controlado con mucha precisión. Pequeñas alteraciones en ese ritmo pueden dejar un paladar cubierto por piel y mucosa pero insuficientemente sostenido por hueso.
Una pequeña etiqueta azucarada con un gran papel en el desarrollo
Los autores se centran en una “etiqueta” química llamada O-GlcNAc, un pequeño azúcar que las células pueden unir a muchas proteínas distintas para ajustar finamente su comportamiento. Una única enzima, la O-GlcNAc transferasa (OGT), añade esta etiqueta, actuando como una suerte de centralita molecular que responde al estado nutricional y de estrés de la célula. En embriones de ratón expuestos a ácido retinoico todo-trans, un compuesto que causa de manera fiable paladar hendido, el equipo observó que tanto las etiquetas O-GlcNAc como los niveles de OGT estaban marcadamente reducidos en el paladar en desarrollo. Esto sugirió que cuando este sistema de etiquetado azucarado se atenúa, el paladar puede tener dificultades para formar hueso normal.
Lecciones de peces y células del paladar humano
Para probar si esta etiqueta azucarada es realmente importante para construir el paladar, los investigadores recurrieron al pez cebra, cuyo desarrollo craneofacial refleja estrechamente aspectos clave de los mamíferos. Cuando bloquearon OGT o inhibieron químicamente la O-GlcNAc en embriones de pez cebra, los peces desarrollaron tasas mucho mayores de aberturas tipo hendidura en el área del paladar y una mineralización más débil de un hueso craneal central. Suministrar material genético extra de ogt rescató parcialmente estos defectos, reforzando la relación entre la O-GlcNAc y la formación sana del paladar. En paralelo, el equipo usó células mesenquimales palatinas embrionarias humanas (HEPM)—células similares a las que forman el paladar duro humano. Reducir OGT en estas células no detuvo su proliferación, pero sí ralentizó su capacidad para convertirse en células formadoras de hueso y depositar minerales, confirmando que el sistema de etiquetado azucarado está vinculado directamente a la capacidad osteogénica.
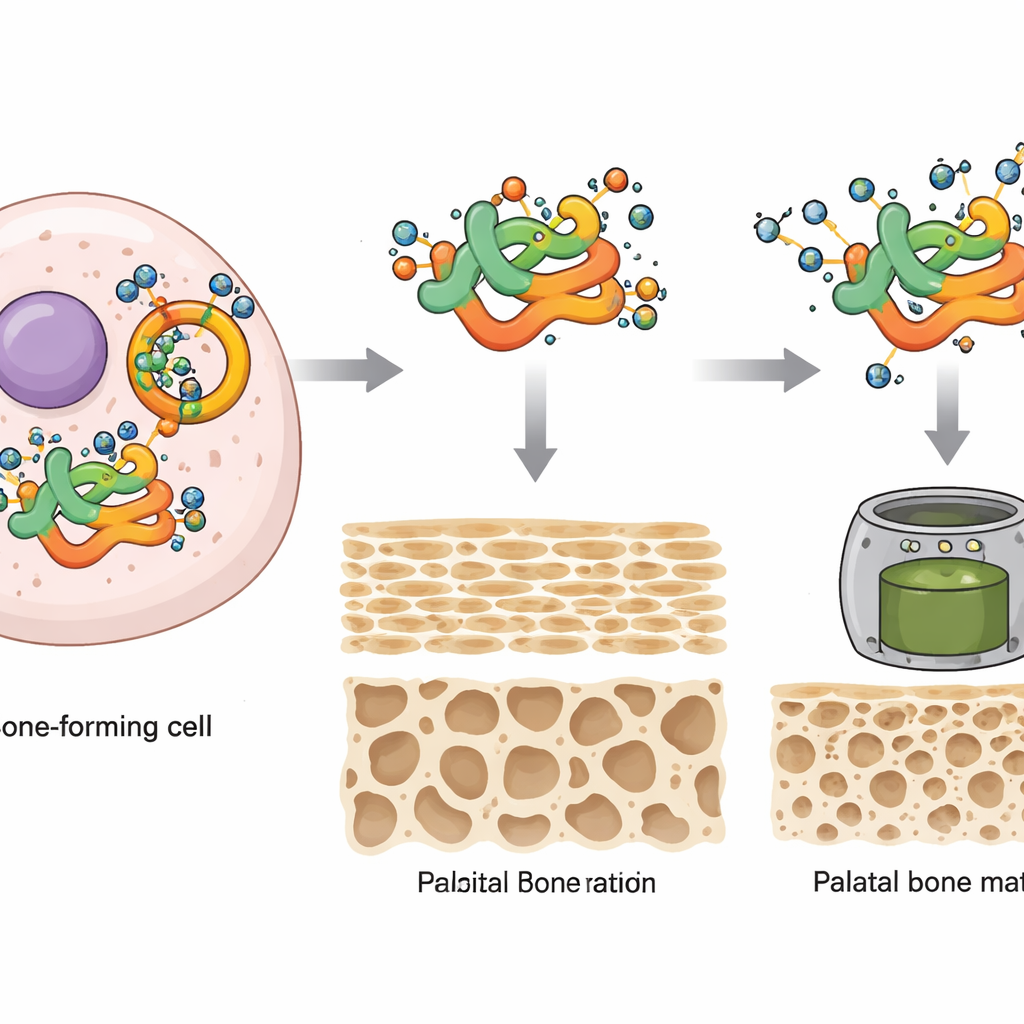
Protegiendo a una proteína “arquitecto” clave de ser eliminada
El estudio se centró luego en una proteína específica llamada MEIS2, un factor que se une al ADN y que ya se sabe que es crucial para el desarrollo craneofacial y que, cuando está mutado, se asocia con paladar hendido en niños. Los autores descubrieron que MEIS2 se asocia físicamente con OGT y porta etiquetas O-GlcNAc en una posición concreta del aminoácido (llamada Ser237 en mamíferos). Cuando este sitio se alteró de modo que ya no podía ser etiquetado, MEIS2 perdió la mayor parte de su modificación azucarada. Sin una correcta O-GlcNAc, los niveles de la proteína MEIS2 cayeron rápidamente, no porque su gen dejara de expresarse, sino porque la proteína quedó más fuertemente marcada para su destrucción por el sistema ubiquitina–proteasoma de la célula. Por tanto, la O-GlcNAc actúa como un escudo que estabiliza MEIS2 y evita que sea degradada prematuramente.
Conectando los puntos con los genes formadores de hueso
MEIS2 estabilizada hace más que simplemente existir: activa otros genes. Uno de sus objetivos importantes es SHOX2, otro regulador implicado de forma destacada en el desarrollo del paladar duro. El equipo mostró que MEIS2 se une a la región de control del gen SHOX2 y aumenta su actividad, mientras que la pérdida de OGT, o la mutación del sitio de etiquetado de MEIS2, debilitan esta activación. En células HEPM sin OGT, la reintroducción de MEIS2 normal restauró marcadores osteogénicos y depósitos minerales, pero una versión de MEIS2 que no podía portar la etiqueta azucarada no lo hizo. En pez cebra, el ARN mensajero extra de meis2 pudo rescatar defectos del hueso palatino causados por la pérdida de ogt, mientras que una versión carente de la etiqueta volvió a fallar. En conjunto, estos experimentos describen una cadena clara: OGT añade etiquetas azucaradas a MEIS2, lo que mantiene estable a MEIS2, que a su vez activa SHOX2 y otros genes óseos, permitiendo que el hueso palatino se forme correctamente.
Qué significa esto para el cuidado futuro del paladar hendido
En términos cotidianos, este trabajo identifica un sistema microscópico de control de calidad que ayuda a las células del paladar embrionario a mantener a un proteína “arquitecto” clave en el puesto el tiempo suficiente para construir un techo óseo sólido de la boca. Cuando la enzima de etiquetado azucarado OGT se debilita—por cambios genéticos o por factores ambientales—la proteína MEIS2 queda despojada y destruida demasiado pronto, las instrucciones para formar hueso no se ejecutan por completo y aumenta el riesgo de paladar hendido. Aunque cualquier aplicación clínica está todavía lejos, comprender esta cadena OGT–MEIS2–SHOX2 ofrece un nuevo marco para pensar cómo genes, nutrición y exposiciones químicas se entrelazan durante el desarrollo facial, y apunta a dianas moleculares que podrían algún día usarse para diagnosticar, predecir o incluso prevenir algunos casos de paladar hendido.
Cita: Zhang, Z., Shan, Z., Chen, X. et al. OGT mediates O-GlcNAcylation of MEIS2 and affects palatal osteogenic development. Int J Oral Sci 18, 32 (2026). https://doi.org/10.1038/s41368-026-00431-w
Palabras clave: paladar hendido, desarrollo craneofacial, modificación postraduccional, O-GlcNAcilación, MEIS2