Clear Sky Science · zh
体细胞突变与正常组织中的克隆演化及癌症发生
健康细胞内的隐秘变化
在肿瘤可在影像上被看到或在体表触及成块之前很久,我们的细胞已经在随着年龄增长、应对环境刺激和修复日常损伤的过程中悄然积累遗传改变。本文综述说明了这些被称为体细胞突变的不可见变化如何在外观正常的组织中累积,某些突变如何赋予个别细胞竞争优势,以及数十年慢速的“克隆演化”如何最终为癌症铺路。理解这片隐秘的演化景观正在重塑我们对癌症何时真正开始以及如何更早检测与预防它的看法。
科学家如何追踪微小的细胞家族
正常组织由许多微小的细胞家族或克隆组成,这些克隆中的大多数太小以至于传统方法难以研究。综述介绍了几种新工具,能以极高精度读取极少细胞的DNA。一种方法是用激光微切割取出微小组织片段并对其中全部DNA测序,从而获得克隆在空间上的排列快照。另一种方法是从单个细胞培养出迷你器官(类器官),并对其后代进行测序,揭示每个细胞的个人突变史。第三种策略是采用超高精度测序,在无需培养的情况下在大量细胞混合物中找到罕见突变。这些技术共同显示,即便是“健康”组织也充斥着携带类似癌症突变的细胞。 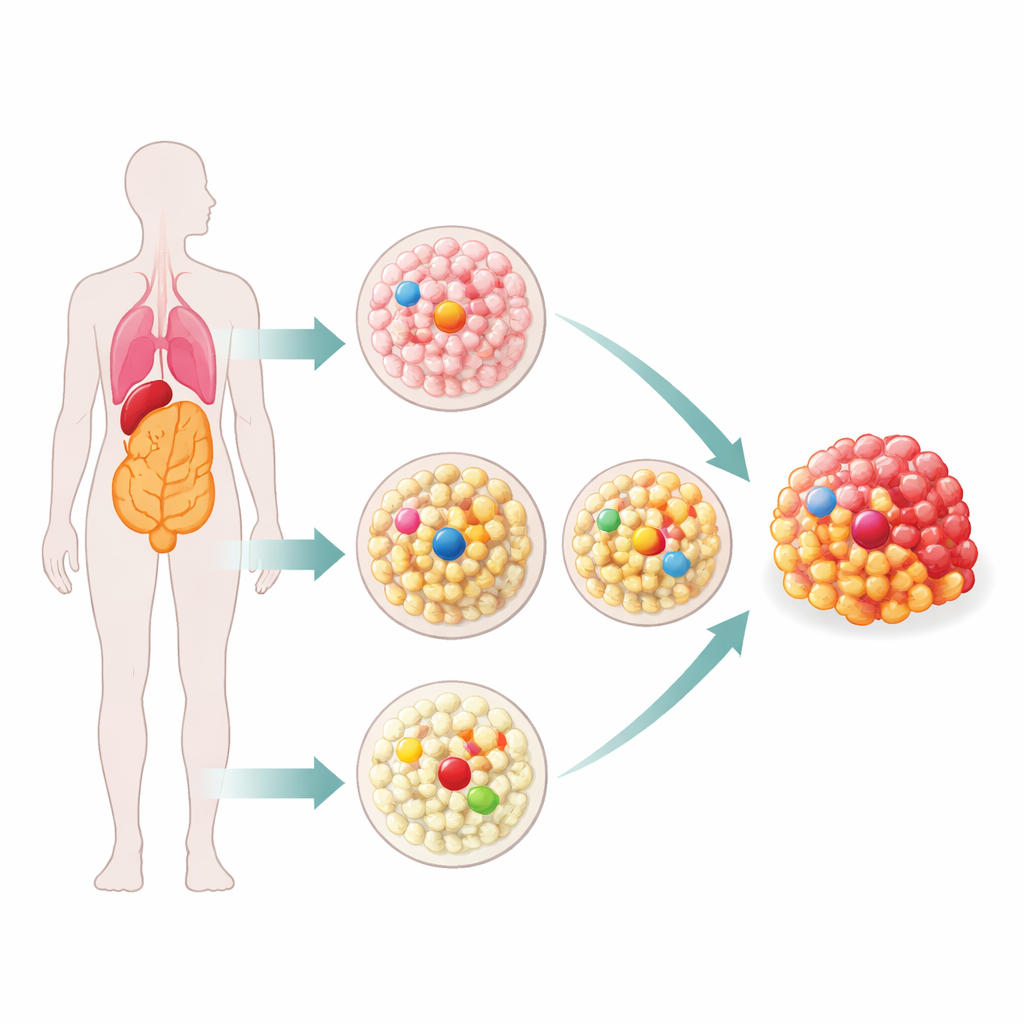
突变为何不断出现
正常细胞的突变来源大致可分为两类:内部磨损与外部暴露。从胚胎期最初的细胞分裂起,DNA复制就并非完美,细胞内的化学反应随着时间逐步损伤遗传物质。这些与年龄相关的过程在DNA中留下特征性的“署名”,可在许多器官中发现,甚至在神经元和肌肉等寿命较长的细胞中亦然。除此之外,外界因素如烟草烟雾、酒精、紫外线、炎症、某些感染及化疗等医学处理会带来各自不同的损伤模式。那些在DNA修复或其他保护系统上存在遗传弱点的人,在正常组织中会积累更多突变,这也有助于解释为何某些家族的癌症风险明显更高。
当突变细胞获得优势时
大多数突变是无害的“乘客”,但有些会改变控制生长、生存或修复的关键基因。携带这些“驱动”突变的细胞可以相较邻居获得微小但重要的优势,使其克隆扩张。例如在血液中,携带特定驱动突变的干细胞随年龄变得更常见,这种状况称为克隆性造血,能提高血液癌症以及某些心脏和肝脏疾病的风险。在许多表面组织——如皮肤、食管、气道、膀胱、胃和子宫——携带与癌症相关的驱动基因(如NOTCH1、TP53或PIK3CA)的细胞斑块会在外观正常的组织中扩散。这些突变常常出现在令人惊讶的早期,甚至童年时期,并能在显微镜下任何可见的癌前病变出现之前重塑大片组织区域。
并非所有克隆都走向癌症
克隆演化在不同器官中表现各异,克隆扩张并不必然导致癌症。在结肠、前列腺和肝脏等结构中,干细胞生活在小而物理上分隔的单元中,这限制了单一克隆的扩展范围。有些克隆的出现并非为了促进肿瘤生长,而是为了帮助细胞在压力下生存。例如,在慢性炎症或代谢疾病中,细胞可能获得能抑制有害信号或减少毒性损伤的突变,这是一种“适应性救援”形式。其他突变,例如食管中某些Notch通路的改变,甚至可能减缓新生肿瘤的生长,暗示某些突变克隆可能对抗癌具有保护作用。在携带驱动突变的众多克隆中,只有少数获得了成为危险克隆所需的额外改变。
从正常细胞到癌症的漫长道路
通过拼凑同一受检者的正常组织、癌前增生和肿瘤中的突变图谱,研究者现在可以重建癌症发生的大致时间线。在血液疾病和乳腺癌中,最初的驱动突变常常在诊断前数十年就已出现,随后是缓慢的克隆增长,之后再次出现的打击最终触发明显的疾病。然而关键问题仍未解:哪些突变组合与环境因素促使某个克隆越过阈值,为什么一些高风险克隆从不进展,以及细胞“软件”(表观遗传标记)如何与DNA突变相互作用。随着工具的改进,绘制这些隐秘的克隆史可能使血液或组织检测早期识别高风险克隆成为可能,指导如戒烟或感染控制等预防策略,并最终将癌症医学转向在肿瘤形成多年之前进行干预。 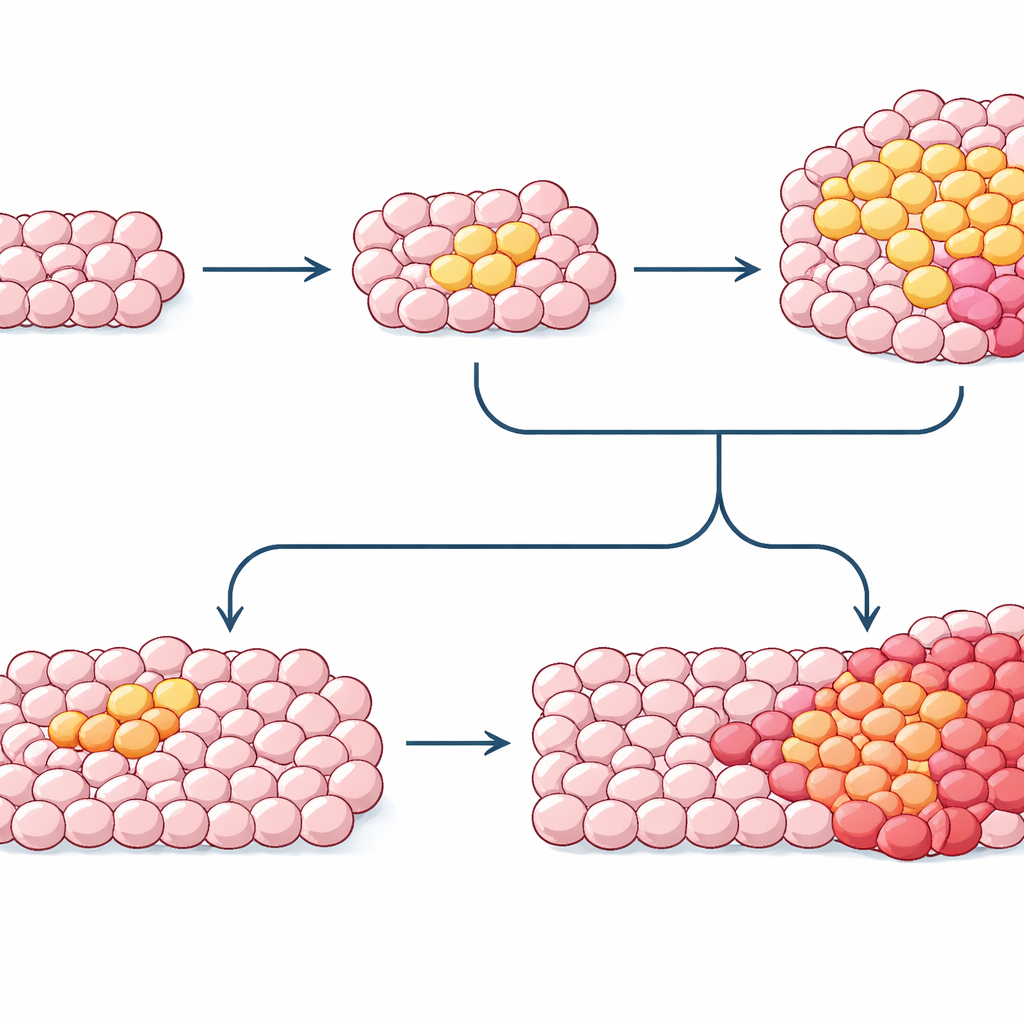
这对日常健康意味着什么
本文表明,癌症并非突发事件,而是发生在正常组织内一段漫长且大多无声的进化过程的终点。我们的细胞在年龄、基因和环境的共同作用下不断变化,许多细胞在疾病出现之前就已携带突变。通过识别哪些类型的克隆增长是危险的、哪些是无害甚至具保护性的,以及生活方式或遗传因素如何改变这种平衡,科学家希望设计更聪明的筛查方案、个性化风险评估,并开发将细胞演化引导远离癌症的干预手段。
引用: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
关键词: 体细胞突变, 克隆演化, 正常组织, 癌症风险, 早期致癌