Clear Sky Science · es
Mutaciones somáticas y evolución clonal en tejidos normales y desarrollo del cáncer
Cambios ocultos dentro de células sanas
Mucho antes de que un tumor pueda verse en una exploración o palparse como un bulto, nuestras células van acumulando silenciosamente cambios genéticos a medida que envejecemos, reaccionamos al entorno y repararnos del desgaste diario. Este artículo de revisión explica cómo estos cambios invisibles, llamados mutaciones somáticas, se acumulan en tejidos aparentemente normales, cómo ciertas mutaciones confieren a algunas células una ventaja competitiva y cómo la lenta “evolución clonal” durante décadas puede, finalmente, preparar el terreno para el cáncer. Entender este paisaje oculto está redefiniendo las ideas sobre cuándo comienza realmente el cáncer y cómo podríamos detectarlo o prevenirlo mucho antes en la vida.
Cómo los científicos rastrean pequeñas familias celulares
Los tejidos normales son mosaicos de muchas pequeñas familias de células, o clones, y la mayoría son demasiado pequeños para estudiarse con métodos antiguos. La revisión describe nuevas herramientas que permiten a los investigadores leer ADN de muy pocas células con notable precisión. Un enfoque es recortar piezas diminutas de tejido mediante microdisección láser y secuenciar todo el ADN contenido, ofreciendo una instantánea de cómo se disponen los clones en el espacio. Otro consiste en cultivar versiones en miniatura de órganos, llamadas organoides, a partir de células individuales y secuenciar a sus descendientes, revelando la historia personal de mutaciones de cada célula. Una tercera estrategia emplea secuenciación ultra precisa que puede detectar mutaciones raras en mezclas celulares grandes sin necesidad de cultivarlas. Juntas, estas técnicas muestran que incluso los tejidos “saludables” están llenos de células que portan mutaciones similares a las del cáncer. 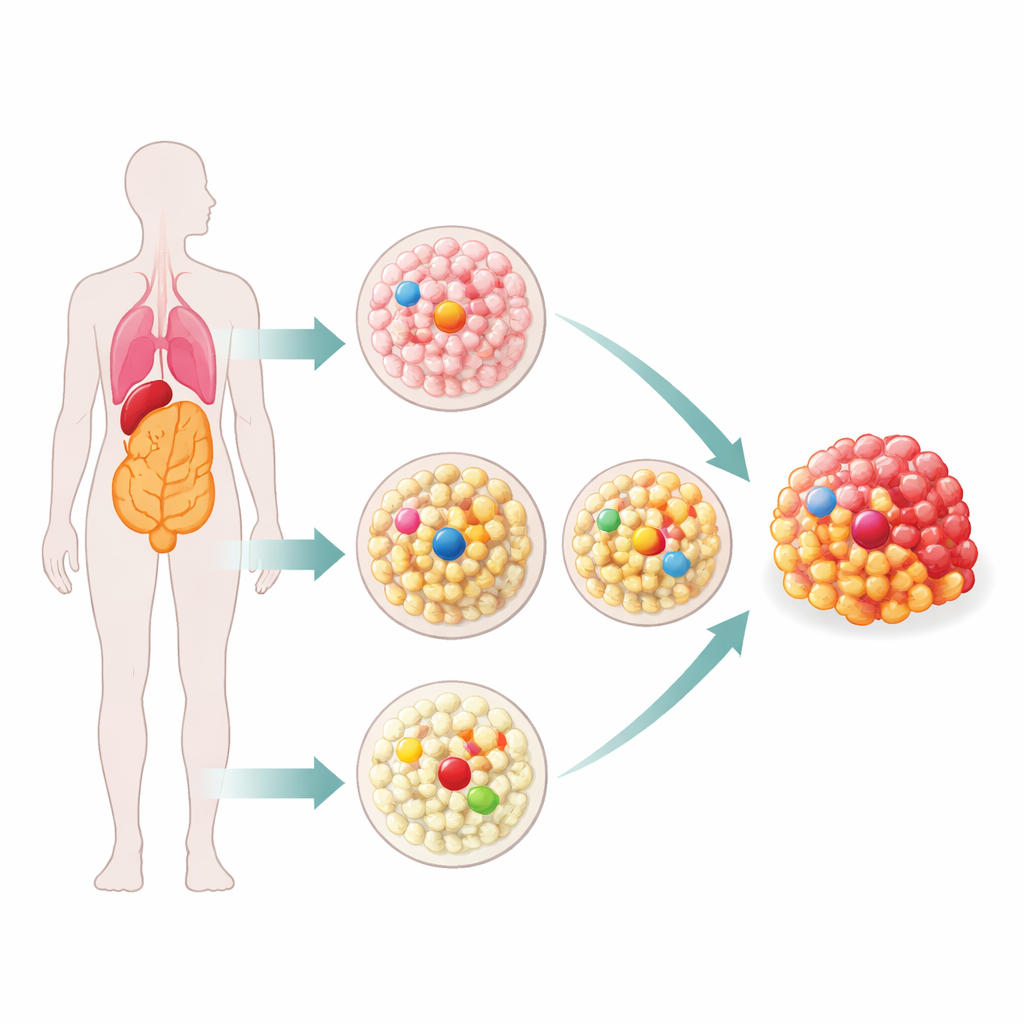
Por qué las mutaciones siguen apareciendo
Las mutaciones en células normales surgen de dos grandes fuentes: el desgaste interno y las exposiciones externas. Desde nuestras primeras divisiones celulares en el embrión, la copia del ADN es imperfecta, y las reacciones químicas dentro de las células dañan lentamente el material genético con el tiempo. Estos procesos relacionados con la edad dejan “firmas” características en el ADN que se observan en muchos órganos, incluso en células longevas como neuronas y músculo. Además de esto, influencias externas como el humo del tabaco, el alcohol, la luz ultravioleta, la inflamación, ciertas infecciones y tratamientos médicos como la quimioterapia añaden sus propios patrones distintivos de daño. Las personas nacidas con debilidades hereditarias en la reparación del ADN u otros sistemas protectores pueden acumular muchas más mutaciones en tejidos normales, lo que ayuda a explicar por qué algunas familias tienen riesgos de cáncer mucho más altos.
Cuando las células mutadas obtienen una ventaja
La mayoría de las mutaciones son pasajeros inofensivos, pero algunas alteran genes clave que controlan el crecimiento, la supervivencia o la reparación. Las células que portan estas mutaciones “impulsoras” pueden adquirir una ventaja pequeña pero importante sobre sus vecinas, permitiendo que su clone se expanda. En la sangre, por ejemplo, las células madre con mutaciones impulsoras específicas se vuelven más comunes con la edad, una condición llamada hemopoyesis clonal que aumenta el riesgo de cánceres hematológicos y de algunas enfermedades cardíacas y hepáticas. En muchos tejidos superficiales—como la piel, el esófago, las vías respiratorias, la vejiga, el estómago y el útero—parches de células que llevan impulsores asociados al cáncer como NOTCH1, TP53 o PIK3CA se extienden por tejido que por lo demás parece normal. A menudo estas mutaciones aparecen sorprendentemente temprano en la vida, incluso en la infancia, y pueden remodelar grandes áreas de tejido mucho antes de que cualquier lesión precancerosa sea visible al microscopio.
No todos los clones avanzan hacia el cáncer
La evolución clonal se desarrolla de forma diferente según el órgano, y la expansión de un clone no significa automáticamente que vaya a surgir cáncer. En estructuras como el colon, la próstata y el hígado, las células madre viven en unidades pequeñas y físicamente separadas, lo que limita hasta dónde puede propagarse un solo clone. Algunos clones surgen no para promover tumores sino para ayudar a las células a sobrevivir al estrés. Por ejemplo, en enfermedades inflamatorias crónicas o metabólicas, las células pueden adquirir mutaciones que atenúan señales dañinas o reducen el daño tóxico, una forma de “rescate adaptativo”. Otras mutaciones, como ciertos cambios en la vía Notch en el esófago, pueden incluso ralentizar el crecimiento de tumores emergentes, lo que sugiere que algunos clones mutantes podrían proteger contra el cáncer. Solo una pequeña fracción de los muchos clones que portan mutaciones impulsoras parece adquirir las alteraciones adicionales necesarias para volverse peligrosos.
El largo camino de la célula normal al cáncer
Al ensamblar patrones de mutación de tejido normal, crecimientos precancerosos y tumores en la misma persona, los investigadores pueden ahora reconstruir cronologías aproximadas del desarrollo del cáncer. En trastornos sanguíneos y en el cáncer de mama, las mutaciones impulsoras iniciales suelen surgir décadas antes del diagnóstico, con un crecimiento clonal lento seguido de golpes posteriores que finalmente desencadenan la enfermedad manifiesta. Sin embargo, siguen abiertas preguntas clave: qué combinaciones de mutaciones y factores ambientales empujan a un clone más allá del límite, por qué algunos clones de alto riesgo nunca progresan y cómo interactúan los cambios en el “software” celular (marcas epigenéticas) con las mutaciones del ADN. A medida que mejoren las herramientas, mapear estas historias clonales ocultas podría permitir pruebas en sangre o tejido que detecten clones riesgosos temprano, orientar estrategias de prevención como dejar de fumar o el control de infecciones y, en última instancia, desplazar la medicina oncológica hacia la intervención años antes de que se forme un tumor. 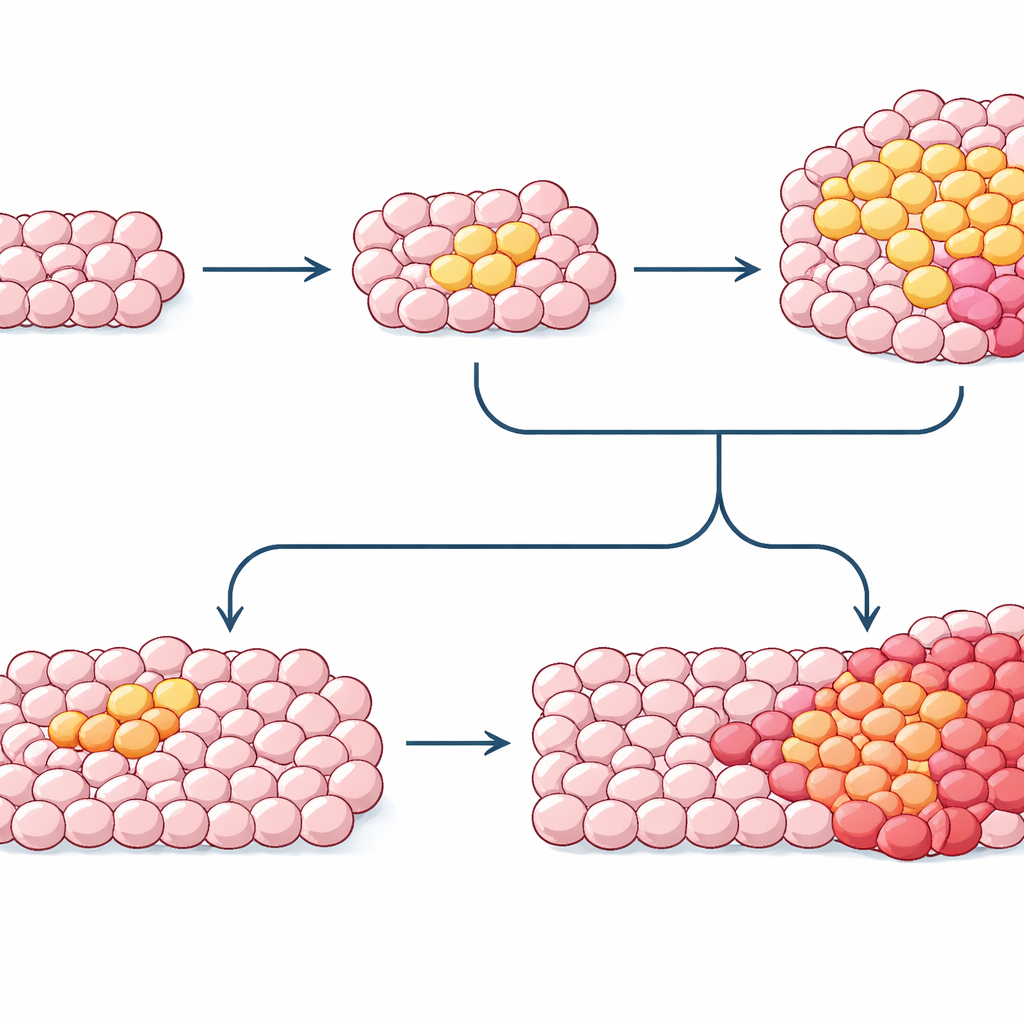
Qué significa esto para la salud cotidiana
Este artículo muestra que el cáncer no es un evento repentino sino el punto final de un largo y mayormente silencioso proceso evolutivo que ocurre dentro de tejidos normales. Nuestras células cambian constantemente, moldeadas por la edad, los genes y el entorno, y muchas portan mutaciones mucho antes de que aparezca cualquier enfermedad. Al aprender qué tipos de crecimiento clonal son peligrosos, cuáles son inocuos o incluso protectores y cómo factores de estilo de vida o hereditarios inclinan la balanza, los científicos esperan diseñar cribados más inteligentes, personalizar estimaciones de riesgo y desarrollar maneras de orientar la evolución celular para alejarla del cáncer.
Cita: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
Palabras clave: mutaciones somáticas, evolución clonal, tejidos normales, riesgo de cáncer, carcinogénesis temprana