Clear Sky Science · fr
Mutations somatiques et évolution clonale dans les tissus normaux et le développement du cancer
Changements cachés à l’intérieur des cellules saines
Bien avant qu’une tumeur ne soit visible à l’imagerie ou palpable comme une masse, nos cellules accumulent silencieusement des altérations génétiques au fil du vieillissement, des réactions à l’environnement et des processus de réparation. Cet article de synthèse explique comment ces modifications invisibles, appelées mutations somatiques, s’accumulent dans des tissus par ailleurs normaux, comment certaines mutations confèrent à quelques cellules un avantage compétitif et comment une lente « évolution clonale » sur des décennies peut finalement préparer le terrain pour un cancer. Comprendre ce paysage caché transforme les idées sur le moment où le cancer commence réellement et sur la manière dont on pourrait le détecter ou le prévenir beaucoup plus tôt dans la vie.
Comment les scientifiques suivent de petites familles cellulaires
Les tissus normaux sont des mosaïques de nombreuses petites familles cellulaires, ou clones, dont la plupart sont trop petites pour être étudiées avec les méthodes anciennes. La revue décrit de nouveaux outils qui permettent aux chercheurs de lire l’ADN à partir d’un très petit nombre de cellules avec une précision remarquable. Une approche consiste à prélever des fragments microscopiques de tissu par microdissection laser et à séquencer tout l’ADN contenu, offrant un instantané de la disposition spatiale des clones. Une autre consiste à cultiver des versions miniatures d’organes, appelées organoïdes, à partir d’une seule cellule et à séquencer ces descendants, révélant l’histoire mutationnelle propre à chaque cellule. Une troisième stratégie utilise un séquençage ultra-précis capable de détecter des mutations rares dans de grands mélanges cellulaires sans nécessité de culture. Ensemble, ces techniques montrent que même les tissus « sains » regorgent de cellules portant des mutations de type cancéreux. 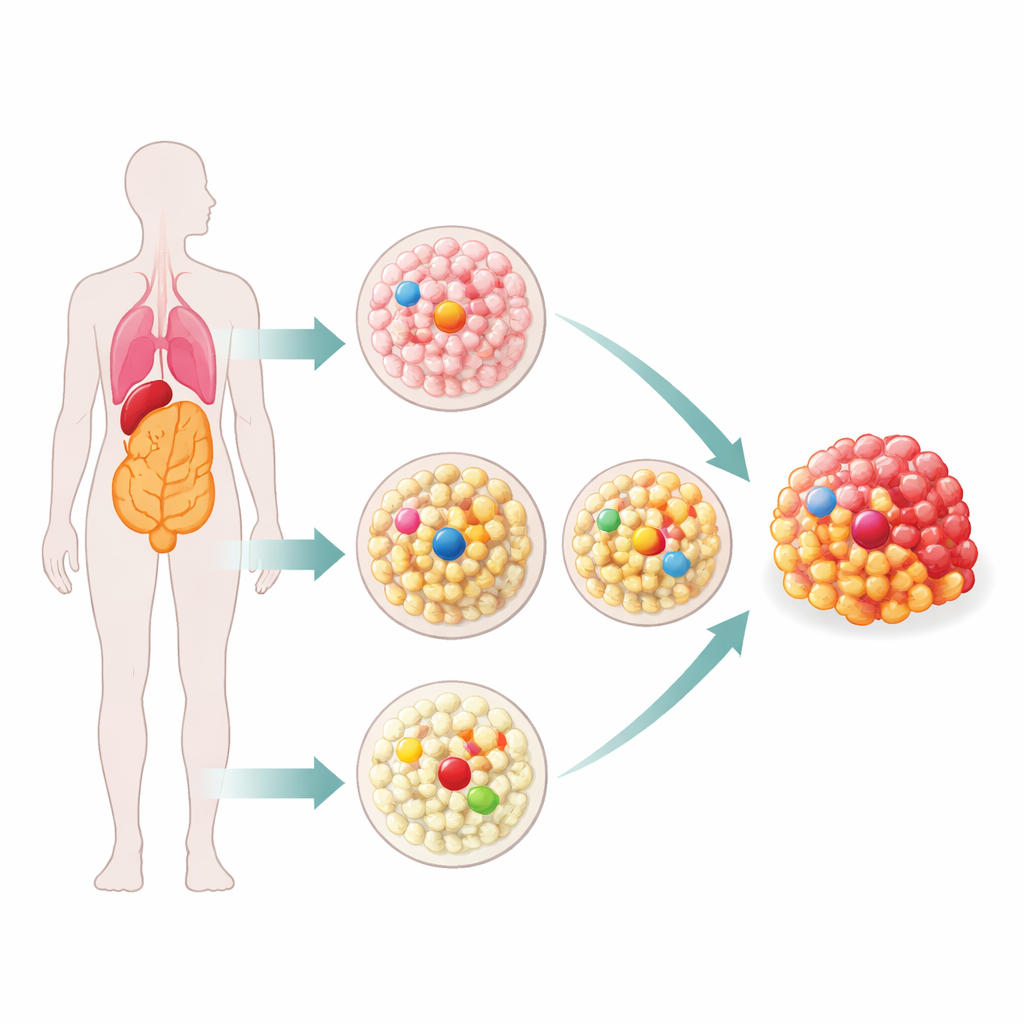
Pourquoi les mutations continuent d’apparaître
Les mutations dans les cellules normales proviennent de deux grandes sources : l’usure interne et les expositions externes. Dès les premières divisions cellulaires de l’embryon, la copie de l’ADN est imparfaite, et des réactions chimiques à l’intérieur des cellules endommagent progressivement le matériel génétique au fil du temps. Ces processus liés à l’âge laissent des « signatures » caractéristiques dans l’ADN observées dans de nombreux organes, y compris dans des cellules longeves comme les neurones et les cellules musculaires. Par-dessus cela, des facteurs externes tels que la fumée de tabac, l’alcool, les rayons ultraviolets, l’inflammation, certaines infections et des traitements médicaux comme la chimiothérapie ajoutent leurs propres schémas de dommages distincts. Les personnes nées avec des faiblesses héritées dans la réparation de l’ADN ou d’autres systèmes protecteurs peuvent accumuler beaucoup plus de mutations dans des tissus normaux, ce qui aide à expliquer pourquoi certaines familles présentent des risques de cancer beaucoup plus élevés.
Quand les cellules mutées prennent l’avantage
La plupart des mutations sont des passagers sans conséquence, mais certaines affectent des gènes clés qui contrôlent la croissance, la survie ou la réparation. Les cellules porteuses de ces mutations « conductrices » peuvent obtenir un avantage, certes faible mais significatif, par rapport à leurs voisines, permettant à leur clone de s’étendre. Dans le sang, par exemple, des cellules souches avec des mutations conductrices spécifiques deviennent plus fréquentes avec l’âge, un état appelé hématopoïèse clonale qui augmente le risque de cancers du sang et de certaines maladies cardiaques et hépatiques. Dans de nombreux tissus de surface — comme la peau, l’œsophage, les voies aériennes, la vessie, l’estomac et l’utérus — des îlots de cellules portant des mutations associées au cancer telles que NOTCH1, TP53 ou PIK3CA se propagent dans des tissus par ailleurs normaux. Souvent, ces mutations apparaissent de manière surprenante tôt dans la vie, parfois dès l’enfance, et peuvent remodeler de larges zones de tissu bien avant qu’une lésion précancéreuse ne soit visible au microscope.
Tous les clones ne glissent pas vers le cancer
L’évolution clonale se déroule différemment selon les organes, et l’expansion d’un clone ne signifie pas automatiquement qu’un cancer suivra. Dans des structures telles que le côlon, la prostate et le foie, les cellules souches résident dans de petites unités physiquement séparées, limitant l’étendue qu’un clone peut atteindre. Certains clones n’apparaissent pas pour promouvoir les tumeurs mais pour aider les cellules à survivre au stress. Par exemple, dans des maladies inflammatoires chroniques ou métaboliques, les cellules peuvent acquérir des mutations qui atténuent des signaux nocifs ou réduisent les dommages toxiques, une forme de « sauvetage adaptatif ». D’autres mutations, comme certaines altérations de la voie Notch dans l’œsophage, peuvent même ralentir la croissance de tumeurs émergentes, ce qui suggère que certains clones mutants pourraient protéger contre le cancer. Seule une petite fraction des nombreux clones porteurs de mutations conductrices semble acquérir les altérations supplémentaires nécessaires pour devenir dangereuse.
La longue route de la cellule normale au cancer
En reconstituant les modèles de mutations dans des tissus normaux, des croissances précancéreuses et des tumeurs chez une même personne, les chercheurs peuvent désormais reconstruire des chronologies approximatives du développement du cancer. Dans les maladies du sang et le cancer du sein, les premières mutations conductrices apparaissent souvent des décennies avant le diagnostic, avec une croissance clonale lente suivie de coups supplémentaires qui déclenchent finalement la maladie manifeste. Pourtant, des questions essentielles demeurent : quelles combinaisons de mutations et de facteurs environnementaux poussent un clone au-delà du seuil, pourquoi certains clones à haut risque ne progressent jamais et comment les changements de « logiciel » cellulaire (marques épigénétiques) interagissent avec les mutations de l’ADN. À mesure que les outils s’améliorent, cartographier ces histoires clonales cachées pourrait permettre des tests sanguins ou tissulaires identifiant tôt les clones à risque, orienter des stratégies de prévention — comme l’arrêt du tabac ou le contrôle des infections — et, au final, faire basculer la médecine oncologique vers des interventions des années avant la formation d’une tumeur. 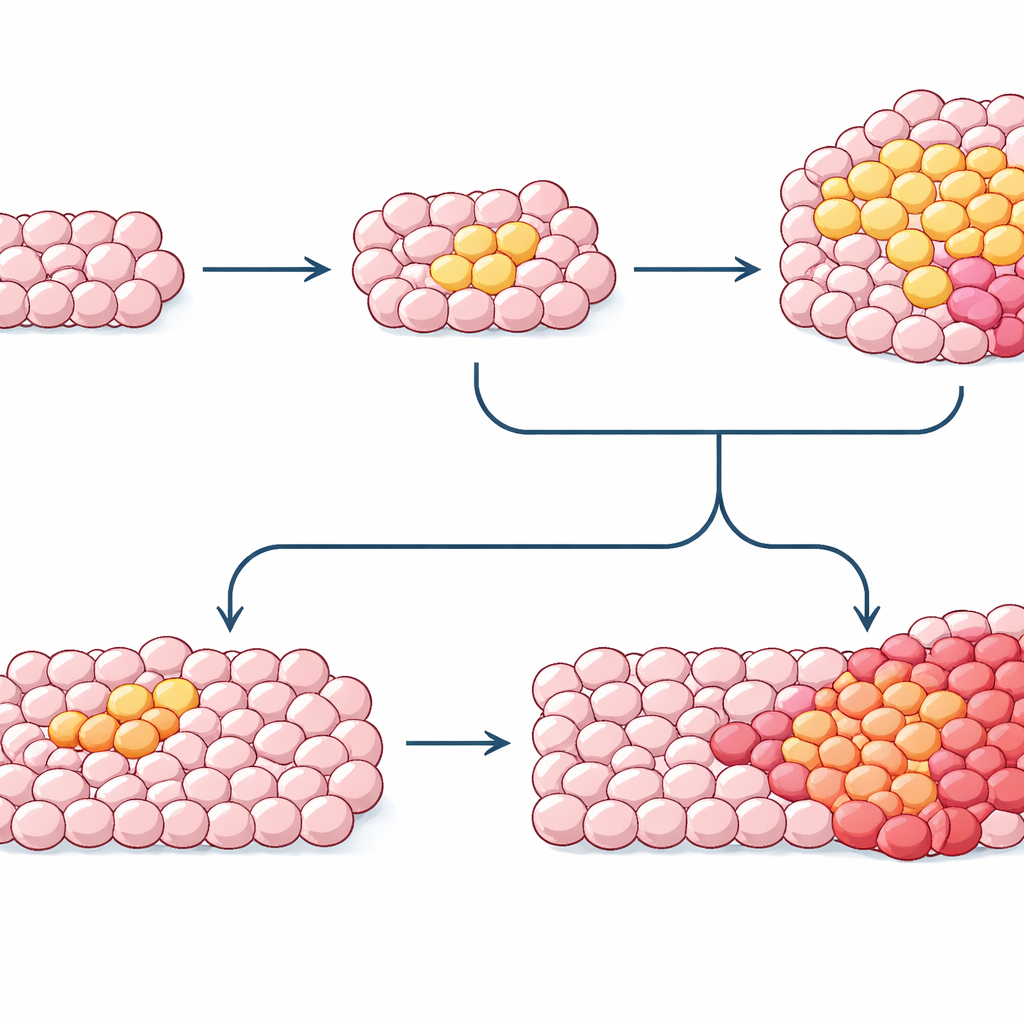
Ce que cela signifie pour la santé quotidienne
Cet article montre que le cancer n’est pas un événement soudain mais l’aboutissement d’un long processus évolutif majoritairement silencieux qui se déroule dans des tissus normaux. Nos cellules changent en permanence, modelées par l’âge, les gènes et l’environnement, et beaucoup portent des mutations bien avant l’apparition d’une maladie. En identifiant quels types de croissances clonales sont dangereuses, lesquelles sont inoffensives ou même protectrices, et comment les facteurs liés au mode de vie ou hérités inclinent la balance, les scientifiques espèrent concevoir un dépistage plus intelligent, affiner les estimations de risque et développer des moyens d’orienter l’évolution cellulaire loin du cancer.
Citation: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
Mots-clés: mutations somatiques, évolution clonale, tissus normaux, risque de cancer, carcinogenèse précoce