Clear Sky Science · nl
Somatische mutaties en clonale evolutie in normale weefsels en kankerontwikkeling
Verborgen veranderingen binnen gezonde cellen
Lang voordat een tumor zichtbaar is op een scan of voelbaar als een knobbel, verzamelen onze cellen stilletjes genetische veranderingen naarmate we ouder worden, reageren op onze omgeving en herstellen van dagelijkse slijtage. Dit overzichtsartikel legt uit hoe deze onzichtbare veranderingen, somatische mutaties genoemd, zich ophopen in anders normale weefsels, hoe bepaalde mutaties sommige cellen een concurrentievoordeel geven en hoe langzaam werkende “clonale evolutie” over decennia uiteindelijk het toneel voor kanker kan bereiden. Inzicht in dit verborgen landschap verandert ideeën over wanneer kanker echt begint en hoe we het veel eerder in het leven zouden kunnen detecteren of voorkomen.
Hoe wetenschappers kleine celgezinnen volgen
Normale weefsels zijn mozaïeken van vele kleine celgezinnen, of klonen, en de meeste zijn te klein om met oudere methoden te bestuderen. Het overzicht beschrijft nieuwe instrumenten waarmee onderzoekers het DNA van zeer weinig cellen met opmerkelijke precisie kunnen lezen. Eén benadering is het uitnemen van piepkleine weefselstukjes met lasergebaseerde microdissectie en het volledig sequentiëren van het DNA daarin, wat een momentopname geeft van hoe klonen ruimtelijk zijn gerangschikt. Een andere is het kweken van miniatuurversies van organen, organoïden genoemd, uit enkele cellen en het sequentiëren van die afstammelingen, waardoor de persoonlijke mutatiegeschiedenis van elke cel zichtbaar wordt. Een derde strategie gebruikt extreem nauwkeurige sequencering die zeldzame mutaties in grote celmengsels kan opsporen zonder ze te hoeven kweken. Samen laten deze technieken zien dat zelfs “gezonde” weefsels vol zitten met cellen die kankervergelijkbare mutaties dragen. 
Waarom mutaties blijven verschijnen
Mutaties in normale cellen ontstaan door twee grote bronnen: interne slijtage en externe blootstellingen. Vanaf onze allereerste celdelingen in het embryo is het kopiëren van DNA onvolmaakt, en chemische reacties binnen cellen beschadigen het genetisch materiaal langzaam in de loop van de tijd. Deze leeftijdsgerelateerde processen laten karakteristieke “signaturen” in het DNA achter die in veel organen te zien zijn, zelfs in langlevende cellen zoals neuronen en spiercellen. Daarbovenop voegen externe invloeden zoals tabaksrook, alcohol, ultraviolet licht, ontsteking, bepaalde infecties en medische behandelingen zoals chemotherapie hun eigen kenmerkende schadepatronen toe. Mensen die geboren zijn met erfelijke zwaktes in DNA-reparatie of andere beschermende systemen kunnen veel meer mutaties in normale weefsels opstapelen, wat helpt verklaren waarom sommige families veel hogere kankerrisico’s hebben.
Wanneer gemuteerde cellen een voordeel krijgen
De meeste mutaties zijn onschuldige passagiers, maar sommige veranderen sleutelgenen die groei, overleving of reparatie regelen. Cellen met deze “driver”-mutaties kunnen een klein maar belangrijk voordeel ten opzichte van hun buren krijgen, waardoor hun kloon kan uitbreiden. In bloed bijvoorbeeld worden stamcellen met specifieke driver-mutaties met het ouder worden vaker, een toestand die clonaal hematopoëse wordt genoemd en die het risico op bloedkankers en sommige hart- en leverziekten verhoogt. In veel oppervlaktelagen—zoals huid, slokdarm, luchtwegen, blaas, maag en baarmoeder—verspreiden zich pleisters cellen die kankergeassocieerde drivers dragen zoals NOTCH1, TP53 of PIK3CA over anders normaal ogend weefsel. Vaak verschijnen deze mutaties verrassend vroeg in het leven, zelfs in de kindertijd, en kunnen ze grote gebieden weefsel herstructureren lang voordat een precancereuze laesie onder de microscoop zichtbaar is.
Niet alle klonen bewegen richting kanker
Clonale evolutie verloopt per orgaan verschillend, en een uitgebreide kloon betekent niet automatisch dat er kanker zal volgen. In structuren zoals de dikke darm, prostaat en lever leven stamcellen in kleine, fysiek gescheiden eenheden, wat beperkt hoe ver één kloon kan uitzaaien. Sommige klonen ontstaan niet om tumoren te bevorderen maar om cellen te helpen stress te doorstaan. Bijvoorbeeld, bij chronische inflammatoire of metabole ziekten kunnen cellen mutaties verwerven die schadelijke signalering dempen of toxische schade verminderen, een vorm van “adaptieve redding.” Andere mutaties, zoals bepaalde veranderingen in de Notch-route in de slokdarm, kunnen zelfs de groei van opkomende tumoren vertragen, wat suggereert dat sommige gemuteerde klonen tegen kanker zouden kunnen beschermen. Slechts een klein deel van de vele klonen met driver-mutaties lijkt de aanvullende veranderingen te verwerven die nodig zijn om gevaarlijk te worden.
De lange weg van normale cel naar kanker
Door mutatiepatronen van normaal weefsel, precancereuze groei en tumoren bij dezelfde persoon samen te brengen, kunnen onderzoekers nu ruwe tijdlijnen van kankerontwikkeling reconstrueren. Bij bloedziekten en borstkanker ontstaan de eerste driver-mutaties vaak decennia vóór de diagnose, met trage clonale groei gevolgd door latere inslagen die uiteindelijk de zichtbare ziekte ontketenen. Toch blijven belangrijke vragen: welke combinaties van mutaties en omgevingsfactoren duwen een kloon over de rand, waarom sommige hoog-risico klonen nooit doorgroeien en hoe veranderingen in de cellulaire “software” (epigenetische merken) met DNA-mutaties samenwerken. Naarmate de instrumenten verbeteren, kan het in kaart brengen van deze verborgen clonale geschiedenissen bloed- of weefseltests mogelijk maken die risicovolle klonen vroeg signaleren, preventiestrategieën zoals stoppen met roken of infectiebestrijding sturen en uiteindelijk de oncologie verschuiven naar ingrijpen jaren voordat een tumor ontstaat. 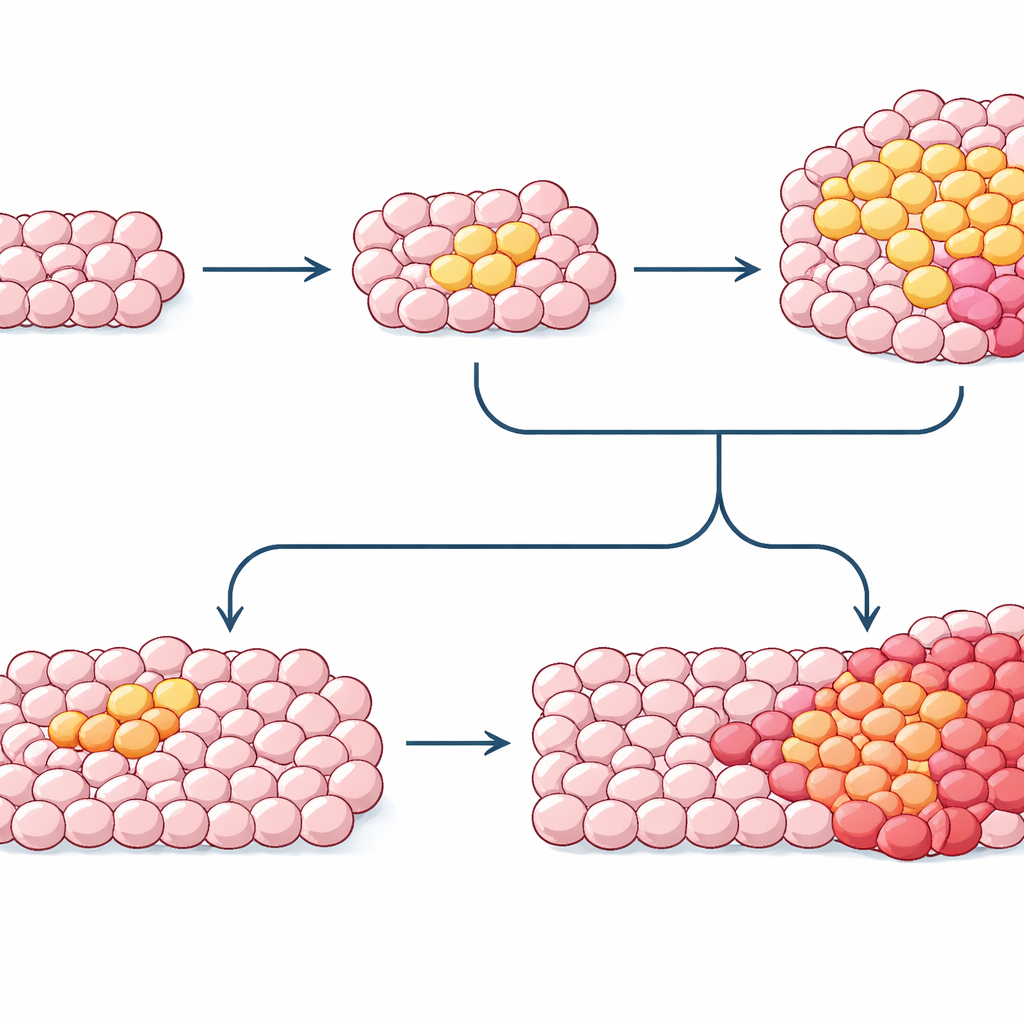
Wat dit betekent voor alledaagse gezondheid
Dit artikel laat zien dat kanker geen plotseling voorval is maar het eindpunt van een lang, grotendeels stil evolutionair proces dat plaatsvindt in normale weefsels. Onze cellen veranderen voortdurend, gevormd door leeftijd, genen en omgeving, en velen dragen mutaties lang voordat een ziekte zichtbaar wordt. Door te leren welke vormen van clonale groei gevaarlijk zijn, welke onschadelijk of zelfs beschermend zijn en hoe leefstijl- of erfelijke factoren het evenwicht beïnvloeden, hopen wetenschappers slimmer te screenen, risicobeoordelingen op maat te maken en manieren te ontwikkelen om cellulaire evolutie weg van kanker te sturen.
Bronvermelding: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
Trefwoorden: somatische mutaties, clonale evolutie, normale weefsels, kankerrisico, vroege carcinogenese